এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞানের একটি গুরুত্বপূর্ণ প্রশ্ন “\(2H_2+O_2=2H_2O\) এই সমীকরণ থেকে কী কী তথ্য জানা যায়?” নিয়ে আলোচনা করব। এই প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞান পরীক্ষার জন্য অত্যন্ত গুরুত্বপূর্ণ। এই “\(2H_2+O_2=2H_2O\) এই সমীকরণ থেকে কী কী তথ্য জানা যায়?” প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞানের তৃতীয় অধ্যায় “রাসায়নিক গণনা“ -এর একটি গুরুত্বপূর্ণ প্রশ্ন। এই প্রশ্নটি মাধ্যমিক পরীক্ষায় এবং চাকরির পরীক্ষায় প্রায়ই দেখা যায়।

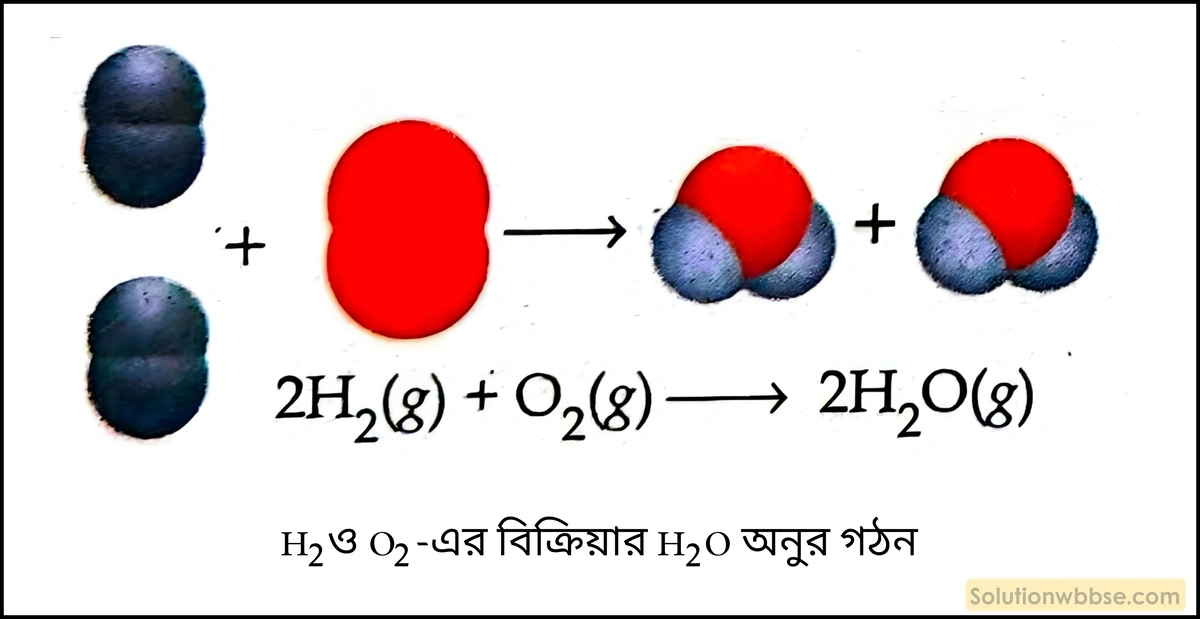
\(2H_2+O_2=2H_2O\) এই সমীকরণ থেকে কী কী তথ্য জানা যায়?
\(2H_2+O_2=2H_2O\) এই সমীকরণ থেকে আমরা যে যে তথ্য পাই সেগুলি নীচে দেওয়া হল –
গুণগত তথ্য –
1. বিক্রিয়কের নাম হাইড্রোজেন ও অক্সিজেন এবং তাদের সংকেত যথাক্রমে \(H_2\) ও \(O_2\)। বিক্রিয়াজাত পদার্থ হল জল ও তার সংকেত \(H_2O\)।
2. হাইড্রোজেনের চিহ্ন হল \(H\) এবং অক্সিজেনের চিহ্ন হল \(O\)।
3. জল হল হাইড্রোজেন ও অক্সিজেন মৌলের একটি যৌগিক পদার্থ।
পরিমাণগত তথ্য –
- \(2\)-অণু হাইড্রোজেন এবং \(1\)-অণু অক্সিজেনের পারস্পরিক বিক্রিয়ায় \(2\)-অণু জল গঠিত হয়। \(4\)-পরমাণু হাইড্রোজেন এবং \(2\)-পরমাণু অক্সিজেন অর্থাৎ মোট \(6\)টি পরমাণু দিয়ে \(2\)-অণু জল সৃষ্টি হয়।
- \(\underset{2\times\left(2\times1\right)=4}{2H_2}+\underset{2\times16=32}{O_2}=\underset{2\left(2\times1+16\right)=36}{2H_2O}\) \(4\) ভাগ ওজনের হাইড্রোজেন ও \(32\) ভাগ ওজনের অক্সিজেনের সঙ্গে রাসায়নিক বিক্রিয়া করে \(36\) ভাগ ওজনের জল উৎপন্ন করে। \(H_2\), \(O_2\) এবং \(H_2O\) -এর ওজনগত অনুপাত হল \(4:32:36\) বা \(1:8:9\)।
- গ্যাসীয় অবস্থায় হাইড্রোজেন ও অক্সিজেন যুক্ত হয়ে স্টিম উৎপন্ন করলে যদি প্রত্যেকটির আয়তন একই উষ্ণতা ও চাপে নির্ণীত হয়, তবে তাদের আয়তনগত অনুপাত হয় \(2:1:2\)।
- \(4\) ভাগ ভরের \(H\) এবং \(32\) ভাগ ভরের \(O\) অর্থাৎ মোট \(36\) ভাগ ভরের বিক্রিয়ক উৎপন্ন করে \(36\) ভাগ ভরের জল অর্থাৎ বিক্রিয়াজাত পদার্থ। উভয়পক্ষে মোট ভরের পরিমাণ সমান হওয়ায় নিশ্চিতরূপে জানা গেল যে, ভরের সংরক্ষণ সূত্র মান্য হয়।
এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞানের একটি গুরুত্বপূর্ণ প্রশ্ন “\(2H_2+O_2=2H_2O\) এই সমীকরণ থেকে কী কী তথ্য জানা যায়?” নিয়ে আলোচনা করব। এই প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞান পরীক্ষার জন্য অত্যন্ত গুরুত্বপূর্ণ। এই “\(2H_2+O_2=2H_2O\) এই সমীকরণ থেকে কী কী তথ্য জানা যায়?” প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞানের তৃতীয় অধ্যায় “রাসায়নিক গণনা“ -এর একটি গুরুত্বপূর্ণ প্রশ্ন। এই প্রশ্নটি মাধ্যমিক পরীক্ষায় এবং চাকরির পরীক্ষায় প্রায়ই দেখা যায়। আশা করি এই আর্টিকেলটি আপনাদের জন্য উপকারী হয়েছে। আপনাদের কোনো প্রশ্ন বা অসুবিধা থাকলে, আমাদের সাথে টেলিগ্রামে যোগাযোগ করুন।






Leave a Comment