এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞান বিষয়ের একটি অত্যন্ত গুরুত্বপূর্ণ প্রশ্ন — “NaCl -এর লুইস ডট চিত্র অঙ্কন করো।” — নিয়ে আলোচনা করব। এই প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞানের অষ্টম অধ্যায় “পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ” -এর “আয়নীয় ও সমযোজী বন্ধন” অংশ থেকে নেওয়া হয়েছে। মাধ্যমিক পরীক্ষা এবং বিভিন্ন চাকরির পরীক্ষায় এই প্রশ্নটি প্রায়ই আসে, তাই এটি শিক্ষার্থীদের জন্য বিশেষভাবে গুরুত্বপূর্ণ।

NaCl -এর লুইস ডট চিত্র অঙ্কন করো।
সোডিয়াম ক্লোরাইড (NaCl) অণুর গঠন – সোডিয়াম পরমাণুর ইলেকট্রন বিন্যাস হল 2, 8, 1 এবং ক্লোরিন পরমাণুর ইলেকট্রন বিন্যাস হল 2, 8, 7; সোডিয়াম পরমাণু তার সবচেয়ে বাইরের কক্ষের ইলেকট্রনটি ক্লোরিনের সবচেয়ে বাইরের কক্ষে স্থানান্তরিত করে এবং সোডিয়াম ও ক্লোরিন পরমাণু উভয়ই বাইরের কক্ষে 8টি ইলেকট্রন সংখ্যা পূর্ণ করে। Na পরমাণু একটি ইলেকট্রন বর্জন করায় তা Na+ আয়নে পরিণত হয় এবং Cl পরমাণু 1টি ইলেকট্রন গ্রহণ করায় তা Cl– আয়নে পরিণত হয়। অতঃপর Na+ এবং Cl– আয়ন স্থির তড়িৎ আকর্ষণ যুক্ত হয়ে NaCl অণু গঠন করে।
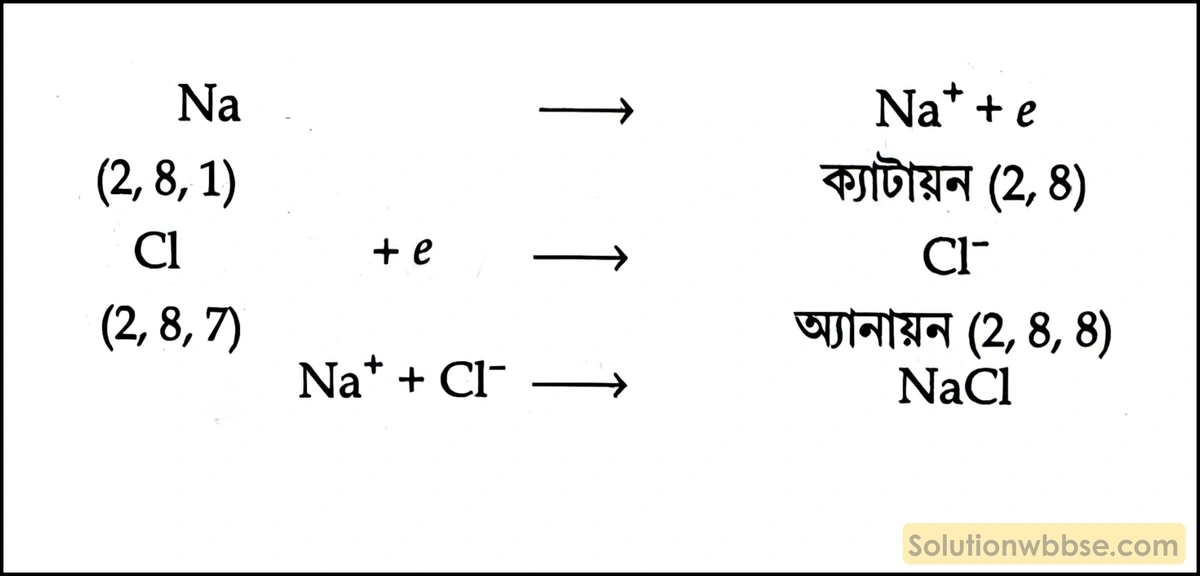
সোডিয়াম পরমাণু 1টি ইলেকট্রন বর্জন করে, তাই Na -এর যোজ্যতা = 1। আবার ক্লোরিন পরমাণু 1টি ইলেকট্রন গ্রহণ করে তাই ক্লোরিনের যোজ্যতা = 1।
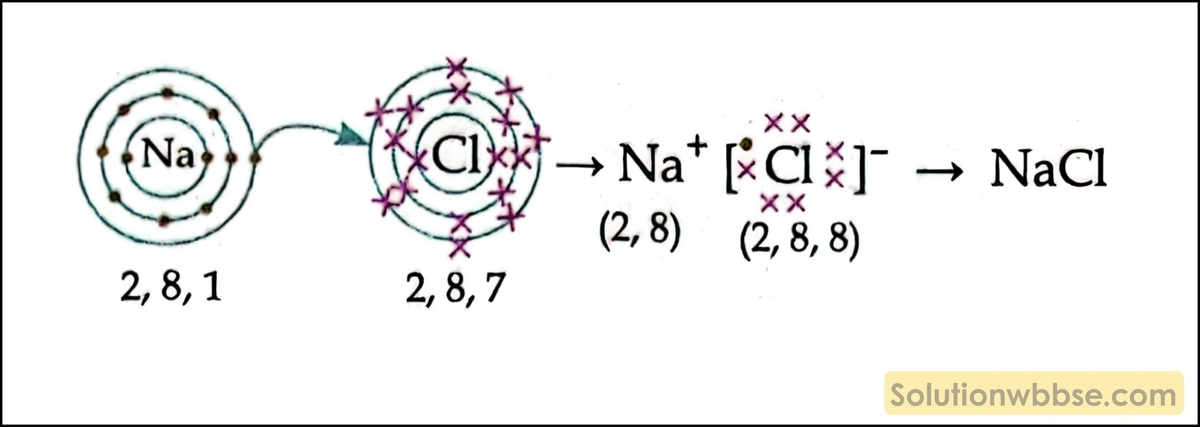
এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞান বিষয়ের একটি অত্যন্ত গুরুত্বপূর্ণ প্রশ্ন — “NaCl -এর লুইস ডট চিত্র অঙ্কন করো।” — নিয়ে আলোচনা করেছি। এই প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞানের অষ্টম অধ্যায় “পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ” -এর “আয়নীয় ও সমযোজী বন্ধন” অংশ থেকে নেওয়া হয়েছে। মাধ্যমিক পরীক্ষা এবং বিভিন্ন চাকরির পরীক্ষায় এই প্রশ্নটি প্রায়ই আসে, তাই এটি শিক্ষার্থীদের জন্য বিশেষভাবে গুরুত্বপূর্ণ। আশা করি এই আর্টিকেলটি আপনাদের জন্য উপকারী হয়েছে। আপনাদের কোনো প্রশ্ন বা অসুবিধা থাকলে, আমাদের সাথে টেলিগ্রামে যোগাযোগ করুন।






Leave a Comment