এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞানের একটি গুরুত্বপূর্ণ অংশ ‘বয়েলের সূত্র’ নিয়ে আলোচনা করব। এটি ‘গ্যাসের আচরণ’ অধ্যায়ের অন্তর্ভুক্ত। মাধ্যমিক পরীক্ষায় এই অংশ থেকে প্রায় প্রতি বছর প্রশ্ন আসে। এছাড়া, চাকরির পরীক্ষার প্রস্তুতির জন্যও এই আর্টিকেলটি আপনার জন্য গুরুত্বপূর্ণ হবে।

বয়েলের সূত্র –
প্রসারণশীলতা –
গ্যাসীয় পদার্থের অণুগুলির মধ্যে আন্তরাণবিক ব্যবধান বেশি থাকে এবং এদের অণুগুলির মধ্যে আন্তরাণবিক আকর্ষণ কম থাকে। ফলে গ্যাসের অণুগুলি সবসময় ছড়িয়ে পড়ার প্রবণতা দেখায় এবং এরা সর্বদা গতিশীল থাকে। গ্যাসের এই ধর্মকে প্রসারণশীলতা বলে।
অর্থাৎ, প্রসারণশীলতা হল গ্যাসের অণুর আয়তন বৃদ্ধির প্রবণতা। আবার, চাপ প্রয়োগ করলে বা উষ্ণতার হ্রাস করলে গ্যাসের আয়তন সংকোচনও হয়, একে সংকোচনশীলতা (Compressibility) বলে।
চাপ –
কোনো বদ্ধ পাত্রে রাখা গ্যাসের অণুগুলি সর্বদা গতিশীল। এরা পাত্রের দেয়ালের সঙ্গে এবং নিজেদের মধ্যে অনবরত সংঘর্ষ ঘটায়। পাত্রের দেয়ালের সঙ্গে সংঘর্ষ হলে দেয়ালে চাপ সৃষ্টি হয়। এই ধাক্কার কারণে পাত্রের দেয়ালের প্রতি একক ক্ষেত্রফলে লম্বভাবে যে বল প্রস্তুত হয় তাকে চাপ বলে।
অর্থাৎ, \(P=\frac FA\)
SI পদ্ধতিতে গ্যাসের চাপের একক নিউটন/বর্গমিটার (N/m2) এবং এটি প্যাস্কাল (Pa) নামে পরিচিত।
CGS পদ্ধতিতে চাপের একক ডাইন/বর্গসেমি (dyne/cm2)।
গ্যাসের চাপ পরিমাপের আর-একটি একক হল অ্যাটমস্ফিয়ার (atm)।
45° অক্ষাংশে 0°C অর্থাৎ 273 K উষ্ণতায় প্রমাণ অভিকর্ষজ ত্বরণে 76 সেমি পারদস্তম্ভের চাপকে এক অ্যাটমস্ফিয়ার (atm) বলে। বায়ুর চাপ মাপার অন্যান্য একক হল বার (bar) বা টর (torr)।
চাপের মাত্রীয় সংকেত –
চাপের মাত্রীয় সংকেত হল – ML-1T-2
চাপের এককের সম্পর্ক –
1 Pa = 10 dyne/cm2
1 bar = 106 dyne/cm2 = 105 Pa
1 torr = 1 mm পারদস্তম্ভের চাপ = 133.3 Pa
1 atm = 1.013 × 106 dyne/cm2
গ্যাসের চাপের পরিমাপ –
আবদ্ধ বায়ু বা গ্যাসের চাপ পরিমাপের জন্য ম্যানোমিটার, ব্যারোমিটার ইত্যাদি যন্ত্র ব্যবহার করা হয়ে থাকে। ম্যানোমিটার যন্ত্রকে চাপমান গেজও বলা হয়ে থাকে।
ম্যানোমিটার একটি U-আকৃতিবিশিষ্ট কাচের নল যা অ্যালকোহল বা পারদ ইত্যাদি তরল দ্বারা আংশিকভাবে পূরণ করা হয় এবং নলটির দুই বাহুর দৈর্ঘ্য অসমান হয়।
নিচের চিত্রে একটি খোলামুখ ম্যানোমিটার প্রদর্শিত হয়েছে। নলটির একটি মুখ গ্যাসপূর্ণ আবদ্ধ পাত্রের সঙ্গে যুক্ত থাকে এবং অপর মুখ বায়ুমণ্ডলে খোলা থাকে।
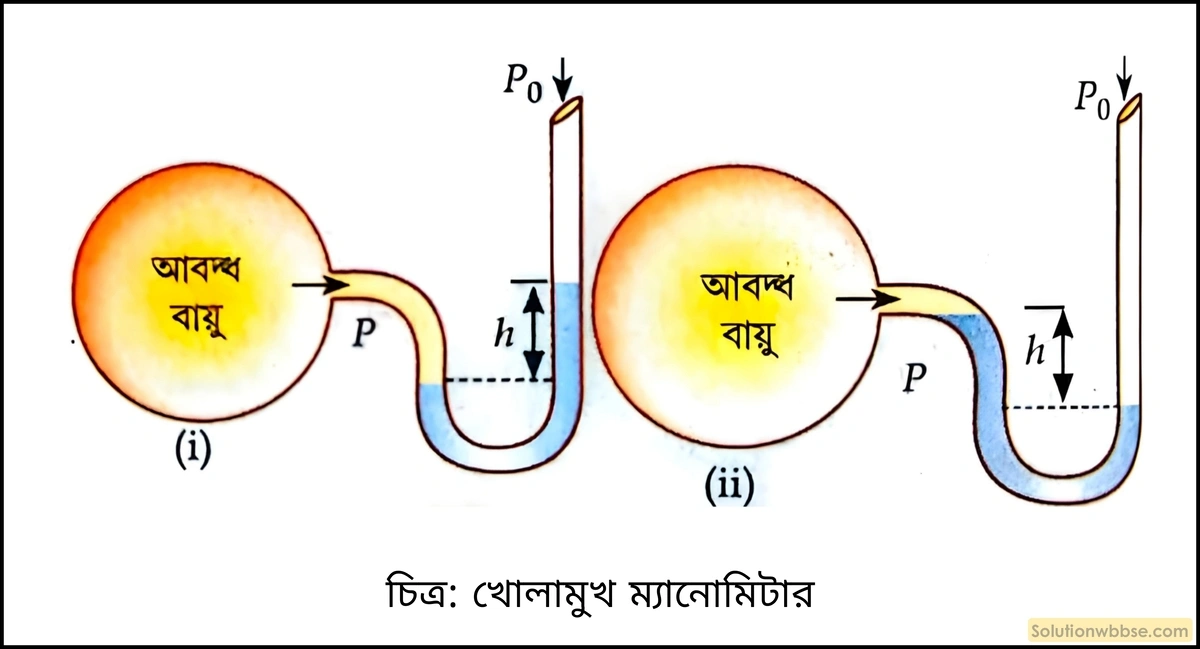
এখন, যদি আবদ্ধ পাত্রে গ্যাসের চাপ P বায়ুমণ্ডলের চাপ P0 অপেক্ষা বেশি হয় অর্থাৎ P > P0 হয় তবে ম্যানোমিটারের খোলা বাহুর তরলপৃষ্ঠ অপর বাহুর তরলপৃষ্ঠ থেকে ওপরে থাকবে [চিত্রে – (i)]। এখন ধরা যাক দুই বাহুর তরলস্তম্ভের উচ্চতার পার্থক্য h। ম্যানোমিটারের তরলের ঘনত্ব ρ হলে, P = P0 + hρg
আবার যদি P < P0 হয়, সেক্ষেত্রে P = P0 – hρg
(P – P0) রাশিটিকে গেজ চাপ বলে। এই পদ্ধতিতে বায়ুমণ্ডলের চাপ জানা থাকলে ম্যানোমিটারের দুই বাহুর তরলের উচ্চতার পার্থক্য মেগে আবদ্ধ বায়ুর চাপ নির্ণয় করা যায়।
বদ্ধ মুখ ম্যানোমিটারে চাপ P দুটি বাহুর মধ্যে পারদস্তম্ভের উচ্চতার পার্থক্যের ওপর নির্ভরশীল অর্থাৎ, P = h⋅d⋅g।
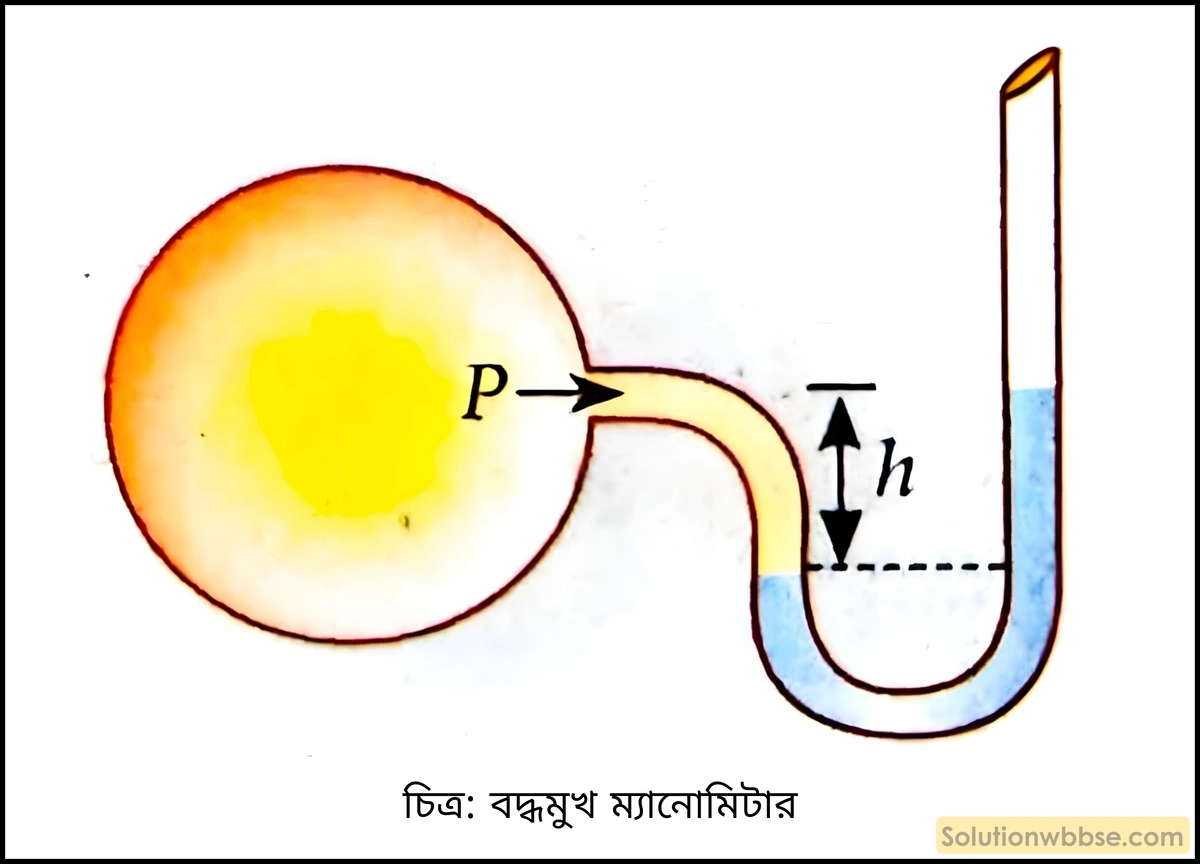
ব্যারোমিটারে পারদস্তম্ভের উচ্চতা 76 cm হলে গ্যাসের প্রমাণ চাপ
= 76 cm পারদস্তম্ভের চাপ
= পারদস্তম্ভের উচ্চতা × পারদের ঘনত্ব × অভিকর্ষজ ত্বরণ
= (76 × 13.6 × 980) ডাইন/বর্গসেমি
= 1.013 × 106 ডাইন/বর্গসেমি
আয়তন –
কোনো গ্যাসকে যখন কোনো বদ্ধ পাত্রে রাখা হয় তখন গ্যাসটি সেই পাত্রের আয়তন অধিকার করে। কোনো গ্যাসের আয়তন তার উপর প্রযুক্ত চাপ ও উষ্ণতার ওপর নির্ভরশীল।
- আয়তনের মাত্রা – L3
- আয়তনের একক – CGS = cm3 (ঘনসেমি), SI = m3 (ঘনমিটার)
- ব্যবহারিক একক – লিটার (L)
সম্পর্ক –
1 L = 1000 cm3 বা 1000 cc
1 cm3 = 1 mL (মিলিলিটার); 1 m3 = 106 cm3
বয়েলের সূত্র –
স্থির উষ্ণতায় কোনো নির্দিষ্ট ভরের গ্যাসের আয়তন ওই গ্যাসটির চাপের সঙ্গে ব্যস্তানুপাতে পরিবর্তিত হয়।
বয়েলের সূত্রের ধ্রুবক দুটি হল,
- গ্যাসের ভর ও
- গ্যাসের উষ্ণতা।
বয়েলের সূত্রের গাণিতিক রূপ হল, \(P\propto\frac1V\); যেখানে P হল চাপ এবং V হল আয়তন।
অর্থাৎ,
বা, PV = ধ্রুবক
সুতরাং, গ্যাসের চাপ ও আয়তন যথাক্রমে P1 ও V1 থেকে পরিবর্তিত হয়ে P2 ও V2 হলে এবং উষ্ণতা ও ভর স্থির থাকলে বয়েলের সূত্রানুযায়ী P1V1 = P2V2 = ধ্রুবক।
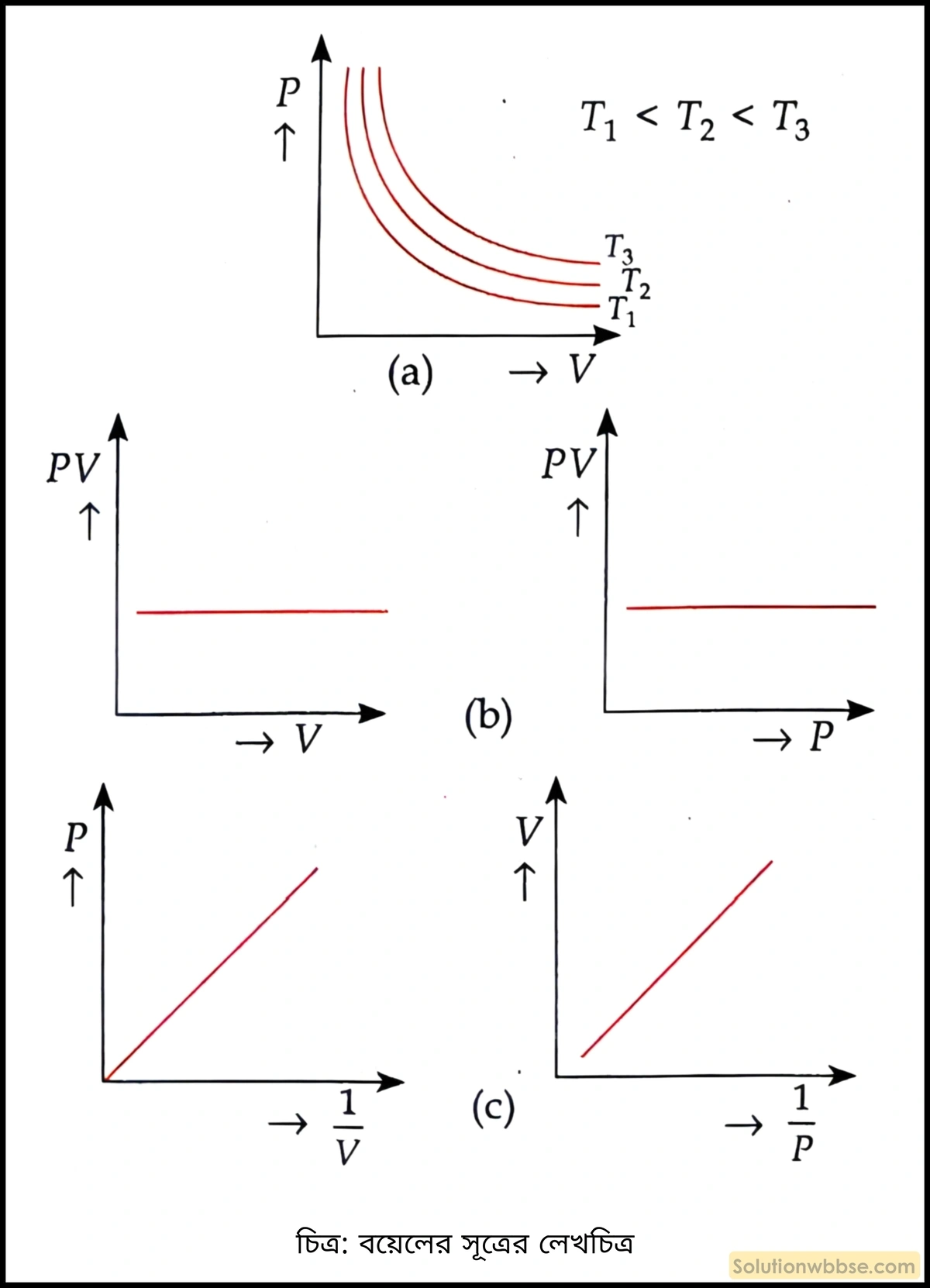
লেখচিত্র –
- P-V লেখচিত্রটি সমপরাবৃত্তাকার। এই লেখচিত্র অনুযায়ী চাপ শূন্য হলে আয়তন অসীম হয়ে যায় এবং আয়তন শূন্য করতে গেলে চাপ অসীমে নিয়ে যেতে হয়। এই লেখচিত্র ব্যবহার করে গ্যাসকে প্রসারণ বা সংকোচনে কৃতকার্য কত তা জানা যায়।
- বয়েলের সূত্রানুযায়ী চাপ ও আয়তনের গুণফল ধ্রুবক হয় অর্থাৎ P বা V পরিবর্তিত হলেও ওই গুণফল পরিবর্তিত হয় না তাই লেখচিত্র P বা V অক্ষের সমান্তরাল সরলরেখা হয়।
- বয়েলের সূত্রানুযায়ী \(P-\frac1V\) বা \(V-\frac1P\) লেখচিত্র মূলবিন্দুগামী সরলরেখা হবে।
সীমাবদ্ধতা –
- বয়েলের সূত্র শুধুমাত্র আদর্শ গ্যাসের ক্ষেত্রে প্রযোজ্য, বাস্তব গ্যাসগুলি নিম্ন চাপে ও উচ্চ উষ্ণতায় এই সূত্র মেনে চলে।
- তাপমাত্রা বা গ্যাসের ভর পালটে গেলে এই সূত্র প্রযোজ্য হয় না।
এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞানের একটি গুরুত্বপূর্ণ অংশ ‘বয়েলের সূত্র’ নিয়ে আলোচনা করেছি, যা ‘গ্যাসের আচরণ’ অধ্যায়ের অন্তর্ভুক্ত। মাধ্যমিক পরীক্ষায় এই অংশটি থেকে প্রায় প্রতি বছর প্রশ্ন আসে এবং চাকরির পরীক্ষার প্রস্তুতির জন্যও এটি অত্যন্ত গুরুত্বপূর্ণ। তাই শিক্ষার্থী ও প্রার্থী সকলের জন্য এই আলোচনা বিশেষভাবে সহায়ক হবে বলে আমরা আশা করি। আশা করি আর্টিকেলটি আপনাদের উপকারে এসেছে। কোনো প্রশ্ন বা অসুবিধা থাকলে, আমাদের টেলিগ্রামে যোগাযোগ করুন—আমরা উত্তর দেওয়ার চেষ্টা করব। পাশাপাশি, যাদের এই তথ্যগুলি প্রয়োজন মনে করছেন, তাদের সাথে এই পোস্টটি শেয়ার করুন। ধন্যবাদান্তে, Team SolutionWbbse






Leave a Comment