এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞান বিষয়ের একটি অত্যন্ত গুরুত্বপূর্ণ প্রশ্ন — “কোনো মৌলের একাধিক পরমাণু বা বিভিন্ন মৌলের পরমাণুগুলি নিজেদের মধ্যে যুক্ত হয়ে অণু গঠন করে কেন? অথবা, পরমাণুগুলির মধ্যে রাসায়নিক সংযুক্তির কারণ লেখো।” — নিয়ে আলোচনা করব। এই প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞানের অষ্টম অধ্যায় “পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ” -এর “আয়নীয় ও সমযোজী বন্ধন” অংশ থেকে নেওয়া হয়েছে। মাধ্যমিক পরীক্ষা এবং বিভিন্ন চাকরির পরীক্ষায় এই প্রশ্নটি প্রায়ই আসে, তাই এটি শিক্ষার্থীদের জন্য বিশেষভাবে গুরুত্বপূর্ণ।

কোনো মৌলের একাধিক পরমাণু বা বিভিন্ন মৌলের পরমাণুগুলি নিজেদের মধ্যে যুক্ত হয়ে অণু গঠন করে কেন?
অথবা, পরমাণুগুলির মধ্যে রাসায়নিক সংযুক্তির কারণ লেখো।
কোনো মৌলের একাধিক পরমাণু বা বিভিন্ন মৌলের পরমাণুগুলি নিজেদের মধ্যে যুক্ত হয়ে অণু গঠন করে কারণ –
- নিষ্ক্রিয় গ্যাসের গঠন কাঠামো লাভ করার জন্য – প্রকৃতিতে পরমাণুগুলির রাসায়নিক সংযুক্তির কারণ অন্তর্নিহিত রয়েছে তাদের ইলেকট্রনীয় গঠন কাঠামো বা বিন্যাসের উপর। হিলিয়াম (2) ছাড়া সমস্ত নিষ্ক্রিয় মৌলের যোজ্যতা কক্ষে 8টি ইলেকট্রন থাকে। এদের যোজ্যতা কক্ষগুলি সম্পূর্ণরূপে ইলেকট্রন দ্বারা পূর্ণ থাকায় নিষ্ক্রিয় মৌলগুলি সুস্থিত হয়। নিষ্ক্রিয় মৌলগুলি ছাড়া অন্যান্য সমস্ত মৌলের পরমাণুগুলির সবচেয়ে বাইরের কক্ষে আটটি ইলেকট্রন থাকে না। এই ধরনের পরমাণুগুলি 8টি (বা 2টি) ইলেকট্রন বিশিষ্ট নিষ্ক্রিয় মৌলের ইলেকট্রনীয় বিন্যাস লাভ করার প্রত্যাশায় রাসায়নিকভাবে সংযুক্ত হয়।
- ন্যূনতম শক্তি লাভ করার জন্য (Tendency to acquire mini-mum energy) – সমস্ত সিস্টেম তার নিজস্ব শক্তিকে কমানোর মাধ্যমে স্থায়িত্ব লাভের চেষ্টা করে। এই স্থায়িত্ব লাভ তখনই সম্ভব যখন অণু দুটির মধ্যে আকর্ষণ বল বৃদ্ধি পায়। আকর্ষণ বল বৃদ্ধি পেলে অণুগুলির শক্তিকে কমিয়ে দেয়। এই শক্তির পরিমাণ যত কমবে অণুটি তত বেশি স্থায়িত্ব লাভ করবে।
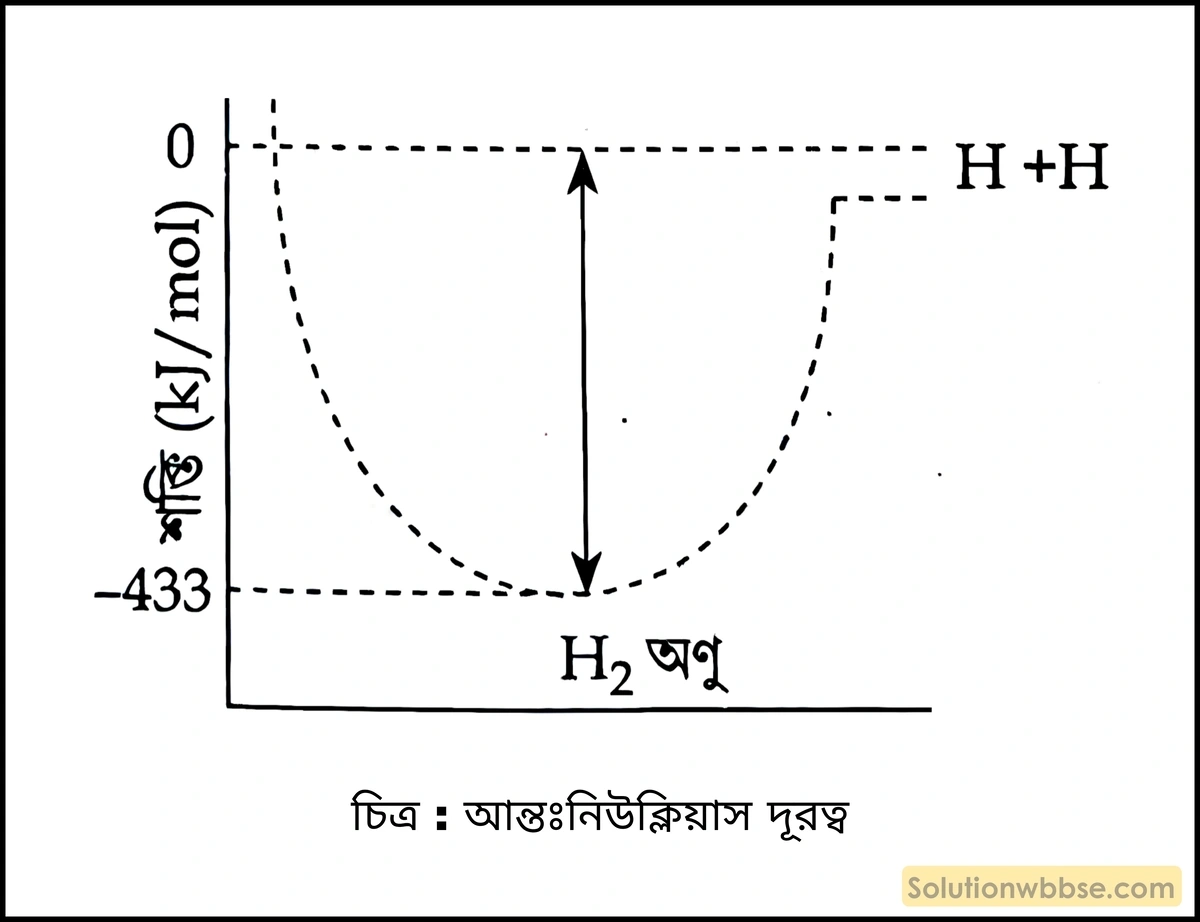
পরীক্ষায় দেখা গেছে যে হাইড্রোজেন পরমাণুগুলি দ্বারা 1 mole হাইড্রোজেন তৈরি করতে 433 kJ শক্তি বেরিয়ে যায়।
এই আর্টিকেলে আমরা মাধ্যমিক ভৌতবিজ্ঞান বিষয়ের একটি অত্যন্ত গুরুত্বপূর্ণ প্রশ্ন — “কোনো মৌলের একাধিক পরমাণু বা বিভিন্ন মৌলের পরমাণুগুলি নিজেদের মধ্যে যুক্ত হয়ে অণু গঠন করে কেন? অথবা, পরমাণুগুলির মধ্যে রাসায়নিক সংযুক্তির কারণ লেখো।” — নিয়ে আলোচনা করেছি। এই প্রশ্নটি মাধ্যমিক ভৌতবিজ্ঞানের অষ্টম অধ্যায় “পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ” -এর “আয়নীয় ও সমযোজী বন্ধন” অংশ থেকে নেওয়া হয়েছে। মাধ্যমিক পরীক্ষা এবং বিভিন্ন চাকরির পরীক্ষায় এই প্রশ্নটি প্রায়ই আসে, তাই এটি শিক্ষার্থীদের জন্য বিশেষভাবে গুরুত্বপূর্ণ। আশা করি এই আর্টিকেলটি আপনাদের জন্য উপকারী হয়েছে। আপনাদের কোনো প্রশ্ন বা অসুবিধা থাকলে, আমাদের সাথে টেলিগ্রামে যোগাযোগ করুন।






Leave a Comment