আজকের আর্টিকেলে আমরা নবম শ্রেণীর ভৌতবিজ্ঞান বইয়ের চতুর্থ অধ্যায় “পদার্থ : পরমাণুর গঠন ও পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ” এর “জল” থেকে সহজ ও সংক্ষিপ্ত প্রশ্ন-উত্তর শেয়ার করবো। এই প্রশ্নগুলো নবম শ্রেণির ইউনিট টেস্ট থেকে বার্ষিক পরীক্ষা এর জন্য যেমন গুরুত্বপূর্ণ, তেমনি চাকরি বা বিভিন্ন প্রতিযোগিতার পরীক্ষাতেও কাজে লাগবে। এই অধ্যায় থেকে স্কুল পরীক্ষা থেকে শুরু করে চাকরির পরীক্ষায় প্রায়ই প্রশ্ন আসে, তাই এই প্রশ্নোত্তরগুলো সবাইকে সাহায্য করবে। প্রতিটি প্রশ্নের উত্তর সহজ ভাষায় লেখা হয়েছে, যাতে সবাই বুঝতে পারেন। পড়ার শেষে এই অধ্যায়ের মুখ্য বিষয়গুলো আপনার আয়ত্তে চলে আসবে এবং যেকোনো পরীক্ষায় আত্মবিশ্বাসের সঙ্গে লিখতে পারবেন।

জ্ঞানমূলক প্রশ্নোত্তর
জলের আপেক্ষিক তাপ ও উচ্চ স্ফুটনাঙ্ক এই ভৌতধর্ম দুটি প্রাণীদের জীবনধারণে কী ভূমিকা পালন করে?
জলের আপেক্ষিক তাপ (Specific heat of water) – কোনো পদার্থের একক ভরের উষ্ণতা একক পরিমাণ বৃদ্ধি করতে যে তাপের প্রয়োজন হয়, সেই তাপকে ওই পদার্থের আপেক্ষিক তাপ বলে। জলের আপেক্ষিক তাপ সব থেকে বেশি (1 Cal g-1°C-1 অথবা, 4200 J kg-1°C-1)। তাই একই উষ্ণতা বৃদ্ধিতে অন্যান্য তরল অপেক্ষা জলের বেশি তাপের প্রয়োজন হয়। ফলে, পরিবেশের উষ্ণতা বৃদ্ধি পেলেও উন্নত দেহবিশিষ্ট প্রাণীদের দেহের তাপমাত্রা নির্দিষ্ট থাকে। বেশি আপেক্ষিক তাপের জন্য জল স্থল অপেক্ষা ধীরে ধীরে উত্তপ্ত হয়, আবার কোনো নির্দিষ্ট উষ্ণতায় অন্য যে-কোনো তরলের থেকে জল বেশি তাপ ধরে রাখতে পারে। ফলে, সমুদ্রের উপকূলবর্তী অঞ্চলের আবহাওয়া গ্রীষ্ম ও শীত উভয় ঋতুতেই অনেক বেশি আরামপ্রদ। জলের এই ধর্মের জন্যেই সেঁক দেওয়ার জন্য গরম জল ব্যবহার করা হয় এবং কলকারখানার যন্ত্রপাতিকে ঠান্ডা করার জন্য ও মোটরগাড়ির রেডিয়েটরে কুল্যান্ট হিসেবেও জল ব্যবহার করা হয়।
উচ্চ স্ফুটনাঙ্ক – স্বাভাবিক বায়ুচাপে জল 100°C উষ্ণতায় ফুটে বাষ্পে পরিণত হয়। অর্থাৎ, 0°C উষ্ণতা থেকে 100°C উষ্ণতার মধ্যে জল তরল অবস্থায় থাকে। তরল অবস্থায় উষ্ণতার এত বড়ো বিস্তৃতি আর অন্য কোনো দ্রাবকের নেই।
এই বিস্তৃত উষ্ণতা পাল্লার মধ্যে জলকে মাধ্যম হিসেবে ব্যবহার করে বিভিন্ন ভৌত ও রাসায়নিক প্রক্রিয়া ঘটানো হয়। এছাড়া জলের স্ফুটনাঙ্ক বেশি হওয়ায় জলের বাষ্পীভবনের জন্য প্রয়োজনীয় তাপ বেশি লাগে। তাই ঘর্ম নিঃসরণের মাধ্যমে প্রাণীদেহ থেকে জল বেরিয়ে গেলেও তুলনামূলকভাবে বেশি পরিমাণ তাপ দেহ থেকে বেরিয়ে যাওয়ায় প্রাণীদেহ শীতল থাকে এবং সর্বদা দেহের স্বাভাবিক তাপমাত্রা বজায় থাকে। আবার জলের উচ্চ স্ফুটনাঙ্কের জন্য উচ্চ তাপমাত্রায় সুসিদ্ধ জীবাণুমুক্ত খাদ্যবস্তু তৈরি করা সম্ভব হয়।
জলের বর্ণহীন ধর্মটি উদ্ভিদের প্রাণের বিকাশে কীভাবে সাহায্য করে?
বিশুদ্ধ জলের কোনো বর্ণ নেই, তাই এটি স্বচ্ছ ও বর্ণহীন। জলে মূলত বিভিন্ন ক্ষুদ্রাতিক্ষুদ্র, অবাঞ্ছিত জীবগোষ্ঠীর মাত্রাতিরিক্ত উপস্থিতি এবং বিভিন্ন জৈব ও অজৈব দূষকের উপস্থিতির জন্য জলের বর্ণ সৃষ্টি (সবুজ, হালকা নীল ইত্যাদি) হয়।
বর্ণহীন জল উদ্ভিদের প্রাণের বিকাশে নিম্নলিখিত ভূমিকা পালন করে থাকে –
- জল বর্ণহীন ও স্বচ্ছ হওয়ায় গভীর জলাশয়ের নীচে সূর্যের আলো সহজেই পৌঁছোতে পারে, আলোর কোনো অংশ শোষিত হয় না। ফলে, জলাশয়ের গভীরে থাকা জলজ উদ্ভিদ সালোকসংশ্লেষ সম্পন্ন করতে পারে। সালোকসংশ্লেষের ফলে উৎপন্ন অক্সিজেন জলে দ্রবীভূত অক্সিজেনের সঠিক মাত্রা বজায় রাখে এবং জলাশয়ের বাস্তুতন্ত্র রক্ষিত হয়।
- বর্ণহীন জলে বিভিন্ন দূষকের পরিমাণ কম থাকে, বিভিন্ন খনিজের যথাযথ পরিমাণ বজায় থাকায় উদ্ভিদের বৃদ্ধি ও জীবনধারণের সহায়ক হয়।
- বর্ণহীন, স্বচ্ছ জল উদ্ভিদদেহে দ্রুত শোষিত হয়। ফলে, উদ্ভিদদেহে জলের চাহিদা দ্রুত মেটে।
জলের কৈশিক ক্রিয়া বলতে কী বোঝায়? এর গুরুত্ব আলোচনা করো।
জলের কৈশিক ক্রিয়া – কাচের কৈশিক নলকে জলের মধ্যে সোজাভাবে আংশিক নিমজ্জিত করলে দেখা যায় যে, কৈশিক নলের ভিতরকার জলতল বাইরের জলতল অপেক্ষা কিছুটা উপরে অবস্থান করছে এবং নলের ভিতরে জলের পৃষ্ঠতল অনুভূমিক না হয়ে অবতল হয়। অর্থাৎ, ওই কৈশিক নলের মধ্যে দিয়ে জল অভিকর্ষের বিপরীতে উপরে উঠতে থাকে। কৈশিক নলে জলের এরূপ ঊর্ধ্বারোহণের ঘটনাকে কৈশিক ক্রিয়া বলে।

কৈশিক ক্রিয়ার গুরুত্ব –
- কৈশিক ক্রিয়ার জন্য মূলরোম দ্বারা শোষিত জল ও জলে দ্রবীভূত খনিজ পদার্থ উদ্ভিদদেহে জাইলেম বাহিকার মধ্যে দিয়ে বাহিত হয়ে উপরে উঠে শেষ পর্যন্ত পাতায় পৌঁছোয়।
- ক্ষুদ্র ব্যাকটেরিয়া থেকে শুরু করে উন্নত শ্রেণির জীবদেহে কৈশিক ক্রিয়ার ফলে জলসহ অন্যান্য জলীয় রস কোশ থেকে কোশান্তরে প্রবাহিত হয়।
- জলের কৈশিক ক্রিয়ার কারণে চাষের জমির নীচের স্তরে থাকা জল মাটির উপরের স্তরের মাটিকে ভিজিয়ে চারাগাছে জলের জোগান দেয়। এর ফলে আপাত শুকনো মাটিতে উদ্ভিদের বিকাশ সম্ভব হয়।
জলের দ্রাবক ধর্মের গুরুত্ব আলোচনা করো।
দ্রাবক ধর্ম – জল একটি উত্তম ধ্রুবীয় (polar) দ্রাবক। কিছু কিছু সমযোজী যৌগ জলে হাইড্রোজেন বন্ধন গঠনের মাধ্যমে দ্রবীভূত হয়। যেমন – চিনি, অ্যালকোহল, গ্লুকোজ প্রভৃতি। HCl, NH3 -এর মতো সমযোজী যৌগের সঙ্গে জল বিক্রিয়া করে দ্রাবিত করে।
\(HCl+H_2O=H_3O^++Cl^-\)
\(NH_3+H_2O=NH_4^++OH^-\)
জলের ধ্রুবীয়তার জন্য অধিকাংশ তড়িৎযোজী যৌগ, যেমন – NaCl, KCl, KNO3, CaCl2 প্রভৃতি জলে দ্রবীভূত হয়। জলের NaCl অণুর ঋণাত্মক বা নেগেটিভ প্রান্ত তড়িৎযোজী যৌগের ধনাত্মক আয়নকে এবং জলের অণুর ধনাত্মক প্রান্ত ওই যৌগের ঋণাত্মক আয়নকে আকর্ষণ করে। ফলে, আয়নগুলি তার বিপরীত আয়ন থেকে বিচ্ছিন্ন হয়ে দ্রবীভূত হয়ে যায়।
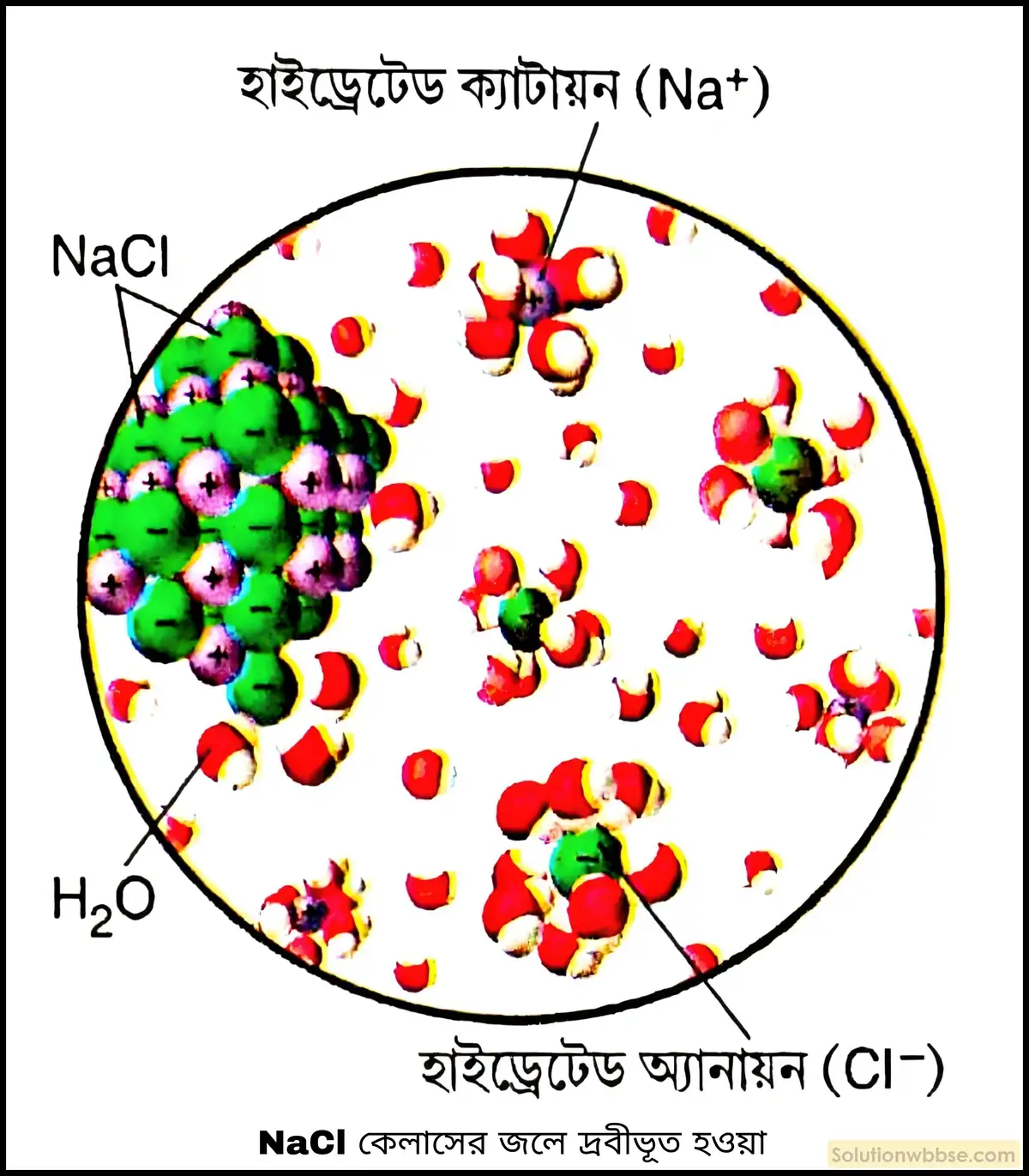
আবার জলের দ্রাবক ধর্মের জন্যই, জীবদেহের প্রতিটি কোশে প্রয়োজনীয় পদার্থের প্রবেশ, জলীয় মাধ্যমে বিপাক ক্রিয়া এবং উৎপন্ন রেচন পদার্থ দেহের বাইরে আনা সম্ভবপর হয়।
জলজ প্রাণীদের ওপর জলের ব্যতিক্রান্ত প্রসারণের প্রভাব আলোচনা করো।
জলের ব্যতিক্রান্ত প্রসারণ (Anomalous expansion of water) – 0°C থেকে উষ্ণতা বৃদ্ধিতে বরফ গলতে থাকে এবং বরফের কেলাস গঠন ভাঙতে শুরু করে। এর ফলে জলের অণুগুলি কাছাকাছি আসতে শুরু করে এবং ঘনত্ব বৃদ্ধি পায়। 4°C উষ্ণতায় জলের অণুগুলি আন্তঃআণবিক বন্ধনী গঠনের মাধ্যমে সবচেয়ে ঘনসন্নিবিষ্ট অবস্থায় থাকে এবং এই উষ্ণতায় জলের ঘনত্ব সর্বাধিক হয়। 4°C -এর ঊর্ধ্বে জলের অণুগুলির তাপীয় গতির ফলে আয়তন বৃদ্ধি পায় এবং ঘনত্ব কমতে থাকে।

শীতের দেশে খুব ঠান্ডার দিনে জলাশয়ের জলের উপরিভাগ ঠান্ডা হাওয়ার সংস্পর্শে এসে ক্রমশ শীতল হয়ে ভারী হয় এবং নীচের দিকে যায়। নীচের দিকের অপেক্ষাকৃত গরম জল উপরে উঠে এসে ঠান্ডা হয়। যখন জলের উষ্ণতা 4°C -এ পৌঁছোয় তখন জল সবচেয়ে ভারী হয় এবং জলাশয়ের নীচে অবস্থান করে। উপরের জল ক্রমশ ঠান্ডা হয়ে বরফে পরিণত হয়, কিন্তু নীচের দিকের জল 4°C উষ্ণতাতেই থাকে। বরফ জল অপেক্ষা হালকা হওয়ায় ওপরে ভাসতে থাকে এবং বরফ তাপের কপরিবাহী বলে নীচের জল থেকে উপরের ঠান্ডা বায়ুতে বেশি তাপ পরিবাহিত হয় না। এই জন্য প্রচণ্ড শীতের দিনে যখন পুকুর বা সমুদ্রের উপরিভাগ বরফে পরিণত হয় তখন নীচের জল 4°C তাপমাত্রায় থাকে বলে মাছ ও জলচর প্রাণীরা বেঁচে থাকতে পারে।
শীতের দেশে পাইপের মধ্যে জল প্রবাহিত হওয়ার সময় কেন তা জমে বরফে পরিণত হয়ে পাইপ ফাটিয়ে দিতে পারে?
শীতের দেশে পাইপের মধ্যে জল প্রবাহিত হওয়ার সময় অনেক ক্ষেত্রে তা জমে কঠিন বরফে পরিণত হয়। ফলে, আয়তনে বেড়ে যায়। আয়তন বাড়ার ফলে পাইপে প্রচণ্ড চাপ পড়ে এবং এতে জলের পাইপ ফেটে যায়।
Potable Water কাকে বলে?
মানুষের পানের উপযোগী জলকে Potable Water বা পানযোগ্য জল বলে।
পানীয় জলের আবশ্যকীয় কয়েকটি ধর্মের উল্লেখ করো।
অথবা, পানীয় জলের গুণাগুণগুলি উল্লেখ করো।
পানীয় জলের নিম্নোক্ত বৈশিষ্ট্যগুলি থাকা উচিত –
- এটি বর্ণহীন ও গন্ধহীন হওয়া উচিত।
- এটিকে পরিষ্কার ও স্বচ্ছ হতে হবে।
- পানীয় জলে কোনোরূপ রোগ সৃষ্টিকারী জীবাণু থাকা চলবে না।
- এতে কোনোরকম প্রলম্বিত বা দ্রবীভূত অশুদ্ধি থাকা অনুচিত।
- আমাদের শরীরের পক্ষে উপকারী কিছু খনিজ (সোডিয়াম, ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রন ইত্যাদি) উপযুক্ত মাত্রায় দ্রবীভূত থাকতে হবে।
- পানীয় জলকে স্বাদু করার উদ্দেশ্যে এতে কিছু গ্যাসও দ্রবীভূত থাকতে হবে।
- বিষক্রিয়া সৃষ্টিকারী নাইট্রেট, সায়ানাইড, ইউরিয়ার মতো কোনো ক্ষতিকর লবণ দ্রবীভূত থাকলে চলবে না। পানীয় জলের মধ্যে লেড, মারকারি, কপার প্রভৃতি ক্ষতিকারক ধাতব পদার্থ দ্রবীভূত থাকা উচিত নয়।
- পানীয় জলের কলিফর্ম কাউন্ট শূন্য হওয়া উচিত। অর্থাৎ, বিশুদ্ধ পানীয় জল ব্যাকটেরিয়া মুক্ত হতে হবে।
- পানীয় জলে ফ্লুওরাইডের মাত্রা 1 ppm বা 1 mg dm-3 হওয়া বাঞ্ছনীয়। এটি আমাদের দাঁতের ক্ষয় প্রতিরোধ করার জন্য প্রয়োজনীয়। কিন্তু জলে ফুওরাইডের মাত্রা 1.5 ppm বা তার বেশি হলে ফুওরাইড দাঁত ও হাড়ের Ca2+ আয়নের ক্ষতি করে। ফলে, ডেন্টালফ্লুওরোসিস, অস্টিওফ্লুওরোসিস প্রভৃতি রোগ দেখা দেয়।
- জলে দ্রবীভূত অক্সিজেনের পরিমাণ 6 ppm বা এর অধিক হওয়া উচিত।
- পানীয় জলের pH -এর সঠিক মাত্রা 6 – 8.5 হওয়া উচিত।
- পানীয় জলে আর্সেনিকের মাত্রা শূন্য হওয়া উচিত। যদি কিছু পরিমাণে আর্সেনিক উপস্থিত থাকে তবে এর মাত্রা যেন 0.05 ppm -এর বেশি না হয়।
কলিফর্ম কাউন্ট কী? এর গুরুত্ব লেখো।
কলিফর্ম কাউন্ট – কোনো নমুনা জলের প্রতি 100 mL আয়তনে যত সংখ্যক কলিফর্ম ব্যাকটেরিয়ার (এসচেরিশিয়া কোলাই) কলোনি উপস্থিত থাকে, সেই কলোনি সংখ্যাকে ওই নমুনা জলের কলিফর্ম কাউন্ট বা কলিফর্ম সূচক বলে। এই সংখ্যার মান যত বেশি হয় ততই জলে ক্ষতিকর জীবাণু বা ব্যাকটেরিয়া থাকার সম্ভাবনা বৃদ্ধি পায়, অর্থাৎ, সেই জল পানের অনুপযোগী। পানীয় জলের কলিফর্ম সংখ্যার মান শূন্য (0) হওয়া বাঞ্ছনীয়।
কলিফর্ম কাউন্টের গুরুত্ব – বিভিন্ন ধরনের ক্ষতিকারক ব্যাকটেরিয়া (যেমন – E.Coli, ভিব্রিও কলেরি প্রভৃতি), ভাইরাস ও পরজীবী প্রোটোজোয়া পানীয় জলে উপস্থিত থাকলে তা আমাদের স্বাস্থ্যের পক্ষে বিপজ্জনক। এই সমস্ত জীবাণু বিভিন্ন জৈব বর্জ্যপদার্থ ও মানুষের মল দ্বারা নির্গত হয়ে বৃষ্টির জলে ধুয়ে নদী বা পুকুরের জলে মেশে। জলে থাকা এই সমস্ত রোগ সৃষ্টিকারী ব্যাকটেরিয়া ও জীবাণুর উপস্থিতি কলিফর্ম কাউন্ট থেকে জানা যায়। এটি বেশি হলে জলে ব্যাকটেরিয়ার সংখ্যা বেশি হয়। অর্থাৎ, সেটি দূষিত জল। প্রকৃতপক্ষে, কলিফর্ম কাউন্ট হল পানীয় জলের বিশুদ্ধতার অন্যতম সূচক। পানীয় জলের স্বাস্থ্যসম্মত মান কেমন তার নির্দেশকই হল ওই পানীয় জলের কলিফর্ম কাউন্ট। এসচেরিশিয়া কোলাই (Escherichia Coli) হল অন্যতম উল্লেখযোগ্য কলিফর্ম ব্যাকটেরিয়া।
জলের মধ্যে মূলত কোন তিনটি বিশেষ ব্যাকটেরিয়ার সংখ্যা নির্ণয়ের জন্য কলিফর্ম কাউন্ট ব্যবহার করা হয়?
কলিফর্ম কাউন্টের সাহায্যে জলের মধ্যে মূলত তিনটি বিশেষ ব্যাকটেরিয়ার (E.Coli, Klebsiella pneumoniae, Enterobacter aerogenes) সংখ্যা নির্ণয় করা হয়।
কলিফর্ম ব্যাকটেরিয়া কী এবং এটি কোন পরিবেশে সাধারণত বিদ্যমান থাকে?
কলিফর্ম ব্যাকটেরিয়ারা প্রকৃতপক্ষে গ্রাম নেগেটিভ ব্যাকটেরিয়া যা 35°C – 37°C উষ্ণতায় ল্যাকটোজকে সন্ধান প্রক্রিয়ায় জারিত করে গ্যাস ও অ্যাসিড উৎপন্ন করে। এই ব্যাকটেরিয়া জল ও মাটিতে অবস্থান করে। উষ্ণ রক্ত বিশিষ্ট প্রাণীদের অস্ত্রে এই ব্যাকটেরিয়া দেখা যায়।
পানীয় জলের pH মাত্রা কীরূপ হওয়া প্রয়োজন?
বিশুদ্ধ ও প্রশমিত জলের pH = 7 হলেও পানীয় জলে নানা প্রয়োজনীয় খনিজ পদার্থ মিশে থাকায় পানীয় জলের pH -এর মান পরিবর্তিত হয়। পানীয় জলের অনুমোদিত pH মাত্রার পাল্লা 6 – 8.5 পর্যন্ত হওয়া উচিত।
পানীয় জলে pH মাত্রা সঠিক না থাকলে আমাদের দেহ তরলের অ্যাসিড ও ক্ষারের ভারসাম্য বিঘ্নিত হবে। পানীয় জলের pH -এর মান অনুমোদিত মাত্রার ঊর্ধ্বসীমার চেয়ে বেশি হলে তা চোখ, ত্বক, চুলের ক্ষতি করে, হজমশক্তি কমিয়ে দেয়। আবার pH -এর মান অনুমোদিত মাত্রার নিম্নসীমার চেয়ে কম হলে ওই জল চোখের সংস্পর্শে এলে চোখ লাল হয়ে যায়, চামড়ায় ক্ষত সৃষ্টি হয়।
দ্রবীভূত অক্সিজেন (DO) বলতে কী বোঝায়?
দ্রবীভূত অক্সিজেন (Dissolved oxygen) – মানুষের ব্যবহৃত পানীয় জলে, জলাশয়ে যে অক্সিজেন গ্যাস দ্রবীভূত অবস্থায় থাকে, তাকে দ্রবীভূত অক্সিজেন বলে। একে সংক্ষেপে DO দ্বারা প্রকাশ করা হয়। কোনোভাবে জলদূষণের ফলে যদি জলে শৈবাল বা আগাছা বৃদ্ধি পায় তবে জলে DO -এর পরিমাণ কমে যায়। তাই দ্রবীভূত অক্সিজেনের মান দ্বারা জলের গুণাগুণ বিচার করা যায়।
জলজ উদ্ভিদ ও প্রাণীর স্বাভাবিক জীবনযাপনের জন্য DO -এর স্বাভাবিক মাত্রা 4 – 6 mg/L। DO -এর মান যত বেশি হয় জল তত ভালো বা বিশুদ্ধ হয়। DO -এর মান কম হলে জল দূষিত হয়। তাপমাত্রা বৃদ্ধিতে জলে দ্রবীভূত অক্সিজেনের পরিমাণ হ্রাস পায় এবং তাপমাত্রা হ্রাস পেলে জলে দ্রবীভূত অক্সিজেনের পরিমাণ বৃদ্ধি পায়।
উদাহরণ স্বরূপ বলা যায় যে, বাড়িতে রাখা জলের উষ্ণতা নদীর জলের থেকে বেশি হওয়ায়, দ্রবীভূত অক্সিজেনের পরিমাণ কম হয়। এই কারণে নদী থেকে ধরে আনা মাছ বাড়িতে জলের পাত্রে রাখলে তা মরে যায়। দেখা গেছে যে, প্রতি 1g জলে দ্রবীভূত অক্সিজেনের পরিমাণ 0.0004 g -এর কম হলে মাছ বাঁচতে পারে না।
জলে অক্সিজেন/অন্যান্য গ্যাস দ্রবীভূত থাকার সুবিধা লেখো।
জলে অক্সিজেন/অন্যান্য গ্যাস দ্রবীভূত থাকার সুবিধা –
- জলজ উদ্ভিদ ও প্রাণীর বেঁচে থাকার জন্য জলে অক্সিজেন দ্রবীভূত থাকা একান্ত দরকার।
- জলজ উদ্ভিদের সালোকসংশ্লেষ প্রক্রিয়া দ্বারা খাদ্য তৈরির জন্য জলে কার্বন ডাইঅক্সাইড দ্রবীভূত থাকা দরকার।
- দ্রবীভূত অক্সিজেন জলে উপস্থিত ব্যাকটেরিয়া, জীবাণুকে ধ্বংস করে জলকে জীবাণু মুক্ত রাখে।
- জলজ শামুক, ঝিনুকের দেহের খোলস গঠনে জলে দ্রবীভূত কার্বন ডাইঅক্সাইড ব্যবহৃত হয়।
BOD কাকে বলে?
BOD – কোনো দূষিত জলের প্রতি লিটারে উপস্থিত জৈব দূষকের বিয়োজনের জন্য যত মিলিগ্রাম O2 প্রয়োজন হয়, সেই সংখ্যাকে জৈব-রাসায়নিক অক্সিজেন চাহিদা বা Biochemical Oxygen Demand (BOD) বলা হয়।
COD কাকে বলে?
COD – কোনো দূষিত জলে উপস্থিত বিয়োজনযোগ্য ও বিয়োজন অযোগ্য দূষকের জারণের জন্য যে পরিমাণ অক্সিজেন প্রয়োজন হয়, তাকে রাসায়নিক অক্সিজেন চাহিদা বা Chemical Oxygen Demand (COD) বলে।
পানীয় জলে ক্লোরাইড, ফ্লুওরাইড ও আর্সেনিক যৌগের উপস্থিতির প্রভাব আলোচনা করো।
পানীয় জলে ক্লোরাইড ‘ক্লোরিনেটেড’ যৌগ হিসেবে উপস্থিত থাকে। ফ্লুওরাইড বিভিন্ন ধাতু ও অধাতুর (N2 ও O2 বাদে) সঙ্গে যুক্ত হয়ে ফ্লুওরাইড যৌগ গঠন করে থাকে। পানীয় জলে মাত্রাধিক ফ্লুওরাইড থাকলে অস্টিওফ্লুওরোসিস, ডেন্টাল ফ্লুওরোসিস প্রভৃতি রোগ হয়। আর্সেনিক পানীয় জলে দ্রাব্য আর্সেনেট এবং আর্সেনাইট যৌগরূপে থাকে। পানীয় জলে এর মাত্রা 0.01 mg/L -এর বেশি থাকা বিপজ্জনক। এর থেকে বেশি মাত্রায় আর্সেনিক যৌগ ক্যানসার, চর্মরোগ, দেহের সংবহনতন্ত্রের বিভিন্ন রোগ সৃষ্টি করে।
পানীয় জল প্রস্তুতিতে জল পরিশোধনের বিভিন্ন ধাপগুলি আলোচনা করো।
পানীয় জল প্রস্তুতিতে জল পরিশোধনের বিভিন্ন ধাপ –
জলকে পানের উপযোগী হতে হলে তা –
- জলে ভাসমান অবাঞ্ছিত অপদ্রব্য ও
- ক্ষতিকারক ব্যাকটেরিয়া ও জীবাণুমুক্ত হতে হবে
জলে ভাসমান অবাঞ্ছিত অপদ্রব্য দূরীকরণ –
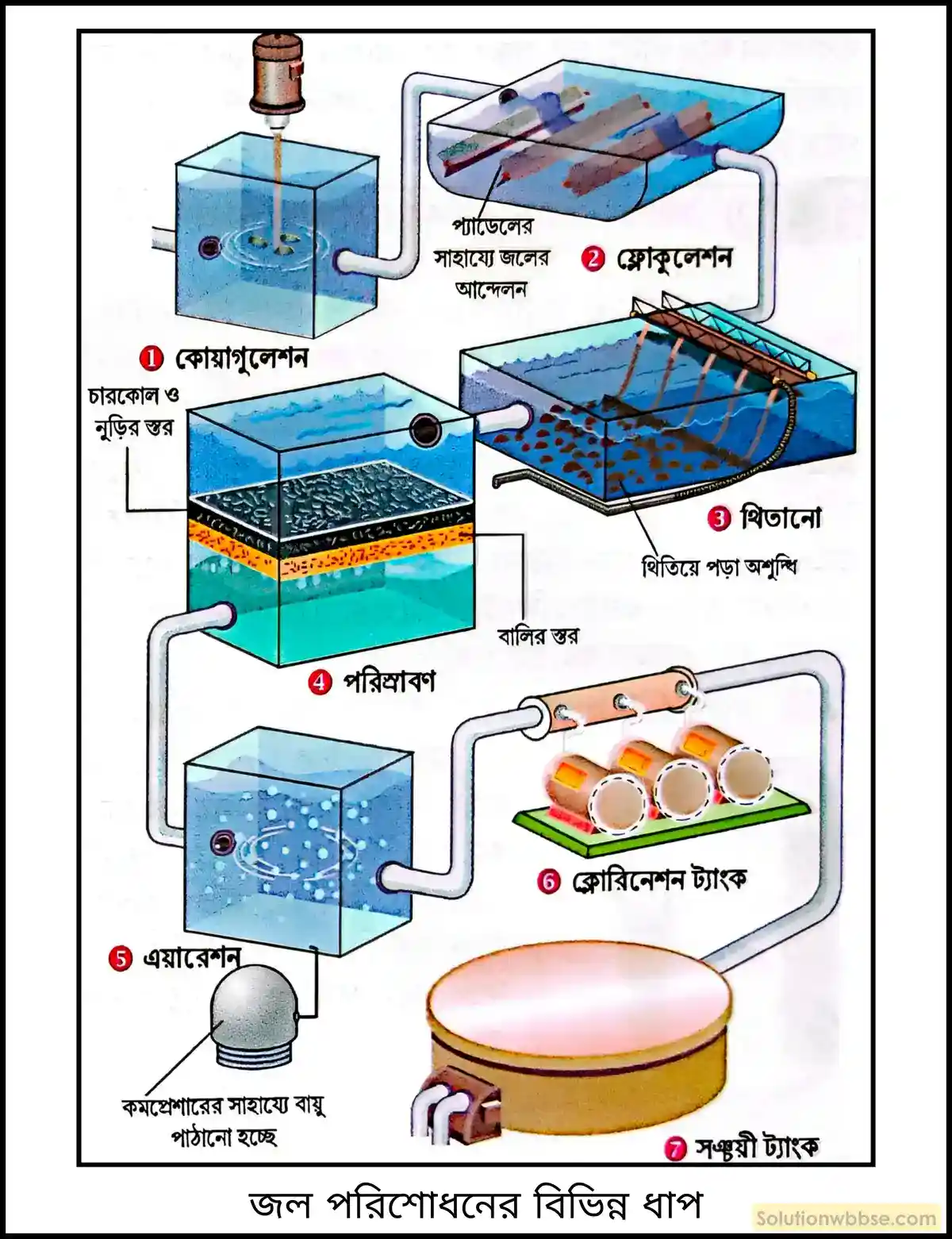
কোয়াগুলেশন ও ফ্লোকুলেশন (Coagulation & Flocculation) – জলের মধ্যে থাকা প্রলম্বিত কঠিন পদার্থকে পৃথক করতে কোয়াগুলেশন এবং ফ্লোকুলেশন পদ্ধতি অবলম্বন করা হয়। প্রথমে ট্যাংকের মধ্যে ফটকিরি [K2SO4⋅Al2(SO4)3⋅24H2O] যোগ করা হয়। ফটকিরিতে উপস্থিত Al3+ আয়ন ও K+ আয়ন দ্বারা জলের অপদ্রব্যের বিপরীত আধান প্রশমিত হয়, অর্থাৎ, আধানহীন হয়। এই K+ এবং Al3+ আয়ন জলে উপস্থিত কাদা, মাটি প্রভৃতিকে তঞ্চিত করে।
এরপর ট্যাংকের মধ্যে প্যাডেলের সাহায্যে ধীরে ধীরে জল প্রবাহিত করে প্রলম্বিত পদার্থের কণাগুলিকে আন্দোলিত করলে সেগুলি জোটবদ্ধ হয়ে আরও বড়ো আকার ধারণ করে, যাদেরকে ফ্লকস্ বলে। এইগুলি জল থেকে পৃথক হয়ে পড়ে এবং জল বিশুদ্ধ হয়।
থিতানো (Sedimentation) – একটি বড়ো ট্যাংকে এই অবিশুদ্ধ জলকে কিছুক্ষণ স্থিরভাবে রাখলে ভাসমান অশুদ্ধিগুলি নীচে থিতিয়ে পড়ে। এই থিতিয়ে পড়ার হার বৃদ্ধি করার জন্য জলে সামান্য পরিমাণ অ্যালাম [K2SO4⋅Al2(SO4)3⋅24H2O] যোগ করা হয়।
পরিস্রাবণ (Filtration) – এবার বড়ো ট্যাংকের জলকে বালি, সক্রিয় চারকোল এবং নুড়িপাথরের স্তরের মধ্যে দিয়ে ধীরে ধীরে চালনা করা হয়। এই পদ্ধতিতে ভাসমান অশুদ্ধিগুলি সম্পূর্ণ দূরীভূত হয়। সক্রিয় চারকোল অশুদ্ধিগুলিকে দৃঢ়ভাবে ধরে রেখে জল বিশুদ্ধিকরণে সাহায্য করে।
ক্ষতিকারক ব্যাকটেরিয়া ও জীবাণু দূরীকরণ –
ভূগর্ভস্থ স্তর থেকে যে জলের উত্তোলন করা হয় বা পৌর অঞ্চলে পাইপ লাইনের মাধ্যমে যে জল সরবরাহ করা হয়, তাতে রোগ সৃষ্টিকারী বিভিন্ন রকমের জীবাণু (প্যাথোজেনিক জীবাণু) উপস্থিত থাকে। তাই নিম্নলিখিত পদ্ধতি দ্বারা জল জীবাণুমুক্ত করে পান করা উচিত।
এয়ারেশন (Aeration) – পরিস্রুত জলযুক্ত ট্যাংকের নীচে দিয়ে বাতাস চালনা করলে, বাতাস মধ্যস্থ অক্সিজেন জৈব পদার্থগুলিকে জারিত করে এবং ক্ষতিকারক জীবাণুকে ধ্বংস করে। জলের মধ্যে দিয়ে বায়ুপ্রবাহ চালনা করলে জল দুর্গন্ধমুক্ত হয়।
ক্লোরিনেশন (Chlorination) – এরপর এই জলকে জীবাণু মুক্ত করতে জলের মধ্যে খুব অল্প পরিমাণে ক্লোরিন যোগ করা হয়। ক্লোরিন জলের সঙ্গে বিক্রিয়া করে জায়মান অক্সিজেন [O] উৎপন্ন করে, যা জলে উপস্থিত ক্ষতিকর জীবাণু, ব্যাকটেরিয়া প্রভৃতিকে ধ্বংস করে।
Cl2 + H2O → [HCl + HOCl] → 2HCl + [O]
জলের মধ্যে ব্লিচিং পাউডার বা জিওলিন বা হ্যালোজেন ট্যাবলেট মেশালেও জল জীবাণু মুক্ত হয়। জিওলিন বা হ্যালোজেন ট্যাবলেটের মূল উপাদান হল সোডিয়াম হাইপোক্লোরাইট যা বিয়োজিত হয়ে ক্লোরিন গ্যাস উৎপন্ন করে, আবার ব্লিচিং পাউডার [Ca(OCl)Cl] থেকে ক্লোরিন গ্যাস নির্গত হয়। এই ক্লোরিন জলকে জীবাণুমুক্ত করে। জলকে কিছুক্ষণ খোলা অবস্থায় রেখে দিলে অতিরিক্ত ক্লোরিন দূরীভূত হয় এবং জল পানের উপযোগী হয়।
তবে জলে বেশি পরিমাণে ক্লোরিন যোগ করলে জলে ক্লোরিনের গন্ধ পাওয়া যায়। অনেক সময় পটাশিয়াম পারম্যাঙ্গানেট, ক্লোরিন এবং অ্যামোনিয়ার মিশ্রণের সাহায্যেও জলকে জীবাণুমুক্ত করা হয়।
অতিবেগুনি রশ্মির (Ultra Violet Ray/UV Ray) সাহায্যে – জল পরিশোধন এবং অসংক্রমণের জন্য অতিবেগুনি রশ্মি ব্যবহার করা হয়। অতিবেগুনি রশ্মির প্রভাবে জলে উপস্থিত রোগজীবাণু মারা যায়। এই UV রশ্মির শোষণে জলে উপস্থিত কিছু জৈব অণু থেকে মুক্ত মূলক (Free Radical) উৎপন্ন হয়। এই মুক্ত মূলক জলে দ্রবীভূত জৈব বস্তুকে জারিত করে। ফলে, জলে জৈব বস্তুর সংক্রমণ হতে পারে না। এই পদ্ধতিতে কোনো রাসায়নিক পদার্থ ব্যবহার করতে হয় না। জীবাণু দুরীকরণে এই পদ্ধতি অনেক বেশি কার্যকর।
ওজোনাইজেশন – আধুনিক পদ্ধতিতে অনেকসময় জলের মধ্যে দিয়ে ওজোন গ্যাস চালনা করে জলকে নির্বীজিত (Sterilised) করা হয়।
Solar Water Disinfection (SODIS) পদ্ধতিতে জল পরিশোধনের জন্য কী কী ধাপ অনুসরণ করতে হয়?
সূর্যের আলো জল পরিশোধনের কাজে ব্যবহৃত হয়। এই পদ্ধতিকে Solar Water Disinfection (SODIS) বলা হয়। এই পদ্ধতিতে জলের মধ্যে উপস্থিত Micro Organism নষ্ট হয়ে যায়। এতে কোনো জ্বালানির প্রয়োজন হয় না। এই পদ্ধতিতে জল পরিশোধনের ধাপগুলি হল –
- প্রথমে বোতলগুলি ভালোভাবে ধুতে হবে।
- বোতলে জল ভরে ঢাকনাগুলি ভালোভাবে আটকাতে হবে।
- বোতলগুলিকে ছাদে বা টিনের চালের ওপর রাখতে হবে।
স্ফুটন পদ্ধতিতে কীভাবে জল পরিশোধন করা হয়? এই পদ্ধতির সীমাবদ্ধতা লেখো।
টিউবওয়েল বা পাইপলাইন থেকে প্রাপ্ত জলকে পরিশোধন করে পানের উপযুক্ত করার সবচেয়ে প্রাচীন পদ্ধতি হল স্ফুটন। উপযুক্ত পাত্রে পরিমাণমতো জল নিয়ে প্রায় 20 – 30 মিনিট 100°C উষ্ণতায় ফোটানো হয়। ফলে, জলে উপস্থিত রোগজীবাণুগুলি ধ্বংস হয়ে যায়। এবার জলকে ঠান্ডা করলে পাত্রের তলদেশে কিছু অপদ্রব্য থিতিয়ে পড়ে। আস্রাবণ পদ্ধতিতে অথবা পরিস্রাবণ পদ্ধতির মাধ্যমে স্বচ্ছ ও জীবাণু মুক্ত জলকে সংগ্রহ করা হয়।
স্ফুটন পদ্ধতিতে জল পরিশোধনের সীমাবদ্ধতা –
- স্ফুটন পদ্ধতিতে জলের মধ্যে উপস্থিত অধিকাংশ রোগজীবাণু বিনষ্ট হলেও কিছু তাপরোধী রোগজীবাণু থেকেই যায়।
- রোগজীবাণু ধ্বংস হলেও স্ফুটনের মাধ্যমে জলে উপস্থিত রাসায়নিক অপদ্রব্য ও বিষাক্ত পদার্থ অপসারিত হয় না।
- জলে দ্রবীভূত প্রয়োজনীয় ধাতব লবণ স্ফুটনের মাধ্যমে অদ্রাব্য পদার্থে পরিণত হয়ে থিতিয়ে পড়ে। ফলে, জলের স্বাদ নষ্ট হয়। এমনকি দেহের পক্ষে উপযোগী অনেক প্রয়োজনীয় খনিজ লবণ থেকেও আমরা বঞ্চিত হই।
- ভূগর্ভস্থ জলকে এই পদ্ধতিতে পরিশোধন করে পানীয় জল প্রস্তুত করা গেলেও নদী, হ্রদ প্রভৃতি বড়ো বড়ো জলাশয়ের জলকে এই পদ্ধতিতে পরিশোধন করা সময়সাপেক্ষ, জ্বালানির খরচও বেশি।
- ফোটানো জল বেশিদিন রাখলে পুনরায় রোগজীবাণু দ্বারা আক্রান্ত হওয়ার সম্ভাবনা থাকে।
- বেশি খরতাযুক্ত জল পাত্রে নিয়ে ফোটালে ওই পাত্রের তলদেশে কঠিন আস্তরণ পড়ে এবং পাত্রটি ধীরে ধীরে ক্ষয়প্রাপ্ত হয়।

দৈনন্দিন জীবনে পান করার উদ্দেশ্যে যে জল ব্যবহার করা হয় তা সেরামিক ক্যান্ডেল ও ওয়াটার পিউরিফায়ারের সাহায্যে কীভাবে পরিশোধিত হয়?
সেরামিক ক্যান্ডেলের সাহায্যে জল পরিশোধন – জলকে প্রথমে ফুটিয়ে জীবাণুমুক্ত করা হয়। এরপর ওই ফোটানো জলকে কিছুক্ষণ স্থিরভাবে রেখে দিলে জল মধ্যস্থ অদ্রাব্য ভাসমান অশুদ্ধি নীচে থিতিয়ে পড়ে। উপর থেকে স্বচ্ছ জলকে ওয়াটার ফিলটারে ঢেলে নিয়ে সেরামিক ক্যান্ডেলের সাহায্যে ফিলটার করে ব্যবহার করা যেতে পারে।
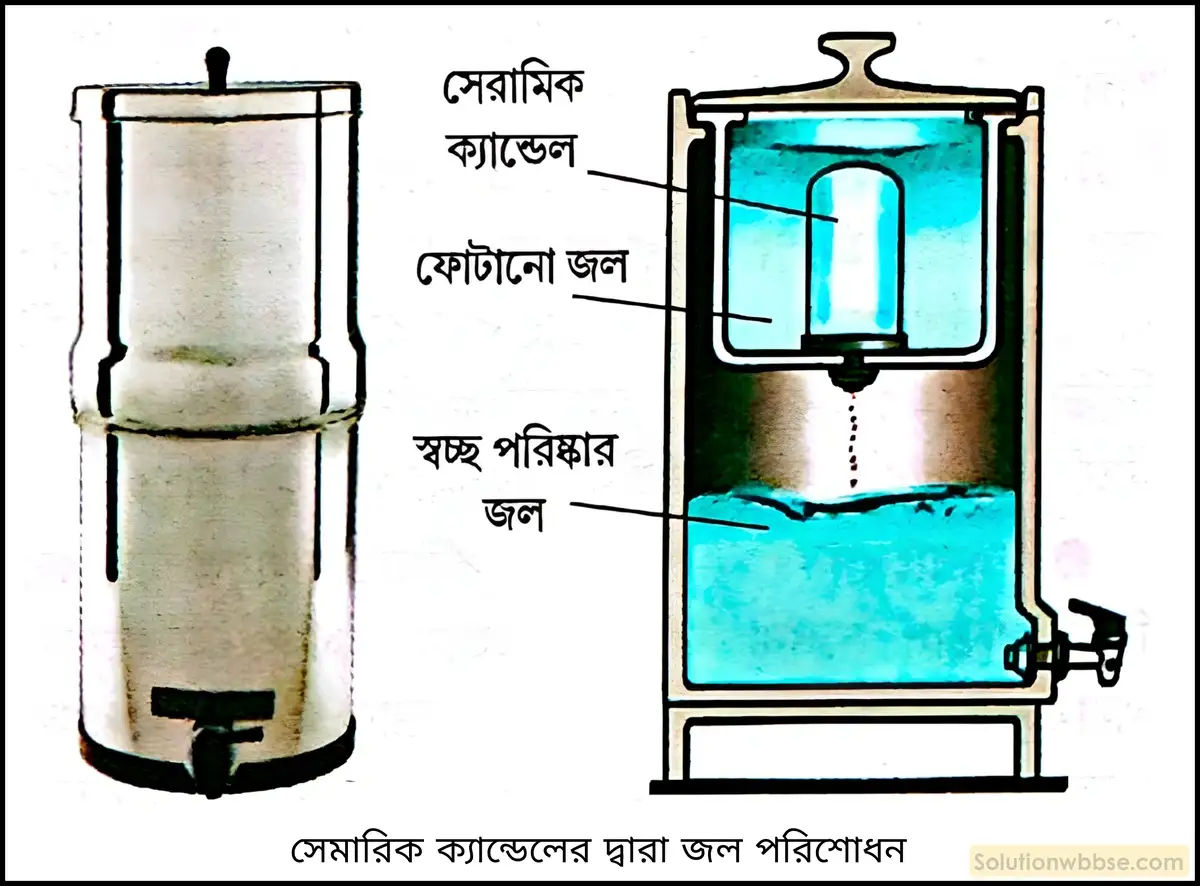
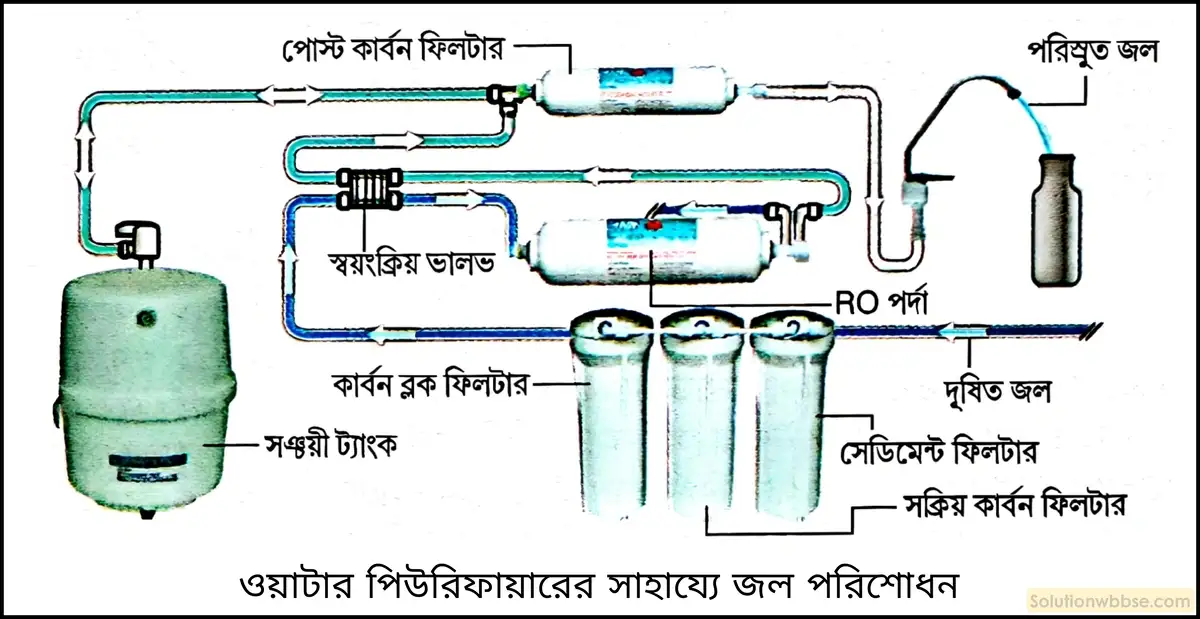
ওয়াটার পিউরিফায়ারের সাহায্যে জল পরিশোধন – বর্তমানে যে-সমস্ত ওয়াটার পিউরিফায়ার ব্যবহৃত হয়, তাতে বিভিন্ন ধাপে কলের জলকে পরিশোধন করা হয়।

প্রথমে জলকে পর্যায়ক্রমিকভাবে সেডিমেন্ট ফিলটার, সক্রিয় কার্বন ফিলটার, কার্বন ব্লক ফিলটারে মধ্যে দিয়ে পাঠানো হয়। ফলে জলে থাকা পলি জাতীয় অপদ্রব্য এবং ক্লোরিন দূরীভূত হয়। এরপর জলকে বিপরীত অভিস্রবণ পদ্ধতিতে পরিস্রুত করা হয়, যা জলে থাকা বিভিন্ন দূষিত পদার্থকে (আর্সেনিক, ক্লোরাইড, ব্রোমাইড, লেড, নাইট্রেট) দূরীভূত করে। সবশেষে জলকে পোস্ট কার্বন ফিলটারের মধ্যে দিয়ে পাঠানো হয় এবং বিশুদ্ধ জল সঞ্চয়ী ট্যাংকে জমা হয়। কিছু কিছু ওয়াটার পিউরিফায়ারে জলকে UV ল্যাম্পের থেকে নির্গত UV -রশ্মির সাহায্যে জীবাণুমুক্ত করা হয়।
ক্লোরিনের সাহায্যে জল পরিশোধনের মূল অসুবিধাগুলি উল্লেখ করো।
ক্লোরিনেশন পদ্ধতিতে জল পরিশোধনের অসুবিধা –
- ক্লোরিন জলে মিশ্রিত জৈব যৌগের সঙ্গে বিক্রিয়া করে স্বাস্থ্যের পক্ষে ক্ষতিকারক পদার্থ, যেমন – হ্যালো অ্যাসিটিক অ্যাসিড, ট্রাইহ্যালো মিথেন (THM) প্রভৃতি উৎপন্ন করে। বিশেষত মিথেনের যৌগগুলি মানুষের দেহে প্রবেশ করে যকৃত ও বৃক্কে ক্যানসার, হার্টের অসুখ, অচেতনতা এমনকি মৃত্যুরও কারণ হয়ে উঠতে পারে।
- জলে অ্যামোনিয়া মিশে থাকলে ক্লোরিনের সঙ্গে বিক্রিয়ায় বিষাক্ত ক্লোরামিন (ClNH2) উৎপন্ন করে যা শরীরের পক্ষে বিপজ্জনক।
- জলের মধ্যে ক্লোরিন মিশে থাকায় জলের স্বাদ নষ্ট হয় এবং ক্লোরিনের গন্ধ থেকে যায়।
- জলের ক্লোরিনেশনে ক্লোরিন গ্যাস জলে দ্রবীভূত হয়ে হাইড্রোক্লোরিক অ্যাসিড (HCl) ও হাইপোক্লোরাস অ্যাসিড (HOCl) উৎপন্ন করায় জল আম্লিক হয়ে যায়।
- ক্লোরিনেশন পদ্ধতিতে জলকে জীবাণুমুক্ত করে কিছুদিন রেখে দিলে উদ্বায়ী ক্লোরিন গ্যাস বেরিয়ে বাতাসে মেশে। ফলে জীবাণুগুলি পুনরায় সক্রিয় হয়ে ওঠার সম্ভাবনা থাকে।
- কিছু প্যাথোজেনিক জীবাণুকে ক্লোরিনেশন পদ্ধতিতে ধ্বংস করা যায় না।
UV -রশ্মি ব্যবহারের মাধ্যমে জল পরিশোধন ব্যবস্থার সুবিধা ও অসুবিধাগুলি উল্লেখ করো।
UV -রশিার দ্বারা জল পরিশোধনের সুবিধাগুলি হল –
- UV -রশ্মির দ্বারা জল পরিশোধন করলে জলের স্বাদ ও গন্ধ অপরিবর্তিত থাকে।
- এই পদ্ধতিতে জল পরিশোধন করলে তুলনামূলক কম সময় লাগে।
- জলে উপস্থিত রোগজীবাণু বহনকারী ব্যাকটেরিয়া, ভাইরাস ধ্বংস করার ক্ষেত্রে এই পদ্ধতি অধিক কার্যকর।
- এই পদ্ধতিতে জল পরিশোধনের ক্ষেত্রে জলের pH -এর মানের কোনো পরিবর্তন হয় না।
- রাসায়নিক পদার্থ ছাড়াই জল পরিশোধিত হয়। ফলে, রাসায়নিক পদার্থ জলে মিশে যাওয়ার সম্ভাবনা থাকে না। এই পদ্ধতি অন্যান্য রাসায়নিক পদ্ধতির তুলনায় কম খরচ সাপেক্ষ।

UV -রশ্মি ব্যবহারের মাধ্যমে জল পরিশোধন ব্যবস্থার অসুবিধা –
- জলের মধ্যে দিয়ে UV রশ্মি চালনা করার আগে জলকে ফিলটার করে নিতে হবে। জল বেশি ঘোলাটে হলে এই রশ্মির কার্যকারিতা কমে যায়, কারণ – জলে উপস্থিত অপদ্রব্য দ্বারা এই রশ্মির কিছু অংশ শোষিত ও বিচ্ছুরিত হয়। ফলে, ক্ষতিকর জীবাণুগুলির ওপর এই রশ্মির কার্যকারিতা কমে যায়।
- অতিরিক্ত সংক্রামকনাশক না থাকার জন্য UV রশ্মি দ্বারা পরিশোধিত জল বেশিক্ষণ রাখা যায় না, কারণ – জল পরিশোধনের পর সাধারণ আলোর সংস্পর্শে থাকলে পুনরায় রোগজীবাণু জলের মধ্যে সংক্রামিত হওয়ার সম্ভাবনা থাকে।
খর জল ও মৃদু জলের উদাহরণসহ সংজ্ঞা দাও।
খর জল (Hard water) – যে জলে সাবান ঘষলে তা সহজে দ্রবীভূত হয়ে ফেনা উৎপন্ন করে না, তাকে খর জল বলে।
খর জলের উদাহরণ – টিউবওয়েলের জল, নদীর জল ইত্যাদি।

মৃদু জল (Soft water) – যে জলে সাবান ঘষলে তা সহজে দ্রবীভূত হয়ে ফেনা উৎপন্ন করে, তাকে মৃদু জল বলে।
মৃদু জলের উদাহরণ – পাতিত জল, বৃষ্টির জল ইত্যাদি।

জলের খরতার কারণ উল্লেখ করো।
খরতার কারণ – খর জলে নানা ধাতব লবণ দ্রবীভূত থাকে, যেমন – ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রন ইত্যাদির কার্বনেট, বাইকার্বনেট, ক্লোরাইড ও সালফেট লবণ। সাবান হল উচ্চ আণবিক গুরুত্ববিশিষ্ট বিভিন্ন জৈব ফ্যাটি অ্যাসিডের সোডিয়াম বা পটাশিয়াম লবণ। এই আয়নগুলি সাবানের সঙ্গে বিক্রিয়ায় সাদা অধঃক্ষেপ (অদ্রাব্য) উৎপন্ন করে। ফলে, সাবান ফেনা তৈরি করতে পারে না। এই আয়নগুলি অধঃক্ষেপ হিসেবে জল থেকে দূরীভূত হলে তারপর ফেনা উৎপন্ন হয়।
খরতার মাত্রা কাকে বলে?
খরতার মাত্রা – জলের কোনো নমুনায় প্রতি দশ লক্ষ ভাগ ওজনে উপস্থিত খরতা সৃষ্টিকারী বিভিন্ন লবণের সমতুল্যাঙ্ক পরিমাণ ক্যালশিয়াম কার্বনেট যত ভাগ ওজনের ক্যালশিয়াম কার্বনেটকে নির্দেশ করে, সেই সংখ্যাকে ওই জলের নমুনার খরতার মাত্রা বলে। খরতার মাত্রাকে ppm (parts per million) এককে প্রকাশ করা হয়।
কোনো জলে খরতা 220 ppm বলতে কী বোঝায়?
কোনো জলের খরতা 220 ppm বলতে বোঝায় ওই নমুনার জলের প্রতি দশ লক্ষ ভাগ ওজনে 220 ভাগ ওজনের ক্যালশিয়াম কার্বনেট (CaCO3) অথবা, ওর তুল্য পরিমাণ খরতা উৎপাদনকারী লবণ উপস্থিত।
খরতা অনুযায়ী জল কয় প্রকার ও কী কী? প্রত্যেক প্রকারের সংজ্ঞা দাও।
অথবা, খর জল কত প্রকার ও কী কী? প্রত্যেক প্রকারের সংজ্ঞা দাও।
খরতা দুই প্রকার। যথা – স্থায়ী খরতা ও অস্থায়ী খরতা। অনুরূপে খর জলও দুই প্রকার। যথা – স্থায়ী খর জল ও অস্থায়ী খর জল।
স্থায়ী খরতা ও স্থায়ী খর জল – জলে খরতা সৃষ্টিকারী ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রন ইত্যাদির ক্লোরাইড, সালফেট ইত্যাদি লবণ দ্রবীভূত থাকলে যে খরতা সৃষ্টি হয়, তাকে স্থায়ী খরতা বলে। স্থায়ী খরতাযুক্ত জলকে স্থায়ী খর জল বলে। এই খরতা সহজে দূর করা যায় না, শুধুমাত্র বিশেষ কিছু রাসায়নিক পদ্ধতি দ্বারা পৃথক করা যায়।
অস্থায়ী খরতা ও অস্থায়ী খর জল – জলে খরতা সৃষ্টিকারী ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রন ইত্যাদির বাইকার্বনেট লবণ দ্রবীভূত থাকলে যে খরতা সৃষ্টি হয়, তাকে অস্থায়ী খরতা বলে। অস্থায়ী খরতাসম্পন্ন জলকে অস্থায়ী খর জল বলে। এই খরতা স্ফুটন পদ্ধতিতে সহজেই দূর করা যায়।
খর জল ব্যবহারের সুবিধাগুলি লেখো।
খর জল ব্যবহারের সুবিধা –
- খর জলে সামান্য পরিমাণ খনিজ পদার্থ ও ক্যালশিয়াম লবণ দ্রবীভূত থেকে জলের স্বাদ বাড়ায় ও মানুষের দেহ গঠনে সাহায্য করে। কিন্তু অতি মৃদু জল স্বাদহীন হয়।
- খর জল লেড পাইপের মধ্যে দিয়ে প্রবাহিত হওয়ার সময় লেড পাইপের অভ্যন্তরের দেয়ালে অদ্রাব্য লেড সালফেটের একটি স্তর সৃষ্টি করে। ফলে, লেডের বিষক্রিয়া হয় না কিন্তু মৃদু জলে লেড দ্রবীভূত হয়ে লেডের বিষাক্ত লবণ উৎপন্ন করে। খর জল ব্যবহারের বিভিন্ন অসুবিধা থাকা সত্ত্বেও তাই কয়েকটি বিশেষক্ষেত্রে খর জলের ব্যবহার সুবিধাজনক।
খর জল ব্যবহারের অসুবিধাগুলি লেখো।
খর জল ব্যবহারের অসুবিধা –
- জামাকাপড় পরিষ্কার করতে খর জল ব্যবহার করা হয় না। খর জলে দ্রবীভূত ক্যালশিয়াম, ম্যাগনেশিয়াম এবং আয়রনের লবণ অপসারিত না হওয়া পর্যন্ত সাবানের ফেনা হয় না। ফলে, সাবানের অপচয় হয়। লৌহঘটিত লবণ জল থেকে দূর না করলে জামাকাপড়ে বাদামি রঙের দাগ পড়তে পারে।
- রান্নার কাজে খর জল ব্যবহার করা উচিত নয়, কারণ – খর জলে বিভিন্ন ধাতুর, যেমন – Ca, Mg ইত্যাদির লবণ উপস্থিত থাকে। ফলে, এই জলে রান্না করলে খাদ্যদ্রব্য সহজে সেদ্ধ হয় না।
- অতিরিক্ত খরতাযুক্ত জল পান করা স্বাস্থ্যের পক্ষে ক্ষতিকারক।
- রান্নার পাত্রে বা কেটলিতে খর জল ব্যবহার করলে এবং উত্তপ্ত করলে পাত্রের গায়ে অদ্রাব্য, তাপের কুপরিবাহী ধাতব কার্বনেট \(\left(CO_3^{2-}\right)\) ও সালফেট \(\left(SO_4^{2-}\right)\) প্রভৃতি লবণের আস্তরণ পড়ে। ফলে, পাত্রের ক্ষতি হয় এবং জল সহজে গরম হয় না, বেশি পরিমাণে জ্বালানি খরচ হয়।
- কাগজ, কৃত্রিম সিল্ক প্রস্তুতিতে ও রঞ্জন শিল্পে খর জল ব্যবহার করা যায় না, কারণ – বাদামি রঙের (আয়রনের লবণ বাদামি ফেরিক হাইড্রক্সাইডে পরিণত হয়) দাগ পড়ে।
খর জল লন্ড্রিতে ব্যবহারের অসুবিধা কী? এই অসুবিধা কীভাবে দূর করা যায়?
খর জল লন্ড্রিতে ব্যবহারের অসুবিধা –
- খর জল ব্যবহার করলে সাবানের অযথা অপচয় হয়। সাবানের খরচ বৃদ্ধি পায়।
- জলে আয়রনের লবণ উপস্থিত থাকার কারণে জামাকাপড়ে হলুদ ছোপ পড়ে।
খর জল ব্যবহারের অসুবিধা দূরীকরণ – খর জলে ডিটারজেন্ট ব্যবহার করে এই অসুবিধা দূর করা যায়। ডিটারজেন্টের সঙ্গে খর জলের বিক্রিয়ায় যে ক্যালশিয়াম, ম্যাগনেশিয়াম ও আয়রনঘটিত লবণ উৎপন্ন হয় তা জলে দ্রাব্য। তাই ডিটারজেন্টে অনেক সহজেই ফেনা উৎপন্ন হয় এবং ডিটারজেন্টের খরচ কম হয়।
জলের অস্থায়ী খরতা দূরীভূত করা হয় কীভাবে?
জলের অস্থায়ী খরতা দূরীকরণ – স্ফুটন পদ্ধতিতে জলের অস্থায়ী খরতাকে দূর করা যায়। অস্থায়ী খর জলকে ফোটালে এতে উপস্থিত ক্যালশিয়াম ও ম্যাগনেশিয়াম বাইকার্বনেট লবণ বিয়োজিত হয়ে অদ্রাব্য কার্বনেট লবণরূপে অধঃক্ষিপ্ত হয় এবং কার্বন ডাইঅক্সাইড নির্গত হয়। ফিলটার করে অদ্রাব্য কার্বনেট লবণগুলিকে পৃথক করে নিলেই পরিস্রুতরূপে মৃদু জল পাওয়া যায়।
Ca(HCO3)2 = CaCO3↓ + CO2↑ + H2O
Mg(HCO3)2 = MgCO3↓ + CO2↑ + H2O
এই ম্যাগনেশিয়াম কার্বনেট জলে সামান্য দ্রাব্য হওয়ায় শুধু স্ফুটন পদ্ধতিতে ম্যাগনেশিয়াম বাইকার্বনেট ঘটিত অস্থায়ী খরতা সম্পূর্ণরূপে দূরীভূত হয় না। জলের মধ্যে আয়রন বাইকার্বনেট দ্রবীভূত থাকলে তা স্ফুটনের দ্বারা একইভাবে দূরীভূত হয়।
Fe(HCO3)2 = FeCO3 + CO2↑ + H2O
উৎপন্ন ফেরাস কার্বনেট বায়ুর অক্সিজেনের সংস্পর্শে জারিত হয়ে বাদামি বর্ণের ফেরিক হাইড্রক্সাইড রূপে অধঃক্ষিপ্ত হয়।
আয়ন বিনিময়কারী রেজিন কত প্রকার ও কী কী? ক্যাটায়ন বিনিময়কারী রেজিন ও অ্যানায়ন বিনিময়কারী রেজিন বলতে কী বোঝায়?
রেজিনের প্রকারভেদ – রেজিন প্রকৃতপক্ষে উচ্চ আণবিক গুরুত্ববিশিষ্ট জৈব যৌগ। এটি কৃত্রিম উপায়ে প্রস্তুত করা হয়।
আয়ন বিনিময়কারী রেজিন দুই প্রকার। যথা –
- ক্যাটায়ন বিনিময়কারী রেজিন এবং
- অ্যানায়ন বিনিময়কারী রেজিন।
ক্যাটায়ন বিনিময়কারী রেজিন – এই ধরনের রেজিনে একটি বৃহদাকার হাইড্রোকার্বন মূলকের (R-) সঙ্গে সালফোনিক অ্যাসিড (-SO3H) বা কার্বক্সিল (-COOH) মূলক যুক্ত থাকে। এই রেজিনগুলিকে সাধারণত RSO3H বা RCO2H বা সংক্ষেপে R-H দ্বারা প্রকাশ করা হয়। ক্যাটায়ন বিনিময়কারী রেজিনে উপস্থিত H+ আয়নের সঙ্গে খর জলে উপস্থিত Ca2+, Mg2+, K+ প্রভৃতি ক্যাটায়নের বিনিময় ঘটে। ফলে, জল থেকে খরতা সৃষ্টিকারী ক্যাটায়নগুলি দূরীভূত হয়ে মৃদু জলে পরিণত হয়।
অ্যানায়ন বিনিময়কারী রেজিন – অ্যানায়ন বিনিময়কারী রেজিন হল উচ্চ আণবিক গুরুত্ব সম্পন্ন অ্যামিনো মূলক (-NH2) যুক্ত যৌগ যা জলে উপস্থিত অ্যানায়ন দূর করে (OH– আয়ন ব্যতীত)। একে সংক্ষেপে RNH2 দ্বারা প্রকাশ করা হয়। জলের মধ্যে এটি \(R\overset+NH_3OH^-\) রূপে অবস্থান করে।
\(R-NH_2+H_2O\rightarrow R\overset+NH_3OH^-\)
এই রেজিনগুলিতে অবস্থিত \(OH^-\) আয়নের সঙ্গে খর জলে উপস্থিত \(Cl^-,\;SO_4^{2-}\) প্রভৃতি অ্যানায়নের বিনিময় ঘটে অর্থাৎ, খর জল মৃদু জলে পরিণত হয়।
আয়ন বিনিময় পদ্ধতিতে জলের স্থায়ী খরতা দূর করা হয় কীভাবে?
আয়ন বিনিময় রেজিন পদ্ধতিতে জলের স্থায়ী খরতা দূরীকরণ – আয়ন বিনিময় পদ্ধতিতে উপযুক্ত রেজিন ব্যবহার করে জলের স্থায়ী ও অস্থায়ী খরতা দূর করা যায়। রেজিন হল কৃত্রিম উপায়ে প্রস্তুত উচ্চ আণবিক গুরুত্বসম্পন্ন জৈব যৌগ। এগুলি প্রধানত সালফোনিক অ্যাসিড যৌগ অর্থাৎ, এতে SO3H মূলক উপস্থিত থাকে।
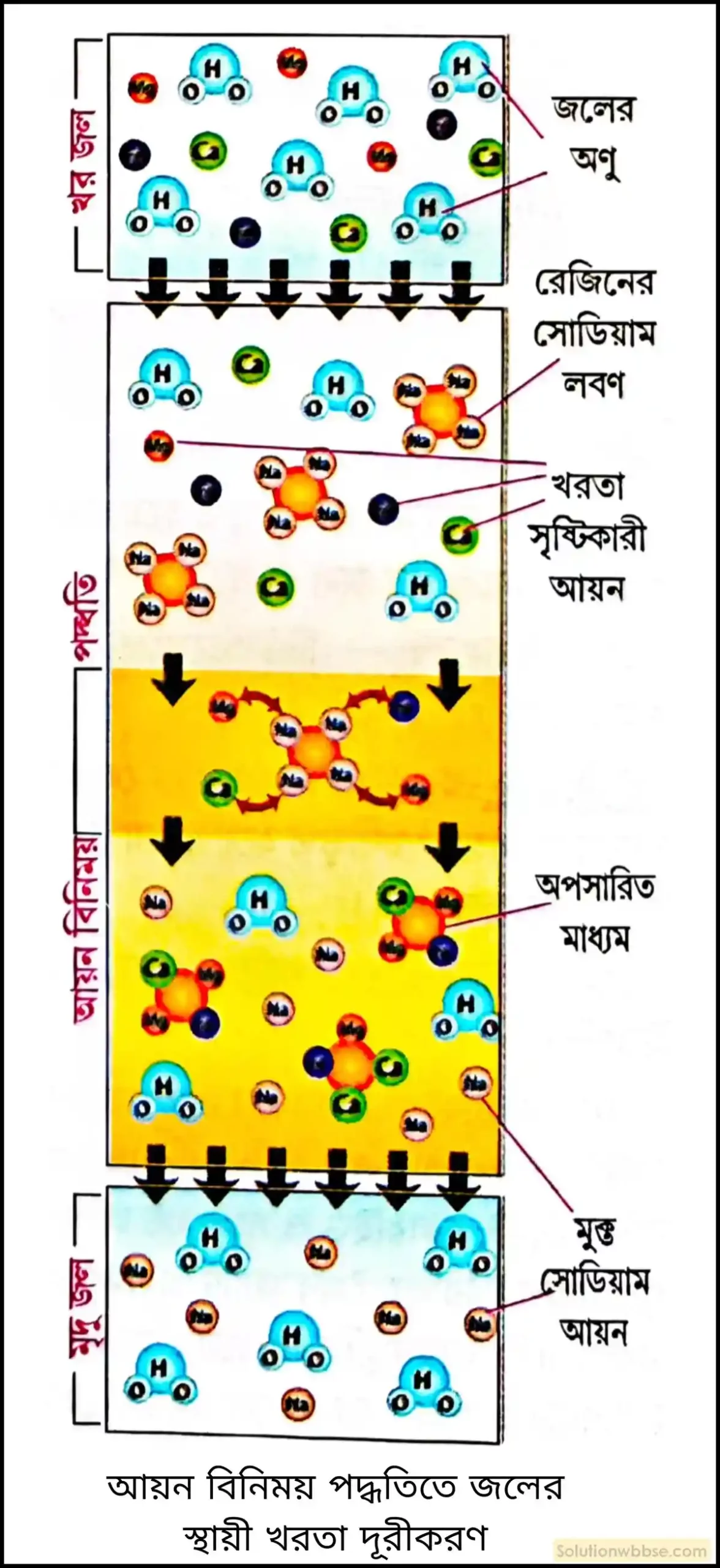
প্রথমে ছোটো দানার রেজিন স্তরের উপর দিয়ে NaCl দ্রবণ প্রবাহিত করে রেজিনকে সোডিয়াম লবণে পরিণত করা হয়।
R-SO3H + NaCl → R-SO3Na + HCl (R = রেজিনের জৈব অংশ)
খর জলকে এই রেজিন স্তরের মধ্যে দিয়ে চালনা করলে জলের খরতা দূরীভূত হয়, কারণ – খর জল মধ্যস্থ Ca++, Mg++ বা Fe++ আয়নের সঙ্গে রেজিনে উপস্থিত Na+ আয়নের বিনিময় ঘটে এবং খর জল মৃদু জলে পরিণত হয়।
2RSO3Na + Ca++ → (RSO3)2Ca↓ + 2Na+
2RSO3Na + Mg++ → (RSO3)2Mg↓ + 2Na+
2RSO3Na + Fe++ → (RSO3)2 Fe↓ + 2Na+
জিওলাইট বা পারমুটিট পদ্ধতি লেখো।
জিওলাইট বা পারমুটিট পদ্ধতি – জিওলাইট হল প্রকৃতিতে প্রাপ্ত জটিল খনিজ লবণ। সোডিয়াম অ্যালুমিনিয়াম সিলিকেটের সঙ্গে জলের অণু যুক্ত থাকে (Na2O⋅Al2O3⋅xSiO2⋅ yH2O)। কৃত্রিমভাবে প্রস্তুত করা জিওলাইটকে পারমুটিট বলে। একে সংক্ষেপে Na2Ze রূপে লেখা হয়। এই পদ্ধতিতে খর জলকে স্তম্ভের মধ্যে রাখা পারমুটিটের মধ্যে দিয়ে ধীরে ধীরে প্রবাহিত করলে স্থায়ী এবং অস্থায়ী খর জলের Ca2+, Mg2+, Fe2+ আয়নের সঙ্গে পারমুটিটের Na+ আয়নের বিনিময় ঘটে মৃদু জল পাওয়া যায়। খরতা দূরীভূত হলেও মৃদু জলে থাকা সমপরিমাণ Na -লবণ দূরীভূত হয় না। অর্থাৎ, জলটি আয়নমুক্ত নয়।
Na2Ze + Ca(HCO3)2 = 2NaHCO3 + CaZe
Na2Ze + CaCl2 = 2NaCl + CaZe
Na2Ze + MgSO4 = Na2SO4 + MgZe
সুতরাং, মৃদু জলে NaHCO3, NaCl, Na2SO4 ইত্যাদি লবণ দ্রবীভূত থাকে। পারমুটিটে Ca2+ ও Mg2+ আয়ন CaZe এবং MgZe রূপে থাকে।
কীভাবে ক্যাটায়ন বিনিময়কারী রেজিন ও অ্যানায়ন বিনিময়কারী রেজিনকে পুনরুজ্জীবিত করা যায় বিক্রিয়াসহ লেখো।
অথবা, জলের স্থায়ী খরতা দূর করার রেজিন কিছুদিন ব্যবহার করার পর তার ক্ষমতা পুনরুদ্ধার করা যায় কীভাবে?
দীর্ঘদিন ব্যবহারের ফলে যখন ক্যাটায়ন বিনিময়কারী রেজিন ও অ্যানায়ন বিনিময়কারী রেজিন তার কার্যক্ষমতা (বিনিময় ক্ষমতা) হারিয়ে ফেলে নিষ্ক্রিয় হয়ে পড়ে। তখন এদেরকে পুনরুজ্জীবীকরণ করা হয়। নিষ্ক্রিয় ক্যাটায়ন বিনিময়কারী রেজিনের মধ্যে দিয়ে লঘু [2M] HCl বা লঘু [2M] H2SO4 -এর দ্রবণ চালনা করলে রেজিন পুনরায় তার কার্যক্ষমতা ফিরে পায়।
(RSO3)2Mg + H2SO4 = 2RSO3H + MgSO4
আবার, নিষ্ক্রিয় অ্যানায়ন বিনিময়কারী রেজিন স্তরের মধ্যে দিয়ে লঘু [2M] NaOH দ্রবণ চালনা করলে তা পুনরায় সক্রিয় হয়ে ব্যবহারযোগ্য হয়ে ওঠে।
(RNH3)2SO4 + 2NaOH = 2[RNH3]+OH– + Na2SO4
আয়নমুক্ত জল কাকে বলে?
আয়নমুক্ত জল (Deionised water) – যে জলে হাইড্রোজেন আয়ন (H+) ছাড়া অন্য কোনো ক্যাটায়ন থাকে না এবং হাইড্রক্সিল আয়ন (OH–) ছাড়া অন্য কোনো অ্যানায়ন থাকে না, তাকে আয়নমুক্ত জল বলে।
আয়নমুক্ত জল কোন্ পদ্ধতিতে প্রস্তুত করা হয়? (বিক্রিয়াসহ লেখো)
আয়ন বিনিময় পদ্ধতিতে উপযুক্ত রেজিন ব্যবহারের মাধ্যমে H+ ও OH– আয়ন ব্যতীত জলে উপস্থিত খরতা সৃষ্টিকারী অন্যান্য সমস্ত আয়ন দূরীভূত করে আয়নমুক্ত জল প্রস্তুত করা হয়। এই পদ্ধতিতে দুই প্রকার রেজিন (ক্যাটায়ন ও অ্যানায়ন বিনিময়কারী রেজিন) ব্যবহার করে খর জলকে মৃদু করা হয়। দ্রাব্য লবণযুক্ত জলকে প্রথমে ক্যাটায়ন বিনিময়কারী রেজিন \(\left(RSO_3^-H^+\right)\) স্তরের মধ্যে দিয়ে চালনা করলে জলের মধ্যে থাকা Ca2+, Mg2+, Na+, Fe2+ প্রভৃতি রেজিনে প্রবেশ করে দূরীভূত হয় এবং তুল্য পরিমাণ H+ আয়ন রেজিন থেকে জলে প্রবেশ করে। এক্ষেত্রে জলের মধ্যে উপস্থিত ধাতব আয়নের সঙ্গে রেজিন মধ্যস্থ H+ আয়নের বিনিময় ঘটে।
2RSO3H + CaCl2 → (RSO3)2Ca ↓ + 2HCl
2RSO3H + MgSO4 → (RSO3)2Mg + + H2SO4
2RSO3H + Fe(HCO3)2 → (RSO3)2Fe ↓ + 2H2CO3
RSO3H + NaCl → RSO3Na ↓ + HCl
ক্যাটায়ন বিনিময়কারী রেজিন ব্যবহার করার পর জলে ক্যাটায়ন হিসেবে শুধুমাত্র H+ আয়ন উপস্থিত থাকে এবং অ্যানায়ন হিসেবে \(Cl^-,\;SO_4^{2-},\;CO_3^{2-}\) প্রভৃতি থেকে যায়।
এবার ধাতব ক্যাটায়ন মুক্ত জলকে অ্যানায়ন বিনিময়কারী রেজিন \(\left(R-\overset+NH_3OH^-\right)\) স্তরের মধ্যে দিয়ে চালনা করলে জলের মধ্যে উপস্থিত অ্যানায়নগুলির সঙ্গে রেজিনে উপস্থিত \(OH^-\) আয়নের বিনিময় ঘটে রেজিনের স্তরে প্রবেশ করে এবং তুল্য পরিমাণ \(OH^-\) আয়ন জলে প্রবেশ করে।
\(R\overset+NH_3OH^-+Cl^-\rightarrow RNH_3Cl\downarrow+OH^-\)
\(2R\overset+NN_3OH^-+SO_4^{2-}\rightarrow{\left(RNH_3\right)}_2SO_4\downarrow+2OH^-\)
\(2R\overset+NH_3OH^-+HCO_3^-\rightarrow R\overset+NH_3CO_3^-\downarrow+OH^-\)
শেষে সংগৃহীত জলের মধ্যে H+ আয়ন ছাড়া অন্য কোনো ক্যাটায়ন এবং OH– আয়ন ছাড়া অন্য কোনো অ্যানায়ন থাকে না। H+ ও OH– আয়ন পরস্পর যুক্ত হয়ে বিশুদ্ধ জল উৎপন্ন করে। ক্যাটায়ন ও অ্যানায়ন বিনিময়কারী রেজিন স্তর অতিক্রম করে নির্গত জল সম্পূর্ণ আয়নমুক্ত হয়। তাই এই জলকে আয়নমুক্ত জল বলে।
আয়নমুক্ত জলের ব্যবহার লেখো।
আয়নমুক্ত জলের ব্যবহার –
- পরীক্ষাগারে বিভিন্ন পরীক্ষানিরীক্ষার কাজে আয়নমুক্ত জল ব্যবহৃত হয়।
- রাসায়নিক কারখানায় উচ্চ চাপে স্টিম উৎপাদনে ও রেলওয়ে লোকোমোটিভে আয়নমুক্ত জল ব্যবহৃত হয়।
- মাইক্রোইলেকট্রনিক শিল্পে, প্রসাধনী শিল্পে, ঔষধ শিল্পে দ্রাবক হিসেবে আয়নমুক্ত জল ব্যবহৃত হয়।
সম্পূর্ণ আয়নমুক্ত হওয়ায় (H+ ও OH– আয়ন ব্যতীত) ব্যাটারিতে এই জল ব্যবহার করা হয়। - এই জল অত্যন্ত মৃদু হওয়ায় বিভিন্ন বয়লারে এর বিপুল ব্যবহার হয়।
- বস্ত্রশিল্পেও আয়নমুক্ত জল ব্যবহার করা হয়।
পাতিত জল কাকে বলে?
পাতিত জল (Distilled water) – যে জলে কোনো অশুদ্ধি, জীবাণু, তড়িৎ-অবিশ্লেষ্য, জৈবপদার্থ, দ্রবীভূত গ্যাস কোনো কিছুই থাকে না তাকে পাতিত জল বলে।
জলদূষণ কাকে বলে?
জলদূষণ (Water Pollution) – বিভিন্ন জৈব ও অজৈব বর্জ্য পদার্থ, রাসায়নিক সার, কীটনাশক, ক্ষতিকর জীবাণু প্রভৃতি জলের সঙ্গে মিশে যাওয়ার ফলে যদি জলের ভৌত, রাসায়নিক, জৈব বৈশিষ্ট্য ও গুণগত মানের পরিবর্তন হয় এবং তার ফলে জল ব্যবহারের অযোগ্য হয়ে পড়ে ও জীবজগতের ক্ষতির কারণ হয়ে ওঠে তখন জলের এরূপ অবস্থাকে জলদূষণ বলে।
জলদূষণের কারণগুলি লেখো।
জলদূষণের কারণ –
- পয়ঃপ্রণালীর দূষিত জল দ্বারা জলদূষণ – শহরাঞ্চলের বিভিন্ন নালা নর্দমাবাহিত নোংরা আবর্জনা ও বিষাক্ত বর্জ্য পদার্থ নদী, জলাশয় ও সমুদ্রে মিশে জল দূষিত করে।
- কলকারখানা নিঃসৃত বর্জ্য পদার্থ দ্বারা জলদূষণ – শিল্পাঞ্চলে বিভিন্ন কলকারখানা থেকে নিঃসৃত বিষাক্ত বর্জ্য পদার্থ, যেমন – পারদ, সিসা, ক্যাডমিয়াম, ক্রোমিয়াম, আর্সেনিক, দস্তা প্রভৃতি ধাতু জলে মিশে জলদূষণ ঘটায়।
- কীটনাশক দ্বারা জলদূষণ – চাষের জমিতে ফসলকে বিভিন্ন পোকামাকড়ের হাত থেকে রক্ষা করার জন্য নানা ধরনের বিষাক্ত কীটনাশক, যেমন – DDT, BHC, গ্যামাক্সিন, এনড্রিন, ক্লোরোভেন প্রভৃতি ব্যবহার করা হয়, যা বৃষ্টির জল দ্বারা বাহিত হয়ে বিভিন্ন জলাশয়, নদীনালার জলের সঙ্গে মিশে জলকে দূষিত করে তোলে।
- রাসায়নিক সার দ্বারা জলদূষণ – কৃষিতে ফলন বৃদ্ধি করার জন্য জমিতে বিভিন্ন রাসায়নিক সার, যেমন – ইউরিয়া, অ্যামোনিয়াম সালফেট, অ্যামোনিয়াম নাইট্রেট, মনো ক্যালশিয়াম ফসফেট প্রভৃতি ব্যবহার করা হয়, যা জল দ্বারা বাহিত হয়ে জলাশয় বা নদনদীতে মিশে জলদূষণ ঘটায়। তাছাড়াও কৃষিকার্যে ব্যবহৃত নাইট্রেট জাতীয় অজৈব সারের অতিরিক্ত অংশ বর্জ্যপদার্থ হিসেবে জলাশয়ে দ্রবীভূত হলে, ওই সারমিশ্রিত জলের প্রভাবে জলজ উদ্ভিদের দ্রুত বংশবৃদ্ধি ঘটে। জলজ উদ্ভিদের অতিবৃদ্ধির ফলে তাদের শ্বসনের জন্য প্রচুর পরিমাণ অক্সিজেন ব্যবহৃত হয়। এর ফলে জলে দ্রবীভূত অক্সিজেনের পরিমাণ দ্রুত হ্রাস পায়।
- গৃহস্থালির দৈনন্দিন আবর্জনা দ্বারা জলদূষণ – আমাদের দৈনন্দিন কাজকর্মের ফলে উৎপন্ন বিভিন্ন বর্জ্য পদার্থ, যেমন – কাচ, কাগজ, শাকসবজির খোসা, প্লাস্টিক প্রভৃতি অনেকসময় নিকটবর্তী জলাশয়ে ফেলা হয়। এই সমস্ত আবর্জনা থেকে তৈরি হওয়া বিষাক্ত ও রোগসৃষ্টিকারী জীবাণু জলে মিশে জল দূষিত করে। এছাড়া প্লাস্টিক জাতীয় বর্জ্য পদার্থ জৈববিশ্লিষ্ট নয়, অবিকৃত অবস্থায় জলাশয়ের তলদেশে জমা হয়ে জলের গভীরতা হ্রাস করে, যা জলচর প্রাণী ও মাছের পক্ষে ক্ষতিকর।
- ডিটারজেন্ট দ্বারা জলদূষণ – গৃহস্থালির কাজে, শিল্পে ব্যাপকভাবে ব্যবহৃত ডিটারজেন্ট নর্দমার জলের দ্বারা বাহিত হয়ে নদী, জলাশয়ে মেশে এবং জলের স্বাভাবিক ধর্মের পরিবর্তন করে জলদূষণ ঘটায়। ডিটারজেন্ট থেকে আসা দূষিত পদার্থ জলের পৃষ্ঠটান কমিয়ে তেল জাতীয় পদার্থের সঙ্গে মিশে ইমালসন বা অবদ্রব এবং ফেনার সৃষ্টি করে যা জলের উপরে ভাসতে থাকে। ফলে, সূর্যরশ্মি জলের মধ্যে প্রবেশ করতে পারে না। তাই জলের স্বাভাবিক উষ্ণতা বজায় থাকে না। ইমালসন বা অবদ্রব ও ফেনা সৃষ্টির ফলে জলে দ্রবীভূত অক্সিজেনের পরিমাণ কমে যায়। ফলে, জলজ উদ্ভিদ ও প্রাণীদের জীবন বিপন্ন হয়। ডিটারজেন্ট মধ্যস্থ ফসফেট যৌগ জলে অণুজীব ও শৈবালের সংখ্যাকে বাড়িয়ে তোলে। ফলে, জলের মধ্যে বসবাসকারী প্রাণীদের অক্সিজেনের অভাব ঘটে যা সামগ্রিকভাবে জলদূষণ ঘটায়। অধিকাংশ ডিটারজেন্ট জৈব-অবিশ্লেষ্য (Non-Biodegradable)। জলে এদের উপস্থিতি জলকে বিষাক্ত করে তোলে যা জলজ জীবদের জীবন বিপন্ন করে।
- খনিজ তেল দ্বারা জলদূষণ – বড়ো বড়ো বন্দরে নোঙর করা তৈলবাহী জাহাজ থেকে খনিজ তেল নিঃসৃত হয়ে জলে মিশে জলকে দূষিত করে। সমুদ্রে ভাসমান তৈলবাহী জাহাজে কোনো কারণে ছিদ্র থাকলে, সেই ছিদ্রপথে খনিজ তেল সমুদ্রের জলে মিশে জলদূষণ ঘটায়।
- তেজস্ক্রিয় পদার্থ দ্বারা জলদূষণ – পারমাণবিক চুল্লি থেকে নির্গত বিভিন্ন তেজস্ক্রিয় পদার্থ সমন্বিত আবর্জনা সমুদ্রগর্ভে নিক্ষিপ্ত করা হয়। পারমাণবিক বিস্ফোরণের দরুন সৃষ্ট বিভিন্ন তেজস্ক্রিয় পদার্থ বৃষ্টির জল দ্বারা বাহিত হয়ে নিকটবর্তী জলাশয়ে মিশে জলকে দূষিত করে।

ডিটারজেন্ট কৃষিক্ষেত্রে ব্যবহৃত কীটনাশক, সার প্রভৃতি দ্বারা জলদূষণের ফলে মানুষ ও অন্যান্য জলজ প্রাণীদের ওপর যে ক্ষতিকারক প্রভাব পড়ে তা সারণি আকারে উল্লেখ করো।
ডিটারজেন্ট এবং কৃষিক্ষেত্রে ব্যবহৃত কীটনাশক সার ব্যবহারের ক্ষতিকর প্রভাব –
| পদার্থ | ক্ষতিকর প্রভাব |
| ডিটারজেন্ট (সোডিয়াম ট্রাইপলি ফসফেট, অ্যালকিল বেঞ্জিন সালফোনেট) | জলে দ্রবীভূত অক্সিজেনের পরিমাণ হ্রাস পায়। ফলে, জলজ প্রাণীদের শ্বসন প্রক্রিয়া ব্যাহত হয়। জলজ প্রাণীদের জীবন বিপন্ন হয়। |
| কীটনাশক (ডিডিটি, গ্যামাক্সিন, ম্যালাথিয়ন, প্যারাথিয়ন, অ্যালড্রিন) | এই কীটনাশকগুলি অত্যন্ত ক্ষতিকর। এর প্রভাবে মাথাধরা, স্নায়বিক দুর্বলতা, পেশির শিথিলতা, ক্যানসার ইত্যাদি রোগ হয়। DDT -এর প্রভাবে মাছ ও অন্যান্য জলজ প্রাণীর প্রজনন ক্ষমতা হ্রাস পায়। এর ফলে বাস্তুতন্ত্রের ভারসাম্য বিনষ্ট হয়। |
| রাসায়নিক সার (ইউরিয়া, অ্যামোনিয়াম সালফেট, অ্যামোনিয়াম নাইট্রেট) | রাসায়নিক সারের যথেষ্ট ক্ষতিকর প্রভাব আছে। নাইট্রেটযুক্ত জল পান করলে শিশুদের ‘Blue Baby Syndrome’ রোগ হয়। এছাড়া নাইট্রেটের প্রভাবে ক্যানসার হয়। |
ইউট্রোফিকেশন এবং অ্যালগাল ব্লুম কী?
ইউট্রোফিকেশন (Eutrofication) – হ্রদ বা অন্য কোনো আবদ্ধ জলাশয়ে সার, কীটনাশক বা ডিটারজেন্টের বর্জ্য অংশ মিশে গেলে জলজ উদ্ভিদের পুষ্টিকর খাদ্যের পরিমাণ বৃদ্ধি পায়। এর ফলে জলজ উদ্ভিদের বৃদ্ধি ও বংশবিস্তার ত্বরান্বিত হয়। এই ঘটনাকে ইউট্রোফিকেশন বলা হয়।
অ্যালগাল ব্লুম (Algal Bloom) – প্রকৃতপক্ষে জলে বিভিন্ন আণুবীক্ষণিক শৈবালের দ্রুত বংশবৃদ্ধিকে অ্যালগাল ব্লুম বলা হয়। অ্যালগাল রুম স্বচ্ছ পরিষ্কার জলে এমনকি সামুদ্রিক পরিবেশেও দেখা যেতে পারে। স্বল্প সংখ্যক ফাইটোপ্ল্যাঙ্কটন এই প্রজাতির অন্তর্গত। স্বচ্ছ জলে ও সমুদ্রে যে ব্লুম দেখা যায় তা কৃষিক্ষেত্রে ব্যবহৃত কীটনাশক ও সারের দূষণের ফলে সৃষ্টি হয়। অ্যালগাল ব্লুম বাস্তুতন্ত্র ও মানুষের জীবনে কুপ্রভাব সৃষ্টি করে। এর বর্ণ সাধারণত সবুজ হয়, তবে শৈবালের প্রজাতির ওপর ভিত্তি করে এর বর্ণ হলদে-বাদামি বা লাল হতে পারে। উজ্জ্বল সবুজ ব্লুম প্রকৃতপক্ষে সায়ানো ব্যাকটেরিয়া নামক আণুবীক্ষণিক জীব।

ইউট্রোফিকেশনের ক্ষতিকারক প্রভাবগুলি লেখো।
ইউট্রোফিকেশনের ক্ষতিকারক প্রভাব –
- জলাশয়, পুকুর বা হ্রদে, জলজ উদ্ভিদ, শ্যাওলা ও আগাছা দ্রুত বৃদ্ধি পাওয়ার ফলে জলে দ্রবীভূত অক্সিজেনের পরিমাণ হ্রাস পায়। কারণ – ওই সমস্ত জলজ উদ্ভিদ, শ্যাওলা ও আগাছা নিজেদের শ্বসনের জন্য প্রচুর পরিমাণে জলে দ্রবীভূত অক্সিজেন শোষণ করে নেয়। ফলে, দ্রবীভূত অক্সিজেনের মান কমে যায়। মাছ ও অন্যান্য জলজ প্রাণীদের শ্বসনের জন্য প্রয়োজনীয় অক্সিজেনের অভাব ঘটে ও তারা মারা যায়।
- জলাশয়, পুকুর বা হ্রদে ওই সমস্ত জলজ উদ্ভিদের মৃত্যু ঘটলে তাদের দেহাবশেষ ক্রমাগত জলের নীচে জমা হয়। ফলে, জলাশয়টি মজে যেতে থাকে।
- এছাড়া অবাত শ্বসনকারী ব্যাকটেরিয়া অস্বাভাবিকভাবে বৃদ্ধি পায় এবং তারা বিভিন্ন বর্জ্য পদার্থের সঙ্গে বিক্রিয়া ঘটিয়ে মিথেন, অ্যামোনিয়া, হাইড্রোজেন সালফাইড প্রভৃতি দুর্গন্ধ সৃষ্টিকারী পদার্থ উৎপন্ন করে।
জলদূষণের ক্ষতিকর প্রভাবগুলি আলোচনা করো।
জলদূষণের ক্ষতিকারক প্রভাব –
মানুষের ওপর জলদূষণের প্রভাব –
- মানবদেহে দূষিত জলে উপস্থিত বিভিন্ন ভাইরাস, ব্যাকটেরিয়া ও জীবাণু দ্বারা বাহিত রোগ কলেরা, টাইফয়েড, জন্ডিস, আমাশয়, হেপাটাইটিস, চর্মরোগ প্রভৃতি দেখা দেয়।
- জলে ক্যাডমিয়াম ঘটিত দূষণের ফলে ‘ইতাই ইতাই’ রোগ দেখা দেয়। জলে পারদ, লেড মিশ্রিত হলে পেটের রোগ, চর্মরোগ দেখা যায়।
- জল আর্সেনিক দ্বারা দূষিত হলে আর্সেনিকোসিস, ব্ল্যাকফুট রোগ দেখা দেয়। ফ্লুওরিন দ্বারা জল দূষিত হলে অস্থিবিকৃতি, প্যারালাইসিস, অ্যালার্জি প্রভৃতি রোগের উদ্ভব হয়।
- নাইট্রেট আয়ন মিশ্রিত জল গ্রহণ করলে শিশুদের হিমোগ্লোবিনের ক্ষতি হয়, যা মিথেমোগ্লোবিনেমিয়া (Methemoglobinemia) এবং ‘ব্লু বেবি সিনড্রোম’ নামক রোগ সৃষ্টি করে। এছাড়া মানবদেহে নাইট্রেট আয়ন প্রবেশ করলে নাইট্রোসোঅ্যামিন জাতীয় যৌগের সৃষ্টি হতে পারে, যার প্রভাবে পাকস্থলীতে ক্যানসার (Stomach Cancer) হওয়ার প্রবণতা বৃদ্ধি পায়।
অন্যান্য প্রাণীদের ও উদ্ভিদের ওপর ক্ষতিকর প্রভাব –
- খনিজ তেল দ্বারা সমুদ্রে জলদূষণের ফলে মাছসহ বিভিন্ন জলজ জীবের মৃত্যু ঘটতে পারে।
- জলদূষণে পাখিরা ‘হাইপোথারমিয়া’ রোগে আক্রান্ত হয়।
- রাসায়নিক সার জলে মিশে জলকে দূষিত করে। এই দূষণের ফলে জলজ শ্যাওলার পরিমাণ বৃদ্ধি পায়, যার ফলে জলে বসবাসকারী মাছেদের ক্ষতি হয়।
- অনেক সময় জল দূষিত হওয়ার ফলে জলজ উদ্ভিদের মধ্যে বিষাক্ত পদার্থ জমা হয়।
মাটির ওপর জলদূষণের ক্ষতিকর প্রভাব –
- দূষিত জল চাষের জমিতে ব্যবহার করলে মাটির উর্বরতা হ্রাস পায়।
- দূষিত জল উদ্ভিদ কর্তৃক শোষিত হলে উৎপন্ন ফসলের উৎপাদন হ্রাস পেতে পারে এবং ফসলের গুণগত মান হ্রাস পায়।
জলদূষণের প্রতিকারের উপায়গুলি লেখো।
জলদূষণের প্রতিকারের উপায় –
- শিল্পাঞ্চলের বিভিন্ন কলকারখানা থেকে নিঃসৃত বর্জ্য পদার্থ যাতে সরাসরি জলে না মেশে তার দিকে নজর রাখতে হবে। প্রয়োজনে সেই সমস্ত পদার্থগুলি বিশোধন করার ব্যবস্থা নিতে হবে।
- পুকুরে বা নদীতে জীবজন্তুদের স্নান করা ও কাপড়কাচা বন্ধ করতে হবে।
- দৈনন্দিন জীবনের ময়লা আবর্জনা, গবাদিপশু ও মানুষের মলমূত্র, জীবজন্তুর মৃতদেহ জলাশয়ে ফেলা বন্ধ করতে হবে।
- নর্দমার জল যথাযথভাবে পরিশোধন করে নদীতে ফেলতে হবে।
- চাষের জমিতে বিষাক্ত কীটনাশক, নাইট্রেট এবং ফসফেটযুক্ত সারের মাত্রাতিরিক্ত ব্যবহার বন্ধ করতে হবে। জৈবভঙ্গুর কীটনাশক এবং জৈবসারের ব্যবহার বাড়াতে হবে।
- তৈলবাহী জাহাজ থেকে খনিজ তেল যাতে নদী বা সমুদ্রে না পড়ে তার জন্য প্রয়োজনীয় ব্যবস্থা গ্রহণ করতে হবে।
- ভূগর্ভস্থ জলের যথেচ্ছ ব্যবহার বন্ধ রাখতে হবে যাতে আর্সেনিক দূষণ ও ফ্লুওরাইড দূষণের মাত্রা হ্রাস পায়।
- খালবিল যাতে কচুরিপানায় ভরে না যায় সেদিকে নজর দিতে হবে। জলে শ্যাওলা ও আগাছার সংখ্যা বেশি হলে জলে দ্রবীভূত অক্সিজেনের মাত্রা কমতে থাকে যা জলজ প্রাণীদের পক্ষে ক্ষতিকর।
- জৈববিশ্লেষ্য ডিটারজেন্ট ব্যবহার করতে হবে।
- সর্বোপরি, সাধারণ মানুষকে জলদূষণের ক্ষতিকারক প্রভাব ও প্রতিকার সম্পর্কে সচেতন করতে হবে এবং জলদূষণ নিয়ন্ত্রণ করার ক্ষেত্রে আইনগুলি কঠোরভাবে প্রয়োগ করতে হবে।
ভারত সরকার শিল্পজাত ও গৃহস্থালির অপদ্রব্য নদীর জলে মিশ্রণকে আইনত নিষিদ্ধ করেছেন এবং নদীর জল বিশুদ্ধ করার জন্য বিভিন্ন যোজনা গ্রহণ করেছেন। এই ধরনের যোজনাগুলির মধ্যে উল্লেখযোগ্য কী কী? উদাহরণস্বরূপ কোন কোন প্রকল্পের নাম লেখো।
ভারত সরকার শিল্পজাত, গৃহস্থালির অপদ্রব্য নদীর জলে সংমিশ্রণ হওয়াকে আইন দ্বারা নিষিদ্ধ করেছেন এবং নদীর জল বিশুদ্ধ করার জন্য নিম্নলিখিত যোজনা গ্রহণ করেছেন –
Ganga Action Plan, Yamuna Action Plan,
Plan to clean Hooghly-Water
পানীয় জলে আর্সেনিকের স্বাভাবিক মাত্রা কত? ভূগর্ভস্থ জলে আর্সেনিক কীরূপে থাকে?
পানীয় জলে আর্সেনিকের WHO দ্বারা নির্ধারিত সর্বোচ্চ মাত্রা 0.05 মিলিগ্রাম/লিটার।
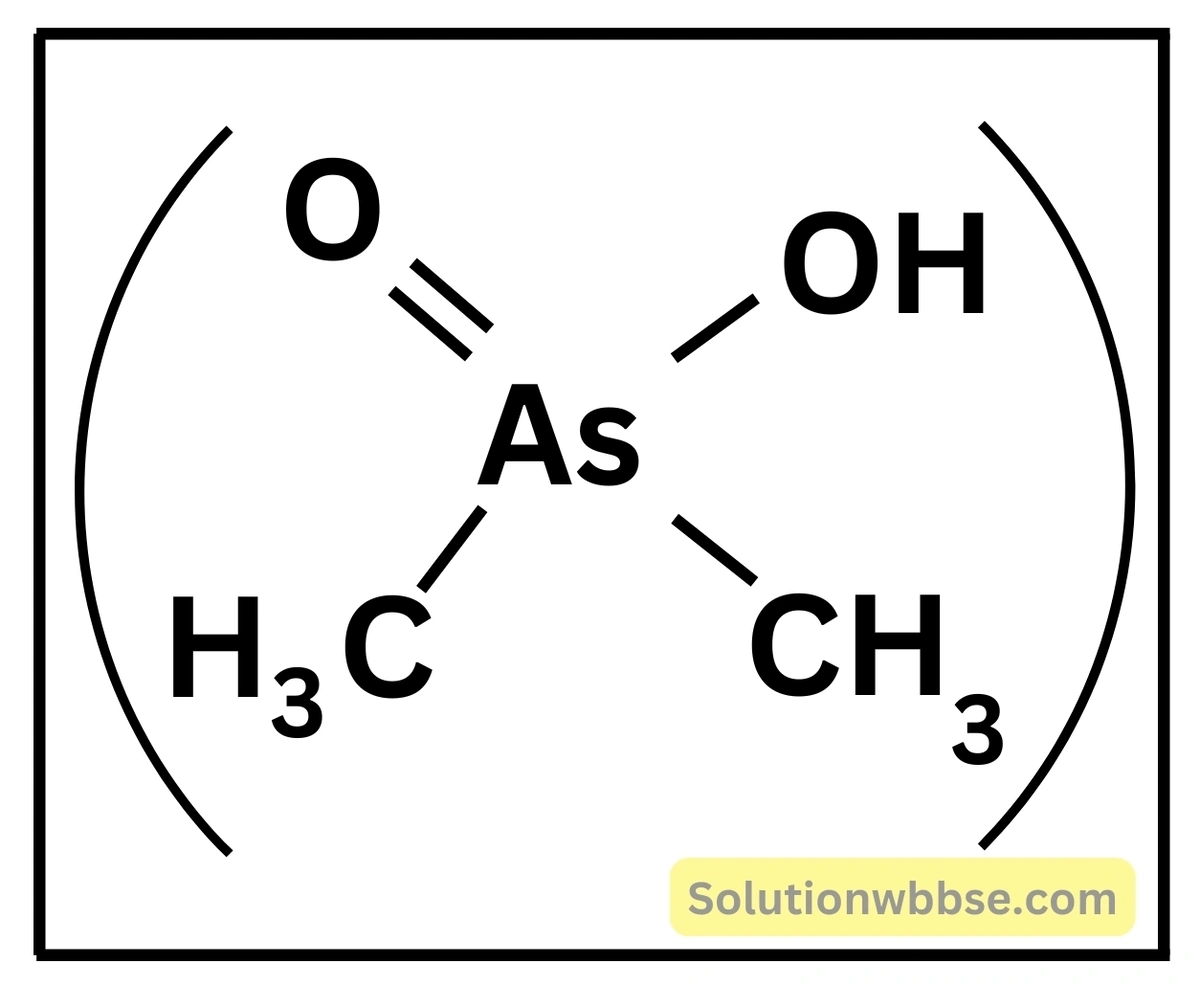
ভূগর্ভস্থ জলে আর্সেনিক অজৈব ও জৈব পদার্থ হিসেবে থাকে। অজৈব পদার্থ হিসেবে এটি আর্সেনাইট (As3+) ও আর্সেনেট (As5+) যৌগ রূপে থাকে। জৈব পদার্থ হিসেবে এটি ক্যাকোডাইলিক অ্যাসিড রূপে থাকে।
আর্সেনিক দূষণ বলতে কী বোঝায়?
আর্সেনিক দূষণ (Arsenic Pollution) – কৃষিক্ষেত্রে আগাছানাশক ও কীটনাশক হিসেবে ব্যবহৃত আর্সেনিক বৃষ্টির জলে ধুয়ে ভূগর্ভস্থ জলকে দূষিত করে। পানীয় জলে আর্সেনিকের এই পরিমাণ স্বাভাবিক মাত্রাকে অতিক্রম করলে সেই জল পানের অযোগ্য হয়ে পড়ে, এই ঘটনাকে আর্সেনিক দূষণ বলা হয়।
আর্সেনিক দূষণের কারণ লেখো।
আর্সেনিক দূষণের কারণ –
- চাষের জন্য যথেচ্ছ পরিমাণে জল তুলে নেওয়ায় ভূগর্ভস্থ জলের পরিমাণ হ্রাস পাচ্ছে। ফলে, আর্সেনিক দূষণ হয়।
- কৃষিক্ষেত্রে আর্সেনিকযুক্ত কীটনাশক ও আগাছানাশক ব্যবহার করলে এগুলি বৃষ্টির জলে ধুয়ে ভূগর্ভস্থ জলকে দূষিত করে।
- ভূগর্ভস্থ জল আর্সেনিকযুক্ত শিলার সংস্পর্শে এলে সব থেকে বেশি জলে আর্সেনিক সংক্রমণ হয়।
- আর্সেনিকযুক্ত আকরিক, যেমন – আর্সেনোপাইরাইট, ওরপিমেন্টের সংস্পর্শে ভূগর্ভস্থ জল এলে আর্সেনিক দূষণ ঘটে।
আর্সেনিক দূষণের কুফলগুলি লেখো।
আর্সেনিক দূষণের ক্ষতিকারক প্রভাব বা কুফল –
মানবদেহে আর্সেনিকের অত্যন্ত ক্ষতিকারক প্রভাব দেখা যায়।
ত্বকের ওপর প্রভাব –
- দীর্ঘদিন আর্সেনিকযুক্ত জল গ্রহণ করলে মানুষের চামড়া খসখসে হয়ে যায়। স্পর্শ-বেদনা ও তাপের অনুভূতি কমে যায়।
- হাত ও পায়ের তলদেশে কালো কালো ছোপ পড়ে যায়। পরে সেখানে ক্ষতের সৃষ্টি হয়। একে ব্ল্যাকফুট রোগ (Black foot disease) বলে।
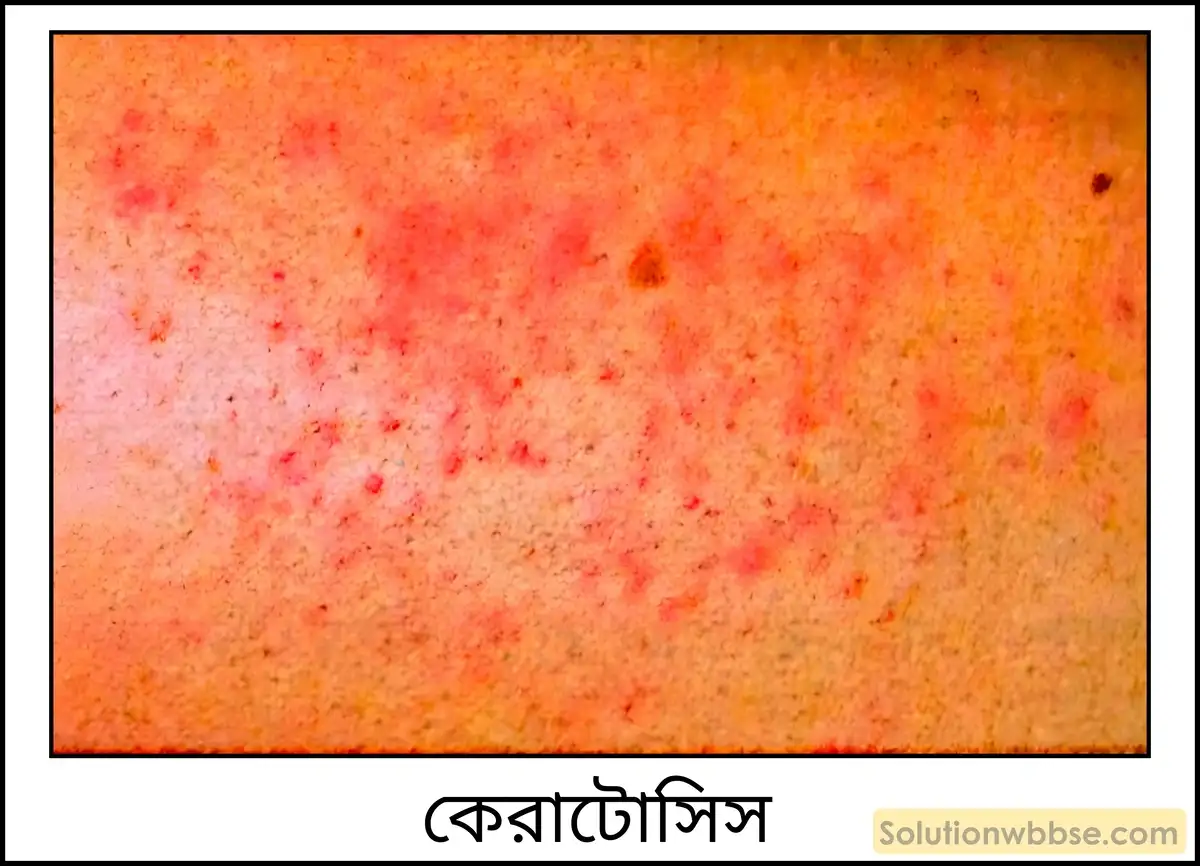
- দীর্ঘদিন আর্সেনিকযুক্ত জল পান করলে হাতের ও পায়ের তালু কঠিন হয়ে যায় এবং এতে অসংখ্য শুষ্ক, অমসৃণ স্ফীতি দেখা যায়। আর্সেনিক বিষক্রিয়ার এই অবস্থাকে বলা হয় কেরাটোসিস।
- দীর্ঘদিন আর্সেনিকযুক্ত জল পান করলে হাত ও পায়ের নখে অসংখ্য অনুভূমিক সাদা খাঁজের সৃষ্টি হয়। এই সাদা খাঁজগুলিকে বলা হয় ‘Mees line’ বা ‘মিইজ রেখা’।
- পানীয় জলে আর্সেনিকের পরিমাণ স্বাভাবিক মাত্রা অতিক্রম করলে অর্থাৎ, প্রতি লিটারে 0.05 মিলিগ্রামের বেশি হলে সেই জল পান করলে মানুষের আর্সেনিকোসিস রোগ হয়। এই রোগে গায়ে ফুসকুড়ি, ফুসফুস ও যকৃতের প্রদাহ, চুলকানি ইত্যাদি উপসর্গ পরিলক্ষিত হয়।
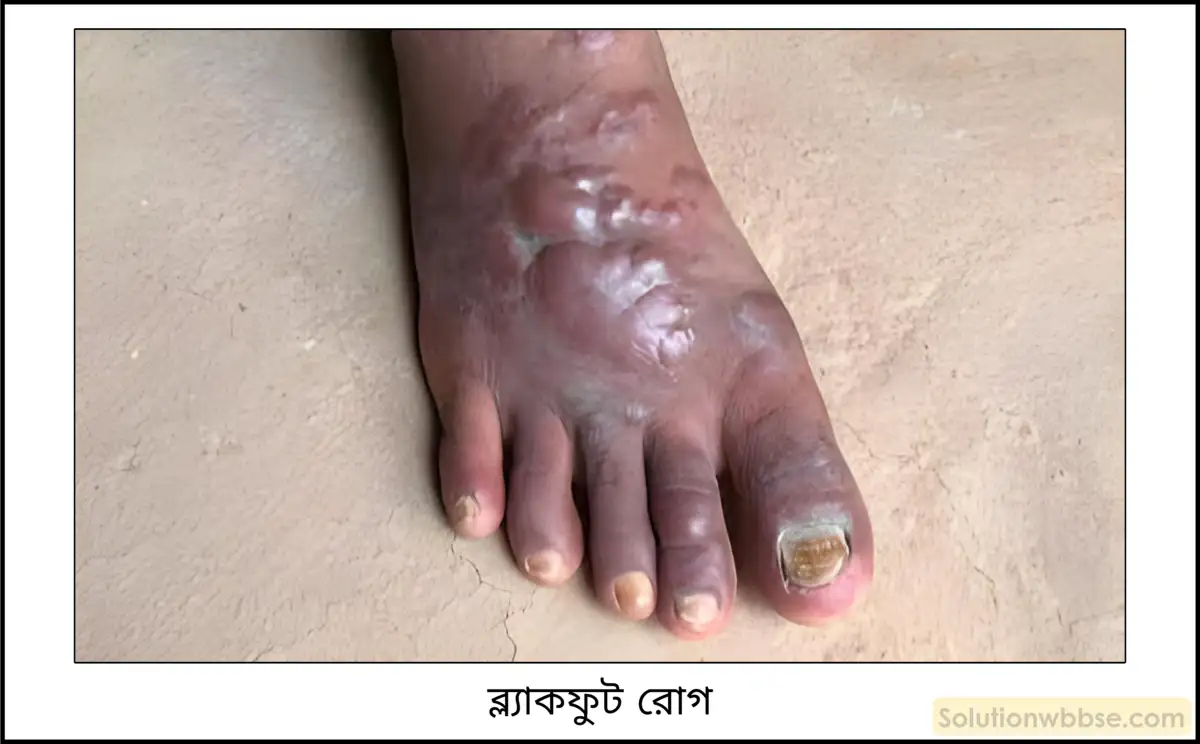
পাকস্থলী, ফুসফুস ও অস্ত্রে প্রভাব –
- পাকস্থলীতে প্রদাহের সৃষ্টি হয়।
- বমি বমি ভাব, পেট ব্যথা, মুখ ও জিহ্বা শুকিয়ে যাওয়া ইত্যাদি দেখা দেয়।
- ডায়ারিয়ার প্রকোপ দেখা দেয়।
- লিভারে সিরোসিস, ফুসফুস ও মূত্রনালীতে ক্যানসার হতে পারে।
- গ্যাসট্রাইটিস, কোলাইটিস ইত্যাদি রোগ দেখা দেয়।
- ফুসফুসে প্রদাহ, ব্রঙ্কাইটিস, অ্যাজমা ইত্যাদি হতে পারে। এছাড়াও রক্তাল্পতা, শারীরিক অবসাদ, দুর্বলতা, হাত-পা ঝিনঝিন করা, পেশিতে টান ধরা ইত্যাদি দেখা দেয়।
উদ্ভিদের ওপর প্রভাব – উদ্ভিদের স্বাভাবিক বৃদ্ধি ব্যাহত হয় এবং উদ্ভিদ কোশ ক্ষতিগ্রস্ত হয়।
মানচিত্রের দ্বারা পশ্চিমবঙ্গের আর্সেনিকপ্রবণ এলাকাগুলি দেখাও।
পশ্চিমবঙ্গের আর্সেনিকপ্রবণ এলাকার মানচিত্র –
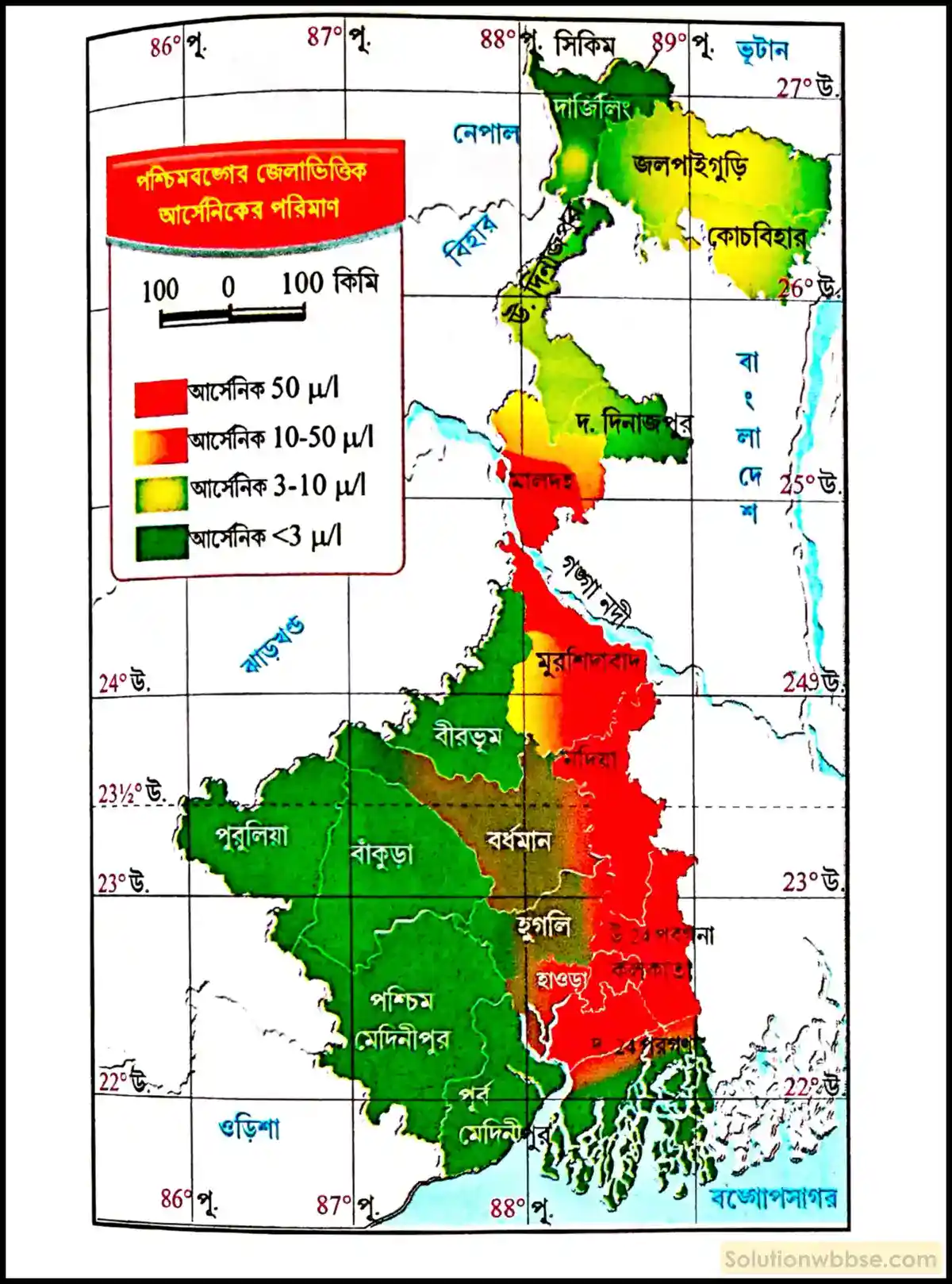
পানীয় জল থেকে আর্সেনিক দূর করার উপায়গুলি লেখো।
নিম্নলিখিত কয়েকটি উপায়ে আর্সেনিকমুক্ত জল পাওয়া যায় –
সহ-অধঃক্ষেপণ (Co-precipitation) – আর্সেনিক লবণ-মিশ্রিত জলে পরিমাণমতো ব্লিচিং পাউডার যোগ করে কয়েক ঘণ্টা রেখে দেওয়ার পর ফিলটার করলে যে পরিস্রুত পাওয়া যায় তাতে ফটকিরি বা ফেরিক লবণ (Fe3+) মিশিয়ে কিছুক্ষণ স্থিরভাবে রেখে দিলে আর্সেনিকঘটিত অধঃক্ষেপ থিতিয়ে পড়ে। এইভাবে উপরের স্বচ্ছ জল পরিস্রাবণ করে আর্সেনিকমুক্ত (90 – 95)% জল পাওয়া যায়।
ভূগর্ভস্থ জল যদি বায়ুর সংস্পর্শে না আসে তাহলে অধিকাংশ আর্সেনিক ত্রিযোজী বা আর্সেনাইটরূপে দ্রবীভূত থাকে। প্রথমে কোনো উপযুক্ত জারকের সাহায্যে আর্সেনাইটকে (AS-III) জারিত করে আর্সেনেটে (As-V) পরিণত করে। এক্ষেত্রে জারক হিসেবে পটাশিয়াম পারম্যাঙ্গানেট বা ব্লিচিং পাউডার ব্যবহৃত হয়।
অধিশোষণ (Adsorption) – পানীয় জলকে আর্সেনিকমুক্ত করার একটি অত্যাধুনিক পদ্ধতি হল অধিশোষণ প্রক্রিয়া। আর্সেনিক দূষিত জলকে Fe(OH)3 -এর আস্তরণযুক্ত অ্যালুমিনা (Al2O3) [সক্রিয় অ্যালুমিনা] ও টাইটানিয়াম ডাইঅক্সাইডের (TiO2) সচ্ছিদ্র মিশ্রণের মধ্যে দিয়ে চালনা করলে জলে উপস্থিত আর্সেনেট ও আর্সেনাইট – এই দুই প্রকার লবণই সক্রিয় অ্যালুমিনা দ্বারা অধিশোষিত হয়। ফলে, আর্সেনিক মুক্ত জল পাওয়া যায়। এই প্রক্রিয়ায় বিশুদ্ধ পানীয় জল উৎপাদনের প্রক্রিয়াটি রেখাচিত্রের মাধ্যমে দেখানো হল –
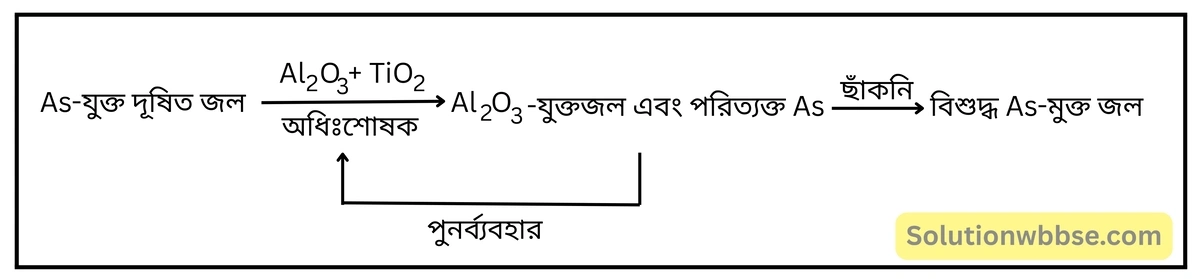
আর্সেনিক মুক্ত ভৌমজল আহরণ করার জন্য টিউবওয়েলের নলের সঙ্গে ‘অ্যালুমিনা স্তম্ভ’ সংযুক্ত করা হয়।
অতিবেগুনি রশ্মির সাহায্যে – UV রশ্মির সাহায্যে জলকে আর্সেনিক মুক্ত করা যায়। এই পদ্ধতিতে আর্সেনাইট \(AsO_3^{3-}\) লবণযুক্ত জলকে UV রশ্মির সাহায্যে অক্সিজেন (O2) দ্বারা জারিত করলে, আর্সেনাইট লবণ আর্সেনেট লবণে \(AsO_4^{3-}\) পরিণত হয়। এরপর এই জলের মধ্যে ফেরিক হাইড্রক্সাইডের আস্তরণযুক্ত অ্যালুমিনিয়াম অক্সাইড ও টাইটেনিয়াম অক্সাইড যোগ করা হলে জল মধ্যস্থ আর্সেনিক, ফেরিক আর্সেনেট (FeAsO4) যৌগরূপে অধঃক্ষিপ্ত হয়। এই অধঃক্ষেপকে ফিলটার করে আর্সেনিকমুক্ত বিশুদ্ধ জল পাওয়া যায়।
বিপরীত অভিস্রবণ (Reverse Osmosis) – এই পদ্ধতিতে জলে সবরকম দ্রবীভূত লবণ সম্পূর্ণভাবে পৃথক করা হয়। এই পদ্ধতিতে সেলুলোজ ট্রাইঅ্যাসিটেটকে অর্ধভেদ্য পর্দা হিসেবে ব্যবহার করা হয়। এই পর্দার বিশেষ গুণ হল, চাপের প্রভাবে শুধু জলের অণুকে পর্দার মধ্যে যেতে দেয়, অন্যান্য দ্রবীভূত লবণকে আটকে দেয়।
আর্সেনিক দূষণ কীভাবে নিয়ন্ত্রণ করা যায়?
আর্সেনিক দূষণ নিয়ন্ত্রণ –
- ভূগর্ভস্থ জলের যথেচ্ছ উত্তোলন বন্ধ করতে হবে।
- চাষের জমিতে কীটনাশক হিসেবে আর্সেনিকযুক্ত রাসায়নিক ব্যবহার বন্ধ করতে হবে।
- নলকূপের জল মাঝে মাঝে পরীক্ষা করতে হবে। যে-সমস্ত এলাকার নলকূপের জলে আর্সেনিক পাওয়া গেছে সেগুলিকে সিল করে দিতে হবে।
- ধাতু নিষ্কাশনের কারখানা থেকে প্রাপ্ত আর্সেনিকযুক্ত বর্জ্য পদার্থ বৈজ্ঞানিক উপায়ে স্তূপীকৃত করতে হবে যাতে আর্সেনিকঘটিত দূষণ না হয়।
- পুকুর, নদী বা কূপের জলকে কমপক্ষে 20 মিনিট ফুটিয়ে পান করতে হবে।
- সহ-অধঃক্ষেপণ, অধিশোষণ, আয়ন বিনিময় প্রভৃতি পদ্ধতিতে আর্সেনিকযুক্ত জল থেকে আর্সেনিক অপসারণের ব্যবস্থা করতে হবে।
- বৃষ্টির জল আর্সেনিকমুক্ত, তাই বৃষ্টির জলকে বড়ো বড়ো জলাধারে ধরে রেখে তা শোধন করে পানীয় জল হিসেবে ব্যবহার করতে হবে।
- সম্প্রতি (2004) আর্সেনিক টাস্ক ফোর্স ভূগর্ভে থাকা আর্সেনিক স্তরগুলিতে সরাসরি সালফারঘটিত পলিমার মিশিয়ে ক্ষতিকারক দ্রাব্য আর্সেনেট যৌগকে অদ্রাব্য আর্সেনেটে পরিণত করে যা মাটিতে মিশে যায়। ফলে জল আর্সেনিকমুক্ত হয়।
পানীয় জলে ফ্লুওরাইডের স্বাভাবিক মাত্রা কত? ভূগর্ভস্থ জলে ফুওরাইড কীরূপে থাকে?
WHO (World Health Organisation) -এর মতে পানীয় জলে ফ্লুওরাইডের সহনমাত্রা সর্বাধিক 0.8 মিলিগ্রাম/লিটার।
ফ্লুওরাইড পানীয় জলে অক্সিজেন ও নাইট্রোজেন ব্যতীত অন্য সকল অধাতব ও ধাতব মৌলের সঙ্গে যুক্ত হয়ে যৌগ গঠন করে থাকে।
ফ্লুওরাইড দূষণ বলতে কী বোঝায়?
ফ্লুওরাইড দূষণ (Fluoride Pollution) – পানীয় জলে ফ্লুওরাইড যৌগের সংক্রমণে মানুষ এবং অন্যান্য জীবের ও পরিবেশের যে ক্ষতিসাধন ঘটে, তাকে ফ্লুওরাইড দূষণ বলে।
জলে ফ্লুওরাইড দূষণের কারণ লেখো।
ফ্লুওরাইড দূষণের কারণগুলি হল –
- ভূগর্ভে উপস্থিত ফ্লুওরাইড যৌগই পানীয় জলে ফ্লুওরাইড দূষণের মূল উৎস।
- কৃষিজমিতে ব্যবহৃত কীটনাশক, প্লাস্টিক এবং সার কারখানায় ব্যবহৃত ফ্লুওরাইড যৌগ মাটি ও জলের মাধ্যমে ভূগর্ভস্থ জলে মিশে জলদূষণ ঘটায়।
ফ্লুওরাইড দূষণের ক্ষতিকর প্রভাবগুলি লেখো।
ফ্লুওরাইড দূষণের ক্ষতিকর প্রভাবগুলি নিম্নরূপ –
- পানীয় জলে ফ্লুওরাইডের মাত্রা স্বাভাবিক মান অতিক্রম করলে আমাদের দাঁত ও হাড়ের ক্ষতি হয়। ফলে, তা ভঙ্গুর হয়ে পড়ে।
- ফ্লুওরাইড দূষণের ফলে নক্-নী সিনড্রোম রোগ দেখা যায়। এই রোগের ফলে অস্থি স্বাভাবিকের তুলনায় দৃঢ় হয় ও অস্থি সন্ধিগুলির ক্ষতি হয় এবং হাঁটুর নীচ থেকে পা বাইরের দিকে বেঁকে যায়।
- এই দূষণের ফলে পেশি ও স্নায়ুর স্বাভাবিক কার্যকারিতা হ্রাস পায়।
- ফ্লুওরাইড দূষণের ফলে অস্টিওফ্লুওরোসিস, ডেন্টালফ্লুওরোসিস প্রভৃতি রোগ হয়।
- এর ফলে মানুষের শ্লেষ্মাঝিল্লি ক্ষতিগ্রস্ত হয়।
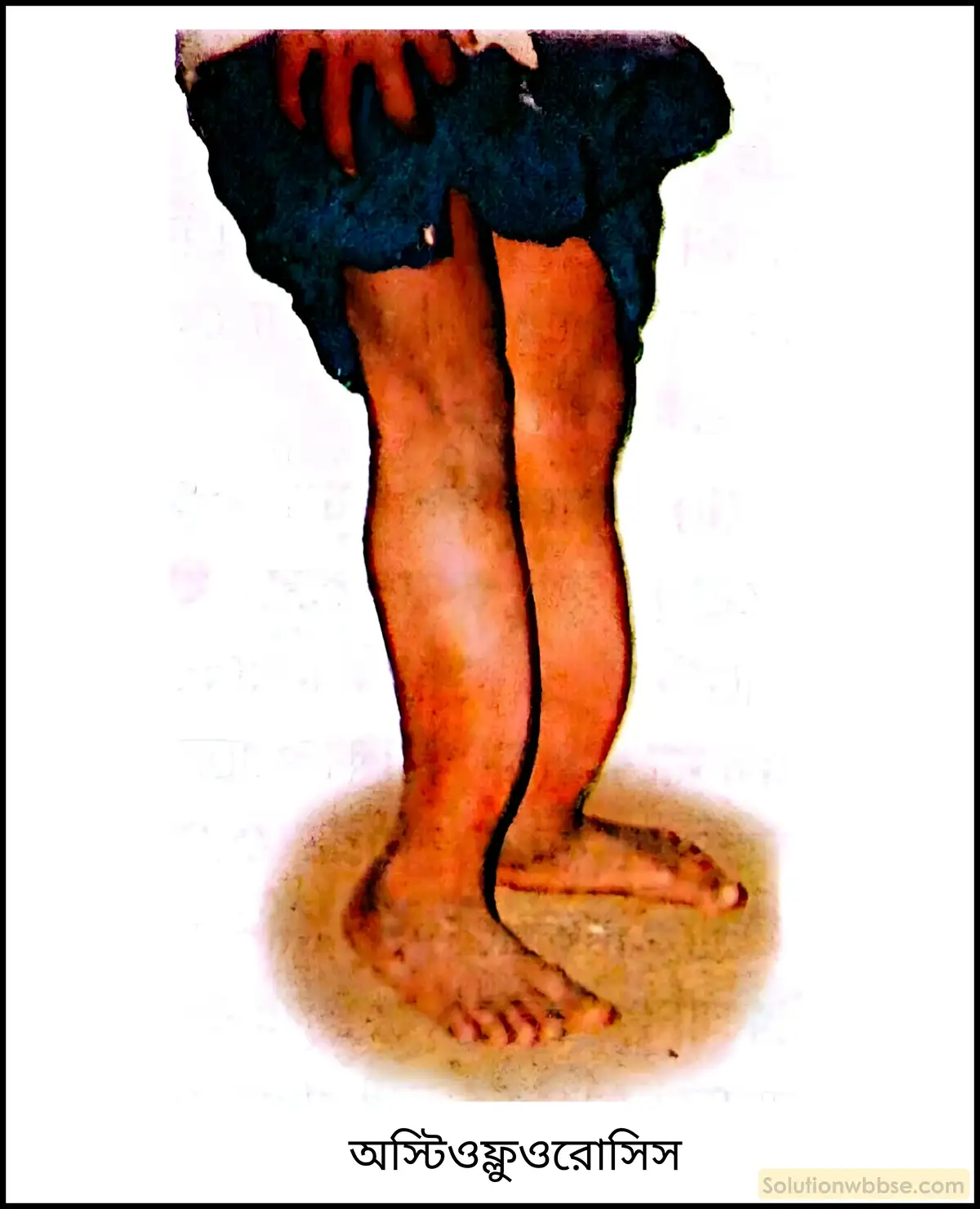
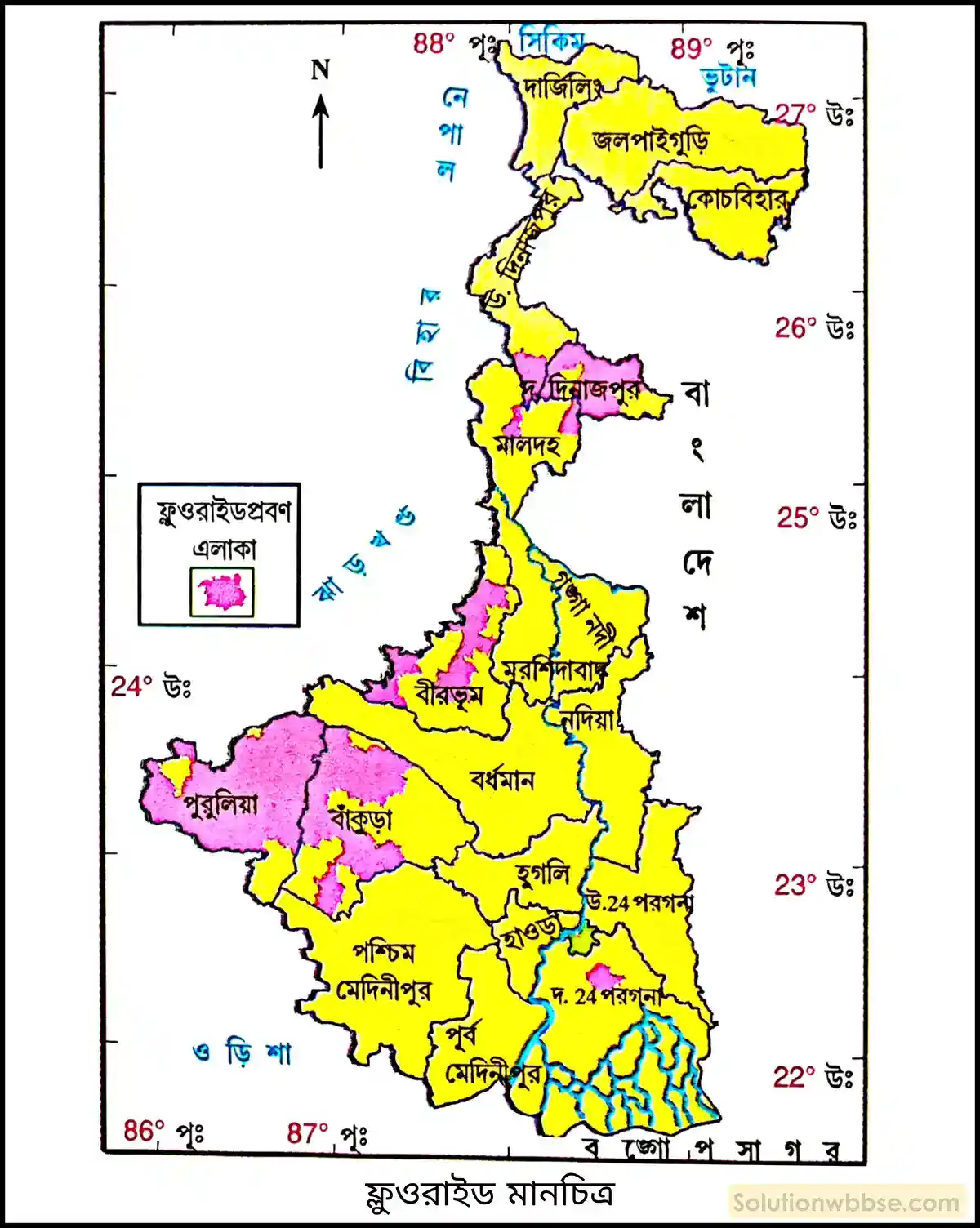
মানচিত্রের মাধ্যমে পশ্চিমবঙ্গের ফ্লুওরাইডপ্রবণ এলাকাগুলি চিহ্নিত করো।
ফ্লুওরাইড আক্রান্ত এলাকার মানচিত্র –
পানীয় জল থেকে ফ্লুওরাইড যৌগ অপসারণের উপায় লেখো।
সক্রিয় চারকোল পদ্ধতি (Activated Charcole Treatment) – কাঠের গুঁড়ো বা নারকেলের খোলাকে আবদ্ধ পাত্রের মধ্যে ZnCl2 যুক্ত করে অন্তর্ধূম পাতন করলে কার্বন চূর্ণ বা চারকোল পাওয়া যায়। এই চারকোলকে ক্ষার (গাঢ় NaOH) দ্বারা জারিত করা হয়। এরপর এর মধ্যে ফটকিরির দ্রবণ যোগ করলে বিশেষ অধিশোষণ ক্ষমতাযুক্ত সক্রিয় চারকোল (Activated Carbon) উৎপন্ন হয়। এরকম সক্রিয় চারকোলের মধ্যে দিয়ে ফ্লুওরাইড দূষিত জল চালনা করলে ওই জল থেকে ফ্লুওরাইড দূরীভূত হয়।
আবার, পানীয় জলে ফ্লুওরাইড মিশে থাকলে তাতে পরিমাণ মতো ফটকিরি এবং চুন মিশিয়ে রাখা হয়। এরপর মিশ্রণটিকে কিছুক্ষণ রেখে দিলে, ফ্লুওরাইডযুক্ত যৌগ পাত্রের তলদেশে থিতিয়ে পড়ে। এরপর উপর থেকে স্বচ্ছ ও পরিষ্কার জল আলাদা করে নিলে কিছুটা বিশুদ্ধ ফ্লুওরাইডমুক্ত পানীয় জল পাওয়া যায়। এছাড়াও পানীয় জলকে ফোটালে ফ্লুওরাইডমুক্ত জল পাওয়া যায়।
জল সংকট বলতে কী বোঝায়?
বর্তমান সভ্যতায় জল একটি অপরিহার্য বস্তু। জল ছাড়া এই সভ্যতার কোনো জীবের অস্তিত্ব সম্ভব নয়। ভূগর্ভস্থ জল আহরণের মাধ্যমে আমরা প্রধানত জলের চাহিদা মেটাই। ভূগর্ভস্থ জলের পরিমাণ সীমিত। বর্তমান সভ্যতার অগ্রগতিতে জনসংখ্যা বৃদ্ধির সঙ্গে সঙ্গে কৃষিকার্যে, গৃহস্থালির কাজে, বিভিন্ন শিল্প প্রতিষ্ঠানগুলিতে জলের অনিয়মিত ও যথেচ্ছভাবে ব্যবহারের জন্য গভীর নলকূপের সাহায্যে নির্বিচারে জল উত্তোলন করা হচ্ছে।
বড়ো বড়ো ইমারত গঠনের জন্য বহুল পরিমাণে বৃক্ষচ্ছেদনের ফলে মাটির জলধারণ ক্ষমতা হ্রাস পাচ্ছে। ফলে, ভূগর্ভস্থ জলস্তর অনেক নীচে নেমে যাওয়ায় আর্সেনিক ও ফ্লুওরাইডঘটিত দূষণের কবলিত হয়ে বিস্তীর্ণ অঞ্চলের জল পানের অযোগ্য হয়ে গেছে। ফলে, এক তীব্র জলের সমস্যা দেখা দিয়েছে। একেই জল সংকট বলা হয়।
জল সংকট মোকাবিলায় বৃষ্টির জল কীভাবে ব্যবহৃত হয়?
যেসব অঞ্চলে জলের উৎসের অভাব আছে, সেখানে বৃষ্টির জল সংরক্ষণ করে পানীয় হিসেবে এবং গৃহস্থালির অন্যান্য কাজে ব্যবহার করা যেতে পারে। বর্তমানে বিভিন্ন মহানগরে ভৌমজল অতিরিক্ত উত্তোলনের ফলে জলের স্তর ক্রমশ নীচে নেমে যাচ্ছে এবং আর্সেনিক যৌগ দ্বারা দূষিত হচ্ছে। তাই নিম্নলিখিত উপায়ে বৃষ্টির জল সংরক্ষণ করে ব্যবহার করতে পারলে জল সমস্যার একটি সমাধান খুঁজে পাওয়া যাবে –
- বড়ো বড়ো জলাধারে বৃষ্টির জল ধরে রেখে কৃষিকার্যে ব্যবহার করা যেতে পারে।
- বাড়ির ছাদে বৃষ্টির জল সংরক্ষণ করে তা গৃহস্থালির কাজে লাগানো যেতে পারে বা ওই জলকে পাইপের সাহায্যে ভূগর্ভের জলাধারে জমা করা যেতে পারে যাতে ওই জল চুঁইয়ে মাটির নীচে চলে গিয়ে ভূগর্ভস্থ জলভাণ্ডার বৃদ্ধি পায়।
বোধমূলক প্রশ্নোত্তর
একটি বর্ণহীন তরল যে জল তা বুঝবে কীভাবে?
অথবা, জলকে কীভাবে শনাক্ত করবে?
বর্ণহীন তরলটিকে শনাক্ত করার জন্য সেটিকে অনার্দ্র কপার সালফেটের সংস্পর্শে আনতে হবে। যদি অনার্দ্র বর্ণহীন কপার সালফেট নীল বর্ণ ধারণ করে, তবে বুঝতে হবে বর্ণহীন তরলটি জল। কারণ – অনার্দ্র বর্ণহীন কপার সালফেট জলের সংস্পর্শে এসে নীল বর্ণের সোদক কপার সালফেটে পরিণত হয়।
সেঁক দেবার কাজে জল ব্যবহার করা হয় কেন?
জলের আপেক্ষিক তাপ (1 Cal⋅g-1/°C) অন্যান্য তরলের তুলনায় বেশি হবার কারণে এটি বহুক্ষণ ধরে তাপ ধরে রাখতে পারে। এই কারণে জল ফোটালে তা থেকে খুব ধীরে ধীরে তাপ ক্ষয় হয়। তাই সেঁক দেবার বোতলে জল ব্যবহার করলে সেক দিতে সুবিধা হয়।
জল একটি উত্তম আয়ন সৃষ্টিকারী দ্রাবক – ব্যাখ্যা করো।
জল একটি সমযোজী যৌগ। জলের পরাবৈদ্যুতিক ধ্রুবক বেশি হবার ফলে বহু তড়িদবিশ্লেষ্য যৌগ জলে দ্রবীভূত হতে পারে। জলীয় দ্রবণে ক্যাটায়ন ও অ্যানায়নের মাঝে জল একটি অন্তরক স্তর গঠন করে। ফলে, আয়নগুলি পরস্পর যুক্ত হয়ে অণু গঠন করতে পারে না, আয়ন হিসেবে থাকে। এই কারণে বলা হয় “জল একটি উত্তম আয়ন সৃষ্টিকারী দ্রাবক”।
জলকে জীবন বলা হয় কেন?
মানবজীবনে জলের ভূমিকা অনস্বীকার্য। সমগ্র জীবকুলের বেঁচে থাকার জন্য জল প্রয়োজন। মানবদেহের বিভিন্ন শারীরবৃত্তীয় কার্যকলাপের জন্য জল প্রয়োজন। মানবজীবনের নানা দৈনন্দিন কাজে, যেমন রান্না করা, স্নান করা, জামাকাপড় কাচা, বাসন মাজা ইত্যাদিতে জল একান্ত প্রয়োজন। শিল্পকারখানা, তাপবিদ্যুৎ কেন্দ্র, পরিবহণ, চিকিৎসাক্ষেত্র সমস্ত গুরুত্বপূর্ণ ক্ষেত্র জল ছাড়া চলতে পারে না। এই সকল কারণে জলকে জীবন বলা হয়।
গরমকালে পুকুরের মাছ মরে যায় কেন?
গরমকালে সূর্যের প্রখর তাপে পুকুরের জল গরম হয়ে ওঠে। ফলে, জলে দ্রবীভূত অক্সিজেনের পরিমাণ হ্রাস পায় (কারণ – জলে গ্যাসের দ্রাব্যতা উষ্ণতা বৃদ্ধিতে হ্রাস প্রাপ্ত হয়)। পুকুরের মাছেরা তাদের শ্বাসকার্যের জন্য প্রয়োজনীয় অক্সিজেনের অভাবে মারা যায়।
উত্তপ্ত জল স্বাদহীন হয় কেন?
জলের স্বাদের জন্য দায়ী জলে দ্রবীভূত কার্বন ডাইঅক্সাইড ও অক্সিজেন গ্যাস। জলকে ফোটালে এতে দ্রবীভূত কার্বন ডাইঅক্সাইড ও অক্সিজেন গ্যাস নির্গত হয়ে যায়। তাই জল বিস্বাদ লাগে।
পানীয় জলে ক্লোরাইডের পরিমাণ নির্ধারিত মাত্রার চেয়ে বেশি থাকলে কী হবে?
পানীয় জলে ক্লোরাইড দ্রাব্য লবণরূপে উপস্থিত থাকে। ক্লোরাইডের দ্রাব্য লবণে উপস্থিত ক্যাটায়নের গাঢ়ত্বের ওপর জলের দূষণ মাত্রা নির্ভর করে। পানীয় জলে ক্লোরাইডের দ্রাব্য লবণ সোডিয়াম ক্লোরাইড (NaCl) নির্ধারিত মাত্রার চেয়ে বেশি পরিমাণে উপস্থিত থাকলে এবং দীর্ঘদিন ধরে ওই জল পান করলে জলের সঙ্গে বেশি পরিমাণ সোডিয়াম ক্লোরাইড শরীরে প্রবেশ করে। ফলে, রক্তচাপ স্বাভাবিকের চেয়ে বেশি হয় এবং উচ্চ রক্তচাপজনিত সমস্যা, যেমন – হৃৎস্পন্দন বৃদ্ধি, মস্তিষ্কে রক্তক্ষরণ প্রভৃতি দেখা দিতে পারে।
টিউবওয়েলের জল খর না মৃদু? এই জলে আর্সেনিক না থাকলে এই জল স্বাস্থ্যকর – একথা বলা হয় কেন?
টিউবওয়েলের জল খর। টিউবওয়েলের মাধ্যমে যে ভূগর্ভস্থ জল উত্তোলন করা হয় তাতে অধিক পরিমাণ খনিজ লবণ মিশে থাকে। এই জলে আর্সেনিক বা অন্য কোনো বিষাক্ত পদার্থ মিশে না থাকলে এই জল স্বাস্থ্যকর, কারণ – টিউবওয়েলের জল মানবদেহের অতি প্রয়োজনীয় বিভিন্ন ধাতু, যেমন – সোডিয়াম, পটাশিয়াম, ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রন প্রভৃতির চাহিদা মেটায় এবং মানুষের শরীর গঠন ও উপযুক্তভাবে তার বৃদ্ধিতে সাহায্য করে।
ঝরনার জল ও বৃষ্টির জলের মধ্যে কোনটির জল খর হওয়ার সম্ভাবনা বেশি এবং কেন?
বৃষ্টির জলের তুলনায় ঝরনার জলের খর হওয়ার সম্ভাবনা বেশি। বৃষ্টির জলে দ্রবীভূত কার্বন ডাইঅক্সাইড (CO2), অক্সিজেন (O2) প্রভৃতি গ্যাস ছাড়া অন্য কোনো ধাতুর আয়ন বা লবণ থাকে না। তাই বৃষ্টির জল খর হয় না। অপরপক্ষে ঝরনা সৃষ্টি হয় পাহাড়ি অঞ্চলের খরস্রোতা নদী থেকে, যার মধ্যে খনিজ সমৃদ্ধ শিলাগুলি ক্ষয়ে জলের সঙ্গে মিশে থাকে। ঝরনার জলে বিভিন্ন ধাতু, যেমন – ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রনের বিভিন্ন লবণ দ্রবীভূত থাকতে পারে। ফলে, ঝরনার জল খর হওয়ার সম্ভাবনা বেশি।
বৃষ্টির জল মৃদু জল কিন্তু পাহাড় পর্বতের উপর দিয়ে নীচে নেমে আসার পর তা খর জলে পরিণত হয় – ব্যাখ্যা করো।
বৃষ্টির জল মৃদু জল। বাতাসের CO2 বৃষ্টির জলে দ্রবীভূত হয়ে কার্বনিক অ্যাসিড (H2CO3) উৎপন্ন করে। পাহাড় পর্বতের পাথর অধিকাংশই ক্যালশিয়াম কার্বনেট (CaCO3) এবং ম্যাগনেশিয়াম কার্বনেট (MgCO3) দ্বারা গঠিত। CO2 মিশ্রিত বৃষ্টির জল পাথরের গায়ে পড়লে অদ্রাব্য CaCO3 বা MgCO3, দ্রাব্য ক্যালশিয়াম বাইকার্বনেট [Ca(HCO3)2] বা ম্যাগনেশিয়াম বাইকার্বনেট [Mg(HCO3)2] লবণে পরিণত হয়ে জলে মিশে যায় এবং বৃষ্টির মৃদু জল খর জলে পরিণত হয়।
জলে Mg(HCO3)2 -এর উপস্থিতি জনিত খরতা স্ফুটনের সাহায্যে কেন সম্পূর্ণ করা যায় না?
জলে ম্যাগনেশিয়াম বাইকার্বনেট ঘটিত খরতা স্ফুটন পদ্ধতিতে সম্পূর্ণ দূর করা যায় না কারণ – ম্যাগনেশিয়াম বাইকার্বনেটঘটিত অস্থায়ী খর জলকে ফোটালে এটি বিয়োজিত হয়ে ম্যাগনেশিয়াম কার্বনেট, কার্বন ডাইঅক্সাইড ও জল উৎপন্ন হয়। ম্যাগনেশিয়াম কার্বনেট জলে সামান্য পরিমাণে দ্রাব্য হওয়ায় কিছু পরিমাণ Mg2+ আয়ন সর্বদা জলে থেকে যায়। তাই এক্ষেত্রে অস্থায়ী খরতা সম্পূর্ণ রূপে দূরীভূত হয় না।
Mg(HCO3)2 = MgCO3 + CO2 + H2O
খর জলে সাবানের পরিবর্তে ডিটারজেন্ট ব্যবহার করা সুবিধাজনক কেন?
সাবান হল স্টিয়ারিক, পামিটিক প্রভৃতি ফ্যাটি অ্যাসিডের সোডিয়াম বা পটাশিয়াম লবণ। খর জলে সাবান ব্যবহার করলে খর জলে উপস্থিত Ca2+, Mg2+, Fe3+ প্রভৃতি ক্যাটায়নগুলির সঙ্গে সাবানের বিক্রিয়া ঘটে অদ্রাব্য Ca, Mg বা Fe -এর স্টিয়ারেট বা পামিটেট লবণ উৎপন্ন হয় এবং দ্রবণ থেকে অধঃক্ষিপ্ত হয়। এইভাবে খরজল থেকে সমস্ত ক্যাটায়ন অধঃক্ষিপ্ত হওয়ার পর মৃদু জলে পরিণত হলে সাবান ঘষলে ফেনা উৎপন্ন হয়। ফলে, সাবানের অপচয় বেশি হয়।
অপরপক্ষে, ডিটারজেন্টে উপস্থিত উপাদানগুলি, যেমন – অ্যালকিল বেঞ্জিন সালফোনেট, সোডিয়াম ট্রাইপলিফসফেট ইত্যাদি খর জলের Ca2+, Mg2+ প্রভৃতি আয়নের সঙ্গে বিক্রিয়ায় জলে দ্রাব্য জটিল লবণ উৎপন্ন করে। তাই খর জলে ডিটারজেন্ট ব্যবহারে ফেনার সৃষ্টি হয়। ফলে, খর জলে ডিটারজেন্টের কার্যকারিতা বজায় থাকে এবং ডিটারজেন্টের অপচয় হয় না।
খর জলে সাবান দিয়ে জামাকাপড় কাচলে জামাকাপড়ে বাদামি বর্ণের দাগ হয় কেন?
খর জলের মধ্যে ফেরাস বাইকার্বনেট [Fe(HCO3)2] লবণ উপস্থিত থাকে, যা জলের অস্থায়ী খরতার অন্যতম কারণ। এই জলকে গরম করে জামাকাপড় কাচলে ফেরাস বাইকার্বনেট তাপে বিয়োজিত হয়ে প্রথমে অদ্রাব্য ফেরাস কার্বনেট (FeCO3) লবণ উৎপন্ন করে। পরে এই ফেরাস কার্বনেট জলের উপস্থিতিতে আর্দ্র বিশ্লেষিত হয়ে লালচে-বাদামি বর্ণের অদ্রাব্য ফেরিক হাইড্রক্সাইড [Fe(OH)3] উৎপন্ন করে, যা কাচার সময় জামাকাপড়ে বাদামি বর্ণের দাগ সৃষ্টি করে।
নলকূপের জল কিছুক্ষণ রেখে দিলে ঘোলাটে বাদামি বর্ণের দেখায় কেন?
নলকূপের জলে দ্রাব্য ফেরাস বাইকার্বনেট লবণ থাকে যা বায়ুর অক্সিজেনের উপস্থিতিতে আর্দ্র বিশ্লেষিত হয়ে ফেরাস হাইড্রক্সাইড [Fe(OH)2] উৎপন্ন করে। ফলে, জল ঘোলাটে হয়ে যায়। এর কিছুক্ষণ পর উৎপন্ন ফেরাস হাইড্রক্সাইড বায়ুর অক্সিজেন দ্বারা জারিত হয়ে বাদামি বর্ণের ফেরিক হাইড্রক্সাইডের [Fe(OH)3] অধঃক্ষেপ সৃষ্টি করে। ফলে, জল বাদামি বর্ণের দেখায়।
জলে কয়েক ফোঁটা খনিজ অ্যাসিড ব্যবহার করলে তা খর জলের মতো আচরণ করে কেন?
জলে কয়েক ফোঁটা খনিজ অ্যাসিড (যেমন – HCl, H2SO4 প্রভৃতি) যোগ করে সাবান ব্যবহার করলে ওই জল খর জলের মতো আচরণ করে কারণ সাবান হল স্টিয়ারিক বা পামিটিক প্রভৃতি ফ্যাটি অ্যাসিডের সোডিয়াম বা পটাশিয়াম লবণ। এগুলি জলে উপস্থিত খনিজ অ্যাসিডের (H+ আয়নের) সঙ্গে বিক্রিয়া করে মূলত ফ্যাটি অ্যাসিডকে অধঃক্ষিপ্ত করে। ফলে, জলে সাবান ঘষলে সহজে ফেনা উৎপন্ন হয় না এবং সাবানের অপচয় বেশি হয় অর্থাৎ, খরজলের ন্যায় আচরণ করে।
জলের দুটি নমুনাতে Ca2+ এবং Mg2+ ক্যাটায়ন আছে, কিন্তু একটি নমুনা স্থায়ী খর জল, অপরটি অস্থায়ী খর জল। এদের মধ্যে কী পার্থক্য আছে?
স্থায়ী খর জলের নমুনাটিতে Ca2+ এবং Mg2+ ক্যাটায়নের ক্লোরাইড বা সালফেট লবণ আছে, তাই ওই জল স্থায়ী খর জল। কিন্তু অপর নমুনাটিতে Ca2+ এবং Mg2+ ক্যাটায়নের বাইকার্বনেট লবণ আছে। তাই ওই নমুনাটি অস্থায়ী খর জল।
বয়লারে খর জল ব্যবহার করা যায় না কেন?
বয়লারে খর জল ব্যবহার করা হয় না কারণ –
- বয়লারে খর জল ব্যবহার করলে বয়লারের ভিতরে তাপের কুপরিবাহী কঠিন CaCO3 বা CaSO4 -এর একটি আস্তরণ পড়ে। একে বয়লারের আঁশ (Boiler Scale) বলে। এজন্য জল ফুটিয়ে বাষ্প তৈরি করতে প্রচুর জ্বালানির অপচয় হয়। ফলে, জ্বালানির খরচও বেড়ে যায়। অত্যধিক তাপ প্রয়োগে বয়লারের স্থায়িত্ব নষ্ট হয়।
- বয়লারের মধ্যে এই আস্তরণ তাপ প্রয়োগে ফেটে যায়, বয়লারের সর্বত্র সমানভাবে উত্তপ্ত হয় না, অসম প্রসারণের ফলে বয়লার ফেটে যেতে পারে।
- খর জলের মধ্যে উপস্থিত ক্লোরাইড বা সালফেট লবণ আর্দ্রবিশ্লেষিত হয়ে HCl বা H2SO4 উৎপন্ন করে, যা বয়লারের গাত্রকে ক্ষয়প্রাপ্ত করে।
- খর জলে দ্রবীভূত পদার্থ বয়লারে জল ফোটার সময় প্রচুর ফেনা উৎপন্ন করে। এই সমস্ত কারণের জন্য খর জলকে বয়লারে ব্যবহারের পূর্বে মৃদু করে নেওয়া হয়।
রেজিন পদ্ধতিকে ‘আয়ন বিনিময় পদ্ধতি’ বলা হয় কেন?
রেজিন পদ্ধতিতে জলের মধ্যে থাকা H+ আয়ন ব্যতীত অন্য যে-কোনো ক্যাটায়ন এবং OH– আয়ন ব্যতীত অন্য যে-কোনো অ্যানায়ন রেজিনের মধ্যে প্রবেশ করে। এই আয়নগুলি রেজিন থেকে তুল্য পরিমাণ H+ ও OH– আয়ন জলে মুক্ত করে। এই H+ ও OH– আয়ন যুক্ত হয়ে জলের অণু (H2O) গঠন করে। এইভাবে আয়নের বিনিময় হয় বলে এই পদ্ধতিকে ‘আয়ন বিনিময় পদ্ধতি’ বলা হয়।
খর জলের একটি নমুনায় \(Mg^{2+},HCO_3^-\) ও \(Cl^-\) আয়ন আছে। এই নমুনাকে আয়নমুক্ত জলে পরিণত করবে কীভাবে?
একটি পাত্রে ক্যাটায়ন বিনিময়কারী রেজিন রেখে তার মধ্যে দিয়ে খর জল চালনা করলে খর জলের মধ্যস্থ Mg2+ আয়ন ক্যাটায়ন বিনিময়কারী রেজিনের H+ আয়নের সঙ্গে স্থান বিনিময় করে অদ্রাব্য পদার্থরূপে জল থেকে পৃথক হয়।
2RSO3H + Mg2+ → R(SO3)2Mg↓ + 2H+
এরপর খর জলের নমুনাটি অপর একটি পাত্রে রাখা অ্যানায়ন বিনিময়কারী রেজিনের মধ্যে দিয়ে চালনা করলে খর জল মধ্যস্থ \(HCO_3^-\) ও \(Cl^-\) আয়ন অ্যানায়ন বিনিময়কারী রেজিনের OH– আয়নের সঙ্গে স্থান বিনিময় করে অদ্রাব্য পদার্থরূপে জল থেকে পৃথক হয়। এইভাবে খর জলের নমুনাকে আয়নমুক্ত জলে পরিণত করা যায়।
\(RNH_3^+OH^-+HCO_3^-\rightarrow RNH_3HCO_3+OH^-\)
\(RNH_3^+OH^-+Cl^-\rightarrow RNH_3Cl+OH^-\)
পাতিত জলে প্রস্তুত একটি চিনির দ্রবণকে পরপর ক্যাটায়ন ও অ্যানায়ন বিনিময়কারী রেজিনের মধ্যে দিয়ে চালনা করা হল। এই দ্রবণের স্বাদ কেমন হবে?
আয়ন বিনিময়কারী রেজিন শুধুমাত্র জলে উপস্থিত ক্যাটায়ন ও অ্যানায়নগুলিকে (H+ ও OH– ব্যতীত) অপসারিত করে। চিনি একটি তড়িৎ-অবিশ্লেষ্য পদার্থ। তাই আয়ন বিনিময়কারী রেজিন চিনিকে জল থেকে দূর করতে পারে না। সুতরাং, চিনির জলীয় দ্রবণকে পরপর ক্যাটায়ন ও অ্যানায়ন বিনিময়কারী রেজিনের মধ্য দিয়ে চালনা করলেও জলের স্বাদ মিষ্টিই থাকবে।
পাতিত জল ও আয়নমুক্ত জলের মধ্যে কোনটি ইনজেকশনের জন্য উপযুক্ত ও কেন?
অথবা, আয়নমুক্ত জল ও পাতিত জলের মধ্যে কোনটি বিশুদ্ধ এবং কেন?
আয়নমুক্ত জলে H+ এবং OH– আয়ন ব্যতীত অন্য কোনো আয়ন উপস্থিত থাকে না ঠিকই কিন্তু বিভিন্ন প্রকার তড়িৎ-অবিশ্লেষ্য পদার্থ, জৈব অশুদ্ধি, CO2 এবং সিলিকা, পাইরোজ প্রভৃতি উপস্থিত থাকতে পারে। অপরদিকে, পাতিত জলে সামান্য পরিমাণ CO2 বা সিলিকা ছাড়া অন্য কোনো তড়িৎ-অবিশ্লেষ্য বা অশুদ্ধি দ্রবীভূত থাকতে পারে না। ফলে, আয়নমুক্ত জল অপেক্ষা পাতিত জল বেশি বিশুদ্ধ। তাই ইনজেকশনের জন্য বা ওষুধ শিল্পে পাতিত জল ব্যবহার করা বেশি যুক্তিযুক্ত।
ব্যাটারিতে পাতিত জলের পরিবর্তে আয়নমুক্ত জল ব্যবহার করা হয় কেন?
ব্যাটারিতে ব্যবহৃত জলের তড়িৎ পরিবাহিতা যত কম হয় সেটি তত ভালো দ্রাবকরূপে ব্যবহৃত হয়। আয়নমুক্ত জলে শুধুমাত্র H+ ও OH– আয়ন থাকে। কিন্তু পাতিত জলে কোনো আয়ন থাকে না। পাতিত জলের থেকে আয়নমুক্ত জলের তড়িৎ পরিবাহিতা প্রায় দশগুণ কম। তাই ব্যাটারিতে পাতিত জলের পরিবর্তে আয়নমুক্ত জল ব্যবহার করা হয়।
পাতিত জল বিশুদ্ধ হলেও পানের অনুপযুক্ত কেন?
পানীয় জলে বিভিন্ন প্রয়োজনীয় ধাতু, যেমন – ক্যালশিয়াম, ম্যাগনেশিয়াম, আয়রন ইত্যাদির লবণ উপস্থিত থাকা একান্ত দরকার। কারণ – এইগুলি আমাদের শরীরে খনিজ লবণের চাহিদা পূরণ করে। পাতিত জলে এই সকল ধাতুর লবণ অনুপস্থিত থাকে বলে এই জল বিশুদ্ধ হওয়া সত্ত্বেও পানের অনুপযুক্ত।
পাতিত জলে জলজ প্রাণীরা বাঁচতে পারে না কেন?
পাতিত জল বিশুদ্ধ হলেও এতে দ্রবীভূত অক্সিজেন থাকে না। ফলে জলজ প্রাণীদের পাতিত জলে রাখলে তারা শ্বাসকার্যের জন্য প্রয়োজনীয় O2 পায় না এবং শ্বাস গ্রহণ করতে না পেরে মারা যায়।
তোমাকে একটি জলের নমুনা দেওয়া হল যার খরতার মাত্রা 0। এই জল কি ওষুধ শিল্পে ব্যবহার করা যাবে? যুক্তিসহ ব্যাখ্যা দাও।
কোনো জলের নমুনার খরতার মাত্রা শূন্য (0) হওয়ার অর্থ ওই জলের নমুনায় খরতা সৃষ্টিকারী Ca, Mg, Fe প্রভৃতি ধাতব আয়নগুলি অনুপস্থিত থাকে।
জলের নমুনার খরতার মাত্রা শূন্য হলেই যে তা ওষুধ শিল্পে ব্যবহার করা যাবে তা নয়। আয়নমুক্ত জল ও পাতিত জল উভয়েরই খরতার মাত্রা শূন্য। কিন্তু আয়নমুক্ত জলের খরতার মাত্রা শূন্য হলেও আয়নমুক্ত জলে –
- কিছু তড়িৎ-অবিশ্লেষ্য জৈব পদার্থ;
- দ্রবীভূত গ্যাসীয় পদার্থ, যেমন – CO2, O2;
- সিলিকা;
- পাইরোজেন নামক বিষাক্ত পদার্থ;
- জীবাণু উপস্থিত থাকতে পারে।
ওষুধের সঙ্গে এই সমস্ত পদার্থের বিক্রিয়ায় ওষুধের কার্যকারিতা নষ্ট হয়। ফলে ওষুধশিল্পে আয়নমুক্ত জল ব্যবহার করা যাবে না।
কিন্তু পাতিত জল আয়নমুক্ত জল অপেক্ষা বেশি বিশুদ্ধ এবং এর মধ্যে কোনো অপদ্রব্য থাকে না। তাই পাতিত জল ওষুধ শিল্পে ব্যবহার করা যায়।
ডিটারজেন্টের প্রভাবে জলে দ্রবীভূত অক্সিজেনের পরিমাণ হ্রাস পায় কেন?
ডিটারজেন্টে উপস্থিত ফসফেট শ্রেণির যৌগ জলে উপস্থিত Ca2+, Mg2+ আয়নের সঙ্গে বিক্রিয়া করে জলে দ্রাব্য জটিল লবণ উৎপন্ন করে। এই লবণ জলজ উদ্ভিদ ও শ্যাওলারা খাদ্য হিসেবে গ্রহণ করে। ফলে, তাদের দ্রুত বংশবৃদ্ধি ঘটে। এই সকল উদ্ভিদের শ্বসনের জন্য প্রচুর অক্সিজেনের প্রয়োজন হয়। ফলে, জলে দ্রবীভূত অক্সিজেনের পরিমাণ হ্রাস পায়।
পার্থক্যধর্মী প্রশ্নোত্তর
খর জল (Hard Water) ও মৃদু জলের (Soft Water) মধ্যে পার্থক্য লেখো।
খর জল (Hard Water) ও মৃদু জলের (Soft Water) মধ্যে পার্থক্যগুলি হল –
| বিষয় | খর জল (Hard Water) | মৃদু জল (Soft Water) |
| সংজ্ঞা | যে জলে অনেকটা পরিমাণ সাবান ঘষলে খুব সামান্য ফেনা উৎপন্ন হয়, তাকে খর জল (Hard Water) বলে। যেমন – সমুদ্রের জল, নদীর জল ইত্যাদি। | যে জলে খুব সামান্য সাবান ঘষলে অনেকটা ফেনা উৎপন্ন হয়, তাকে মৃদু জল (Soft Water) বলে। যেমন – পাতিত জল, বৃষ্টির জল ইত্যাদি। |
| উপস্থিত লবণ | এই জলে Ca, Fe, Mg ইত্যাদির বাইকার্বনেট, ক্লোরাইড বা সালফেট ইত্যাদি লবণ উপস্থিত থাকে। | এই জলে উক্ত লবণগুলি অনুপস্থিত। |
অস্থায়ী খরতা ও স্থায়ী খরতার মধ্যে পার্থক্য লেখো।
অস্থায়ী খরতা ও স্থায়ী খরতার মধ্যে পার্থক্যগুলি হল –
| বিষয় | অস্থায়ী খরতা (Temporary hardness) | স্থায়ী খরতা (Permanent hardness) |
| উপস্থিত লবণ | অস্থায়ী খরতা সৃষ্টিকারী লবণগুলি হল ক্যালশিয়াম, ম্যাগনেশিয়াম ও আয়রনের (Fe2+) বাইকার্বনেট লবণ। | স্থায়ী খরতা সৃষ্টিকারী লবণগুলি হল ক্যালশিয়াম, ম্যাগনেশিয়াম ও আয়রনের ক্লোরাইড ও সালফেট লবণ। |
| খরতা দূরীকরণ | অস্থায়ী খরতা স্ফুটন বা অন্য কোনো সহজ পদ্ধতিতে দূরীভূত করা যায়। | স্থায়ী খরতা সহজে দূর হয় না, বিশেষ রাসায়নিক পদ্ধতিতে (যেমন – আয়ন বিনিময় পদ্ধতিতে) দূরীভূত হয়। |
আয়নমুক্ত জল ও পাতিত জলের মধ্যে সাদৃশ্য ও পার্থক্য লেখো।
আয়নমুক্ত জল ও পাতিত জলের মধ্যে সাদৃশ্য ও পার্থক্যগুলি হল –
সাদৃশ্য –
- দ্রবীভূত লবণ – আয়নমুক্ত জল ও পাতিত জল উভয়েই কোনো লবণ দ্রবীভূত থাকে না।
- খরতার মাত্রা – জল ও পাতিত জল উভয়েরই খরতা শূন্য।
| বিষয় | আয়নমুক্ত জল (Deionised water) | পাতিত জল (Distilled water) |
| আয়নের উপস্থিতি | এই জলে সামান্য পরিমাণে H+ ও OH– আয়ন থাকে। | এই জলে কোনো আয়ন থাকে না। |
| বিশুদ্ধতা | এই জল অপেক্ষাকৃত কম বিশুদ্ধ। | এই জল অপেক্ষাকৃত বেশি বিশুদ্ধ। |
| তড়িৎ পরিবাহিতা | তড়িৎ পরিবাহিতা অপেক্ষাকৃত কম। | তড়িৎ পরিবাহিতা অপেক্ষাকৃত বেশি। |
| ব্যবহার | পরীক্ষাগারে ও ব্যাটারিতে এই জল ব্যবহার করা হয়। | ঔষধ শিল্পে, ইনজেকশন দেওয়ার কাজে পাতিত জল ব্যবহার করা হয়। |
| প্রস্তুতি | আয়ন বিনিময় পদ্ধতির সাহায্যে রেজিন ব্যবহার করে প্রস্তুত করা হয়। | পাতন পদ্ধতি ব্যবহার করে এই জল প্রস্তুত করা হয়। |
| দ্রবীভূত পদার্থ | আয়নমুক্ত জলে জৈব অশুদ্ধি, পাইরোজেন, CO2, O2 দ্রবীভূত থাকতে পারে। | পাতিত জলে কোনো অপদ্রব্য দ্রবীভূত থাকে না। |
নৈর্ব্যক্তিক প্রশ্নোত্তর
সঠিক উত্তরটি নির্বাচন করো
সেঁক দেবার বোতলে জল ব্যবহারের কারণ –
- জলের স্ফুটনাঙ্ক কম
- জল সহজপ্রাপ্য
- জলের আপেক্ষিক তাপ সর্বোচ্চ
- জলের ব্যতিক্রান্ত প্রসারণ ধর্ম আছে
উত্তর – 3. জলের আপেক্ষিক তাপ সর্বোচ্চ
জলের স্ফুটনাঙ্ক বেশি হবার কারণ –
- জলের আপেক্ষিক তাপ বেশি
- H -বন্ধনের উপস্থিতি
- জলের আপেক্ষিক গুরুত্ব কম
- ব্যতিক্রান্ত প্রসারণ
উত্তর – 2. H -বন্ধনের উপস্থিতি
বহুমুখী দ্রাবক হল –
- জল
- অ্যালকোহল
- কেরোসিন
- বেঞ্জিন
উত্তর – 1. জল
জলের পরাবৈদ্যুতিক ধ্রুবকের মান –
- 80.4
- 79.4
- 81.4
- 82.4
উত্তর – 1. 80.4
কোন্ উষ্ণতায় জলের ঘনত্ব সর্বাধিক? –
- 0°C
- 2°C
- 4°C
- 10°C
উত্তর – 3. 4°C
শীতপ্রধান দেশে কোনো জলাশয়ের উপরিতলে বরফ জমে গেলে হ্রদের তলদেশে তাপমাত্রা হয় –
- 0°C
- 4°C
- 3°C
- 2°C
উত্তর – 2. 4°C
কলিফর্ম কাউন্ট হল –
- জলের ফুওরাইড আয়নের পরিমাণ
- জলের খরতা সৃষ্টিকারী লবণের পরিমাণ
- জলে জীবাণুর পরিমাণ
- জলে উপস্থিত কীটনাশকের পরিমাণ
উত্তর – 3. জলে জীবাণুর পরিমাণ
পানীয় জলে দ্রবীভূত O2 (DO) -এর পরিমাণ –
- 3 – 6 ppm
- 4 – 6 ppm
- 1 – 2 ppm
- 3 – 4 ppm
উত্তর – 2. 4 – 6 ppm
জলকে জীবাণুমুক্ত করতে জলে যোগ করা হয় –
- ব্লিচিং পাউডার
- চুন
- ইউরিয়া
- ফটকিরি
উত্তর – 1. ব্লিচিং পাউডার
পানীয় জল প্রস্তুতির কোন্ পদ্ধতিতে সবচেয়ে বেশি জীবাণু ধ্বংস হয়? –
- স্ফুটন
- ক্লোরিনেশন
- UV
- কোনোটিই নয়
উত্তর – 3. UV
ওয়াটার ফিলটারে জলকে –
- আর্সেনিক মুক্ত করা হয়
- খরতা মুক্ত করা হয়
- পরিশোধিত করা হয়
- ফ্লুওরাইড মুক্ত করা হয়
উত্তর – 3. পরিশোধিত করা হয়
জলের খরতার কারণ হল –
- জলে দ্রবীভূত ধাতব ক্লোরাইড লবণ
- জলে দ্রবীভূত ধাতব নাইট্রেট লবণ
- জলে দ্রবীভূত ধাতব সালফাইড লবণ
- জলে দ্রবীভূত Ca, Fe, Mg -এর বাইকার্বনেট, ক্লোরাইড ও সালফেট লবণ
উত্তর – 4. জলে দ্রবীভূত Ca, Fe, Mg -এর বাইকার্বনেট, ক্লোরাইড ও সালফেট লবণ
জলের খরতা –
- 4 প্রকার
- 3 প্রকার
- 2 প্রকার
- 5 প্রকার
উত্তর – 3. 2 প্রকার
জলের খরতা বেশি হলে –
- সহজে ফেনা হয়
- ফেনা উৎপন্ন হয়ই না
- অনেকক্ষণ সাবান ব্যবহারের পর ফেনা হয়
- কোনোটিই নয়
উত্তর – 3. অনেকক্ষণ সাবান ব্যবহারের পর ফেনা হয়
কোন্ জোড়া আয়ন খর জল তৈরি হওয়ার কারণ নয় –
- বাইকার্বনেট, সালফেট
- বাইকার্বনেট, ক্লোরাইড
- নাইট্রেট, ফসফেট
- সালফেট, ক্লোরাইড
উত্তর – 3. নাইট্রেট, ফসফেট
জলের খরতা পরিমাপ করা হয় –
- MgCl2 -এর তুল্য পরিমাণ ভর দ্বারা
- MgCO3 -এর তুল্য পরিমাণ ভর দ্বারা
- CaCl2 -এর তুল্য পরিমাণ ভর দ্বারা
- CaCO3 -এর তুল্য পরিমাণ ভর দ্বারা
উত্তর – 4. CaCO3 -এর তুল্য পরিমাণ ভর দ্বারা
জলে খরতা পরিমাপের একক হল –
- g⋅L-1
- mol⋅L-1
- ppm
- Kg⋅L-1
উত্তর – 3. ppm
জলের খরতা 5 ppm হলে, প্রতি 1 লক্ষ ভাগ ওজনের জলে CaCO3 -এর পরিমাণ –
- 0.5 g
- 5 g
- 50 g
- 0.005 g
উত্তর – 1. 0.5 g
খর জলের সঙ্গে সাবানের বিক্রিয়ায় উৎপন্ন হয় –
- ফেনা
- অবশেষ
- স্কাম (Scum)
- অধঃক্ষেপ
উত্তর – 3. স্কাম (Scum)
একটি মৃদু জলের উৎস হল –
- ঝরনার জল
- বৃষ্টির জল
- নলকূপের জল
- নদীর জল
উত্তর – 2. বৃষ্টির জল
খর জলে উপস্থিত থাকে যে আয়ন –
- \(Ca^{2+}\)
- \(NH_4^+\)
- \(Na^+\)
- \(K^+\)
উত্তর – 1. \(Ca^{2+}\)
আয়নমুক্ত জলের খরতার মাত্রা –
- 0
- 2
- 4
- 7
উত্তর – 1. 0
জলের খরতা সৃষ্টি করে না এরূপ একটি লবণ হল –
- Mg(HCO3)2
- CaCl2
- FeSO4
- Na2SO4
উত্তর – 4. Na2SO4
জলে দ্রবীভূত আর্সেনিক যৌগ যে পদ্ধতিতে দূর করা যেতে পারে তা হল –
- ফিলটার
- পাতন
- কেলাসন
- সহ অধঃক্ষেপণ
উত্তর – 4. সহ অধঃক্ষেপণ
জলের অস্থায়ী খরতার কারণ –
- CaSO4
- CaCl2
- Ca(HCO3)2
- MgCl2
উত্তর – 3. Ca(HCO3)2
স্ফুটনের দ্বারা –
- জলের স্থায়ী খরতা দূর করা যায়
- জলকে আয়নমুক্ত করা যায়
- জলের অস্থায়ী খরতা দূর করা যায়
- জলকে বর্ণহীন করা যায়
উত্তর – 3. জলের অস্থায়ী খরতা দূর করা যায়
অস্থায়ী খরতাকে যদি স্ফুটনের সাহায্যে সম্পূর্ণ দূর করা না যায় তবে ওই জলে আছে –
- ক্যালশিয়াম বাইকার্বনেট
- ক্যালশিয়াম কার্বনেট
- ফেরাস কার্বনেট
- ম্যাগনেশিয়াম বাইকার্বনেট
উত্তর – 4. ম্যাগনেশিয়াম বাইকার্বনেট
ক্যাটায়ন বিনিময়কারী রেজিনকে প্রকাশ করা হয় –
- RH
- RNH2
- ROH
- RNH
উত্তর – 1. RH
ক্যাটায়ন বিনিময়কারী রেজিনের সাহায্যে জল থেকে অপসারিত করা হয় –
- ধাতব আয়ন
- অধাতব আয়ন
- ধাতব ও অধাতব আয়ন
- ফ্লুওরাইড আয়ন
উত্তর – 1. ধাতব আয়ন
ব্যবহৃত অ্যানায়ন বিনিময়কারী রেজিনে পুনরুজ্জীবিত করা হয় –
- লঘু HCl
- মধ্যম গাঢ় NaOH
- Ca(OH)2 দ্রবণ
- লঘু H2SO4
উত্তর – 2. মধ্যম গাঢ় NaOH
জলের অস্থায়ী ও স্থায়ী খরতা একই সঙ্গে দূর করা যায় –
- স্ফুটন পদ্ধতিতে
- ক্লোরিনেশন পদ্ধতিতে
- অতিবেগুনি রশ্মির সাহায্যে
- আয়ন বিনিময় রেজিন পদ্ধতিতে
উত্তর – 4. আয়ন বিনিময় রেজিন পদ্ধতিতে
খর জল মৃদু করার সময় নিঃশেষিত পারমুটিটকে পুনরায় জীবিত করলে তাতে যোগ করা হয় –
- KCl দ্রবণ
- CaCl2 দ্রবণ
- NaCl দ্রবণ
- CaCO3 দ্রবণ
উত্তর – 3. NaCl দ্রবণ
কোন্ বিবৃতিটি সঠিক? –
- আয়নমুক্ত জলের চেয়ে পাতিত জল বেশি বিশুদ্ধ
- আয়নমুক্ত জল বেশি বিশুদ্ধ
- আয়নমুক্ত জল ও পাতিত জল সমান বিশুদ্ধ
- আয়নমুক্ত জল ও পাতিত জল সমান অবিশুদ্ধ
উত্তর – 1. আয়নমুক্ত জলের চেয়ে পাতিত জল বেশি বিশুদ্ধ
ইনজেকশন দেওয়ার জন্য ব্যবহৃত হয় –
- পাতিত জল
- আয়নমুক্ত জল
- মৃদু জল
- সবকটি
উত্তর – 1. পাতিত জল
ডায়েলড্রিন হল এক প্রকার –
- ডিটারজেন্ট
- কীটনাশক ও পেস্টনাশক
- তেজস্ক্রিয় বর্জ্য
- রাসায়নিক সার
উত্তর – 2. কীটনাশক ও পেস্টনাশক
জলদূষণের জন্য দায়ী যৌগটি হল –
- NaCl
- AlCl3
- MgCl2
- Na3AsO3
উত্তর – 4. Na3AsO3
নাইট্রেট আয়নযুক্ত জল পান করলে যে রোগ হয় –
- মিথেমোগ্লোবিনেমিয়া
- ইতাই-ইতাই
- ব্ল্যাকফুট ডিজিজ
- কোনোটিই নয়
উত্তর – 1. মিথেমোগ্লোবিনেমিয়া
অতিরিক্ত নাইট্রেট মিশ্রিত জল পানে শিশুদের নিম্নলিখিত কোন্ রোগটি দেখা যায়? –
- নক-নী সিনড্রোম
- ব্লু-বেবি সিনড্রোম
- কেরাটোসিস
- রিকেট
উত্তর – 2. ব্লু-বেবি সিনড্রোম
কোনটি ইউট্রোফিকেশনের কারণ নয়? –
- জলে ডিটারজেন্টজনিত দূষণ
- জলে ফসফেট আয়নের \(PO_4^{3-}\) উপস্থিতি
- কৃষিজমিতে ব্যবহৃত সারের জলে মিশে যাওয়া
- জলের খরতা
উত্তর – 4. জলের খরতা
এনড্রিন হল –
- অজৈব সার
- আর্সেনিক যৌগ
- পেস্টনাশক
- ডিটারজেন্ট
উত্তর – 3. পেস্টনাশক
বর্তমানে পশ্চিমবঙ্গের জলে যে পদার্থটির উপস্থিতির জন্য জলদূষণ চিন্তার কারণ হয়ে দাঁড়িয়েছে তা হল –
- ফ্লুওরাইড
- আর্সেনিক
- লেড
- মারকারি
উত্তর – 2. আর্সেনিক
জলে শৈবালের অতিবৃদ্ধির জন্য দায়ী –
- ক্লোরাইড
- ফসফেট
- আর্সেনিক
- ফ্লুওরাইড
উত্তর – 2. ফসফেট
ইউট্রোফিকেশনের ফলে জলে –
- অক্সিজেনের পরিমাণ কমে যায়
- অক্সিজেনের পরিমাণ বেড়ে যায়
- অক্সিজেনের পরিমাণ একই থাকে
- কার্বন ডাইঅক্সাইডের পরিমাণ কমে যায়
উত্তর – 1. অক্সিজেনের পরিমাণ কমে যায়
পশ্চিমবঙ্গের কোন্ জেলায় আর্সেনিক দূষণের প্রভাব সবচেয়ে বেশি? –
- মালদহ
- মুরশিদাবাদ
- নদিয়া
- বর্ধমান
উত্তর – 2. মুরশিদাবাদ
WHO -এর মতে, পানীয় জলে আর্সেনিকের নিরাপদ মাত্রার সীমামান হল –
- 0.06 – 0.09 mg/L
- 0.12 – 0.15 mg/L
- 0.17 – 0.20 mg/L
- 0.01 – 0.05 mg/L
উত্তর – 4. 0.01 – 0.05 mg/L
ব্ল্যাকফুট রোগটি জলে যে উপাদান বেশি থাকলে হয় তা হল –
- ফ্লুওরিন
- ক্লোরিন
- আর্সেনিক
- পারদ
উত্তর – 3. আর্সেনিক
মিনামাটা রোগ সৃষ্টি হয় –
- আর্সেনিকঘটিত দূষণ
- মারকারিঘটিত দূষণ
- ফ্লুওরাইডঘটিত দূষণ
- ফসফেটঘটিত দূষণ
উত্তর – 2. মারকারিঘটিত দূষণ
নক্-নী ডিজিজ -এর কারণ –
- Ca
- F
- Fe
- Cl
উত্তর – 2. F
শূন্যস্থান পূরণ করো
জল একটি ___ যৌগ।
উত্তর – জল একটি সমযোজী যৌগ।
জল একটি ___, ___ তরল।
উত্তর – জল একটি বর্ণহীন, গন্ধহীন তরল।
___ ক্রিয়ার দরুন শিকড়ের সাহায্যে সংগৃহীত জল গাছের কাণ্ডের মধ্যে দিয়ে পাতায় পৌঁছোয়।
উত্তর – কৈশিক ক্রিয়ার দরুন শিকড়ের সাহায্যে সংগৃহীত জল গাছের কাণ্ডের মধ্যে দিয়ে পাতায় পৌঁছোয়।
0°C তাপমাত্রায় 1000 mL জলে দ্রবীভূত অক্সিজেনের পরিমাণ প্রায় ___।
উত্তর – 0°C তাপমাত্রায় 1000 mL জলে দ্রবীভূত অক্সিজেনের পরিমাণ প্রায় 30 mL।
___ জলে অল্প সাবান ঘষলে ফেনা উৎপন্ন হয়।
উত্তর – মৃদু জলে অল্প সাবান ঘষলে ফেনা উৎপন্ন হয়।
রান্নার কাজে ___ ব্যবহার করা উচিত।
উত্তর – রান্নার কাজে মৃদু জল ব্যবহার করা উচিত।
খর জলে ক্যালশিয়াম, ম্যাগনেশিয়ামের ___ ও ___ লবণ উপস্থিত থাকে।
উত্তর – খর জলে ক্যালশিয়াম, ম্যাগনেশিয়ামের ক্লোরাইড ও বাইকার্বনেট লবণ উপস্থিত থাকে।
পানীয় জলে বাইকার্বনেট লবণ থাকলে ___ খরতার সৃষ্টি হয়।
উত্তর – পানীয় জলে বাইকার্বনেট লবণ থাকলে অস্থায়ী খরতার সৃষ্টি হয়।
জল ফুটিয়ে দূর করা যায় না ___ খরতায়।
উত্তর – জল ফুটিয়ে দূর করা যায় না স্থায়ী খরতায়।
অ্যানায়ন বিনিময়কারী রেজিনের সাধারণ সংকেত ___।
উত্তর – অ্যানায়ন বিনিময়কারী রেজিনের সাধারণ সংকেত \(RNH_2^+OH^-\)।
রেজিন পদ্ধতির অপর নাম ___ পদ্ধতি।
উত্তর – রেজিন পদ্ধতির অপর নাম আয়ন বিনিময় পদ্ধতি।
আয়নমুক্ত জলে সামান্য ___ ও ___ আয়ন থাকে।
উত্তর – আয়নমুক্ত জলে সামান্য H+ ও OH– আয়ন থাকে।
জলে দ্রবীভূত আর্সেনিকের মান ___ ppm -এর বেশি হলে, জলে আর্সেনিক দূষণ হয়।
উত্তর – জলে দ্রবীভূত আর্সেনিকের মান 0.05 ppm-এর বেশি হলে, জলে আর্সেনিক দূষণ হয়।
জলে ফ্লুওরাইড দূষণের জন্য মানবদেহে ___ রোগ হয়।
উত্তর – জলে ফ্লুওরাইড দূষণের জন্য মানবদেহে ফ্লুওরোসিস রোগ হয়।
জল পান করার আগে পরিশোধন করা দরকার। প্রতি বছর ___ মানুষ জলবাহিত রোগে মারা যায়।
উত্তর – জল পান করার আগে পরিশোধন করা দরকার। প্রতি বছর 3.4 মিলিয়ন মানুষ জলবাহিত রোগে মারা যায়।
___ একটি Billboard রয়েছে যা বায়ু থেকে পানীয় জল প্রস্তুত করে।
পেরুতে একটি Billboard রয়েছে যা বায়ু থেকে পানীয় জল প্রস্তুত করে।
সমুদ্রের জল আমাদের পৃথিবীর অন্যতম জলের উৎস। প্রতি কেজি সমুদ্রের জলে ___ লবণ থাকে।
উত্তর – সমুদ্রের জল আমাদের পৃথিবীর অন্যতম জলের উৎস। প্রতি কেজি সমুদ্রের জলে 35 গ্রাম লবণ থাকে।
ঠিক বা ভুল নির্বাচন করো
জলের বাষ্পীভবনের লীনতাপ ৪০ ক্যালোরি/গ্রাম।
উত্তর – ভুল।
সঠিক উত্তর – ক্যালোরি/গ্রাম।
জল বরফে পরিণত হলে আয়তন বৃদ্ধি পায়, ফলে ঘনত্ব কমে।
উত্তর – ঠিক।
অনার্দ্র সাদা CuSO4 জলের উপস্থিতিতে নীল বর্ণ ধারণ করে।
উত্তর – ঠিক।
জল একটি পোলার অণু, যার দ্বিমেরু ভ্রামকের মান প্রায় 80।
উত্তর – ঠিক।
পানীয় জল শোধনের একটি ঘরোয়া পদ্ধতি হল স্ফুটন।
উত্তর – ঠিক।
জিওলাইট -এর সংকেত Na2O, Al2O3, 3SiO3, 2H2O।
উত্তর – ঠিক।
কোনো জলের নমুনায় Na+ ক্যাটায়ন থাকলে জলটি খর হবে।
উত্তর – ভুল।
সঠিক উত্তর – খর হয় না।
বৃষ্টির জল অপচয় না করে তাকে ভবিষ্যতের জন্য সঞ্চয় করে রাখার পদ্ধতিই ‘রেন ওয়াটার হার্ভেস্টিং’ -এর মূল কথা।
উত্তর – ঠিক।
ডিটারজেন্ট খর জলেও ফেনা উৎপন্ন করতে পারে।
উত্তর – ঠিক।
দু-একটি শব্দে উত্তর দাও
মানবদেহের রক্তের কত শতাংশ জল?
মানবদেহের রক্তের 90 শতাংশ জল।
জল খুব ভালো কুল্যান্ট হিসেবে কাজ করে কোন্ ধর্মের জন্য?
জল খুব ভালো কুল্যান্ট হিসেবে কাজ করে উচ্চ আপেক্ষিক তাপের জন্য ধর্মের।
জলের আপেক্ষিক তাপের মান কত?
জলের আপেক্ষিক তাপের মান 1 cal⋅g-1⋅°C-1 (CGS পদ্ধতিতে)।
জলের কোন্ ভৌত ধর্মগুলি আমাদের দেহের তাপমাত্রা বজায় রাখতে সাহায্য করে?
জলের উচ্চ আপেক্ষিক তাপ ও বাষ্পীভবনের লীনতাপ ভৌত ধর্মগুলি আমাদের দেহের তাপমাত্রা বজায় রাখতে সাহায্য করে?।
জলের রাসায়নিক নাম কী?
জলের রাসায়নিক নাম ডাই হাইড্রোজেন মনোক্সাইড।
জলজ প্রাণীরা কীভাবে শ্বাসকার্য চালায়?
জলজ প্রাণীরা জলে দ্রবীভূত অক্সিজেনের সাহায্যে শ্বাসকার্য চালায়।
জলে দ্রবীভূত অক্সিজেনকে কোন্ পদার্থ দ্বারা দূর করা যায়?
জলে দ্রবীভূত অক্সিজেনকে সোডিয়াম সালফাইট (Na2SO3) পদার্থ দ্বারা দূর করা যায়।
কলিফর্ম কাউন্টে গণ্য করা হয় এমন একটি ব্যাকটেরিয়ার নাম লেখো।
কলিফর্ম কাউন্টে গণ্য করা হয় এমন একটি ব্যাকটেরিয়ার নাম হল এসচেরিশিয়া কোলাই (Escherichia Coli)।
বিশুদ্ধ জলের ‘কলিফর্ম কাউন্ট’ কত হওয়া উচিত?
বিশুদ্ধ জলের ‘কলিফর্ম কাউন্ট’ শূন্য হওয়া উচিত।
জলে DO -এর মান কমে গেলে দূষণের মাত্রার কী পরিবর্তন হয়?
জলে DO -এর মান কমে গেলে দূষণের মাত্রা বৃদ্ধি পাবে।
BOD -এর পুরো কথাটি কী?
BOD -এর পুরো কথাটি Biological Oxygen Demand.
COD -এর সম্পূর্ণ কথাটি কী?
COD -এর সম্পূর্ণ কথাটি Chemical Oxygen Demand.
সর্বজনীন দ্রাবক কাকে বলে?
সর্বজনীন দ্রাবক জলকে বলে।
বিশ্ব জল দিবস কবে পালিত হয়?
বিশ্ব জল দিবস 22 মার্চ পালিত হয়।
জলের মাধ্যমে সংক্রামিত দুটি রোগের নাম লেখো।
জলের মাধ্যমে সংক্রামিত দুটি রোগের নাম হল টাইফয়েড, কলেরা।
জলে ভাসমান পদার্থ দূর করতে জলে কী মেশানো হয়?
জলে ভাসমান পদার্থ দূর করতে জলে ফটকিরি মেশানো হয়।
জলের সঙ্গে কোন্ হ্যালোজেন মৌল যোগ করে জীবাণুমুক্ত করা হয়?
জলের সঙ্গে ক্লোরিন হ্যালোজেন মৌল যোগ করে জীবাণুমুক্ত করা হয়।
জিওলিন ট্যাবলেট থেকে কোন্ গ্যাস উৎপন্ন হয় যা জলকে জীবাণুমুক্ত রাখতে সাহায্য করে?
জিওলিন ট্যাবলেট থেকে ক্লোরিন গ্যাস উৎপন্ন হয় যা জলকে জীবাণুমুক্ত রাখতে সাহায্য করে।
পানীয় জলের ক্ষেত্রে TDS কথাটির সম্পূর্ণ নাম কী?
পানীয় জলের ক্ষেত্রে TDS কথাটির সম্পূর্ণ নাম হল Total Dissolved Solids বা দ্রবীভূত কঠিন পদার্থ।
বয়লারে খর জল না মৃদু জল কোনটি ব্যবহার করা হয়?
বয়লারে খর মৃদু জল ব্যবহার করা হয়।
ক্যাটায়ন বিনিময়কারী রেজিনে কোন্ আয়ন থাকে?
ক্যাটায়ন বিনিময়কারী রেজিনে হাইড্রোজেন আয়ন (H+) থাকে।
জলের একটি নমুনায় ফেরাস সালফেট পাওয়া গেল। ওই জলের খরতা কোন্ প্রকৃতির?
জলের একটি নমুনায় ফেরাস সালফেট পাওয়া গেল। ওই জলের খরতা স্থায়ী প্রকৃতির।
ক্যাটায়ন বিনিময়কারী রেজিনকে কার্যক্ষম করার জন্য কী চালনা করা হয়?
ক্যাটায়ন বিনিময়কারী রেজিনকে কার্যক্ষম করার জন্য লঘু H2SO4 চালনা করা হয়।
অ্যানায়ন বিনিময়কারী রেজিনে কোন্ অজৈব মূলক যুক্ত থাকে?
অ্যানায়ন বিনিময়কারী রেজিনে অ্যামিন (-NH2) অজৈব মূলক যুক্ত থাকে।
খর জলে দ্রবীভূত একটি সালফেট লবণের নাম লেখো।
খর জলে দ্রবীভূত একটি সালফেট লবণের নাম খর জলে দ্রবীভূত একটি সালফেট লবণের নাম হল ম্যাগনেশিয়াম সালফেট।
খর জলের একটি নমুনায় MgSO4 ও Mg (HCO3)2 দ্রবীভূত অবস্থায় আছে। ওই জলকে কীভাবে আয়নমুক্ত জলে পরিণত করবে?
খর জলের একটি নমুনায় MgSO4 ও Mg (HCO3)2 দ্রবীভূত অবস্থায় আছে। ওই জলকে আয়ন বিনিময় রেজিন ব্যবহারের মাধ্যমে আয়নমুক্ত জলে পরিণত করবে।
জলে কোন্ কোন্ আয়ন উপস্থিত থাকলে জল খর হয় না?
জলে \(Na^+,K^+,NH_4^+\) আয়ন উপস্থিত থাকলে জল খর হয় না।
সোডিয়াম পারমুটিটের সংকেত কী?
সোডিয়াম পারমুটিটের সংকেত হল NaAlSiO4, 3H2O।
ক্যাটায়ন বিনিময়কারী রেজিন থেকে নির্গত জলের প্রকৃতি কীরূপ হয়?
ক্যাটায়ন বিনিময়কারী রেজিন থেকে নির্গত জলের প্রকৃতি আম্লিক হয়।
আয়নমুক্ত জলে অশুদ্ধি হিসেবে কী উপস্থিত থাকে?
আয়নমুক্ত জলে অশুদ্ধি হিসেবে তড়িৎ-অবিশ্লেষ্য জৈব পদার্থ উপস্থিত থাকে।
ভারী জলের কোন্ ধর্মের জন্য ভারী জলে স্নান করা স্বাস্থ্যের পক্ষে ক্ষতিকারক?
ভারী জলের জলাকর্ষী ধর্মের জন্য ভারী জলে স্নান করা স্বাস্থ্যের পক্ষে ক্ষতিকারক।
কোন্ যৌগিক পদার্থের উপস্থিতিতে নলকূপের জল বাদামি বর্ণের হয়?
ফেরিক হাইড্রক্সাইড [Fe(OH)3] যৌগিক পদার্থের উপস্থিতিতে নলকূপের জল বাদামি বর্ণের হয়।
পানীয় জলে উপস্থিত কোন্ দূষক রক্তাল্পতা সৃষ্টি করে?
পানীয় জলে উপস্থিত নাইট্রেট দূষক রক্তাল্পতা সৃষ্টি করে।
একটি ক্লোরিনঘটিত ও একটি ফসফেটঘটিত পেস্টিসাইডের নাম লেখো।
একটি ক্লোরিনঘটিত ও একটি ফসফেটঘটিত পেস্টিসাইডের নাম হল DDT এবং ম্যালাথিয়ন।
একটি কীটনাশকের নাম লেখো।
একটি কীটনাশকের নাম হল গ্যামাক্সিন।
অ্যালগাল ব্লমের জন্য দায়ী কোন যৌগ?
অ্যালগাল ব্লমের জন্য দায়ী সার ও ডিটারজেন্টে উপস্থিত ফসফেট যৌগ।
প্যারিস গ্রিন কী?
প্যারিস গ্রিন হল কাঠের পোকা ধ্বংসকারী কীটনাশক।
প্যারিস গ্রিনের রাসায়নিক নাম কী?
প্যারিস গ্রিনের রাসায়নিক নাম কপার হল আর্সেনাইট।
দুটি দীর্ঘস্থায়ী জৈব দূষক বা POP (Permanent Organic Pollutant) -এর নাম লেখো।
দুটি দীর্ঘস্থায়ী জৈব দূষক বা POP (Permanent Organic Pollutant) -এর নাম হল মিথাইল মারকারি এবং DDT।
কোন্ ধাতুকল্পঘটিত যৌগের অতিরিক্ত উপস্থিতি জলদূষণ ঘটায়?
আর্সেনিকঘটিত যৌগ ধাতুকল্পঘটিত যৌগের অতিরিক্ত উপস্থিতি জলদূষণ ঘটায়।
পানীয় জলে ক্লোরাইডের সর্বোচ্চ অনুমোদনযোগ্য সীমা উল্লেখ করো।
পানীয় জলে ক্লোরাইডের সর্বোচ্চ অনুমোদনযোগ্য 250 mg/L সীমা উল্লেখ করো।
জলে ফুওরাইডের পরিমাণ সর্বোচ্চ কোন্ সীমা অতিক্রম করলে দাঁতের ক্ষয় হয়?
জলে ফুওরাইডের পরিমাণ সর্বোচ্চ 1.5 mg/L সীমা অতিক্রম করলে দাঁতের ক্ষয় হয়।
কোন্ কোন্ পদার্থ থেকে ফুওরাইড জলে এসে মেশে?
ক্রায়োলাইট (Na3AlF6), ফ্লুয়োস্পার (CaF2), ফ্লুরঅ্যাপাটাইট [3Ca3(PO4)2⋅CaF2] পদার্থ থেকে ফ্লুওরাইড জলে এসে মেশে।
দন্তক্ষয় রোধ করে কোন্ আয়ন?
দন্তক্ষয় রোধ করে ফ্লুওরাইড আয়ন (F–)।
জলে কোনো নমুনায় CaCl2 মিশ্রিত থাকলে সেই জলের খরতা কোন্ ধরনের হবে?
জলে কোনো নমুনায় CaCl2 মিশ্রিত থাকলে সেই জলের খরতা স্থায়ী খরতা ধরনের হবে।
ক্লোরিন একটি বিষাক্ত, দুর্গন্ধযুক্ত গ্যাস হওয়া সত্ত্বেও কী কাজে ব্যবহার করা হয়?
ক্লোরিন একটি বিষাক্ত, দুর্গন্ধযুক্ত গ্যাস হওয়া সত্ত্বেও একে পানীয় জল এবং সুইমিং পুল -এর জল শোধন করার কাজে ব্যবহার করা হয়।
USA -তে প্রতিদিন কত গ্যালন জল পরিশোধিত হয়?
USA -তে প্রতিদিন 3,46,000 মিলিয়ন গ্যালন জল পরিশোধিত হয়।
বামদিকের সঙ্গে ডানদিক মিল করো
নীচের বামদিকের সঙ্গে ডানদিক মিলিয়ে লেখো।
| বামদিক | ডানদিক | উত্তর |
| 1. ক্যালশিয়াম বাইকার্বনেট | a. ফ্লুওরিন দূষণের প্রভাবে হয় | 1. → g. |
| 2. ব্ল্যাকফুট ডিজিজ | b. আয়ন বিনিময় রেজিন পদ্ধতিতে | 2. → f. |
| 3. সমুদ্রের জল | c. দীর্ঘস্থায়ী জৈব দূষক | 3. → h. |
| 4. পৃথিবীর সমুদ্রে লবণাক্ত জলের পরিমাণ | d. ইউট্রোফিকেশন | 4. → j. |
| 5. দাঁত ও অস্থিসন্ধির ক্ষয় | e. রেন ওয়াটার হার্ভেস্টিং | 5. → a. |
| 6. স্থায়ী খরতা দূর হয় | f. আর্সেনিক দূষণের প্রভাবে হয় | 6. → b. |
| 7. বয়লারে ব্যবহৃত জল | g. অস্থায়ী খরতা সৃষ্টি করে | 7. → i. |
| 8. জল সংকট | h. খর জল | 8. → e. |
| 9. DDT | i. মৃদু জল | 9. → c. |
| 10. সার মিশ্রিত জল | j. 97% | 10. → d. |
For High-Types
ভারী জল কী? ভারী জলে স্নান করা স্বাস্থ্যের পক্ষে ক্ষতিকারক কেন?
হাইড্রোজেনের আইসোটোপ ডয়টেরিয়ামের (1D2) সঙ্গে অক্সিজেনের বিক্রিয়ায় ভারী জল উৎপন্ন হয়। প্রাকৃতিক জলের নমুনাকে বারবার তড়িদবিশ্লেষণ করলে ভারী জল পাওয়া যায়। এর আণবিক ভর 20। নিউক্লিয়ার প্ল্যান্টে কুল্যান্ট রূপে ব্যবহার করা হয়।
ভারী জল একটি তীব্র জলাকর্ষী পদার্থ, যা শরীর থেকে জল শোষণ করে নেয়। তাই ভারী জলে স্নান করলে শরীরের মধ্যে H2O : D2O -এর অনুপাত পরিবর্তিত হয়। ফলে শরীরের বিভিন্ন ধমনির মধ্যে দিয়ে তরলের প্রবাহ কমে যায় যা শরীরের পক্ষে ক্ষতিকারক।
পেট্রোলঘটিত আগুন জল দিয়ে নেভানো যায় না কেন?
জলের বাষ্পীভবনের লীনতাপ 537 ক্যালোরি/গ্রাম। জ্বলন্ত বস্তুর ওপর জল দিলে জল ওই জ্বলন্ত বস্তু থেকে তাপ সংগ্রহ করে দ্রুত বাষ্পীভূত হয়। জ্বলন্ত বস্তুর উষ্ণতা তখন হঠাৎ জ্বলনাঙ্কের নীচে নেমে আসে। আবার উৎপন্ন জলীয় বাষ্প ওই বস্তুর ওপর একটি আচ্ছাদন সৃষ্টি করে অক্সিজেনের সংস্পর্শ ছিন্ন করে দেয়। ফলে, জ্বলন্ত বস্তুটি তখন নিভে যায়। কিন্তু পেট্রোলঘটিত আগুনের ক্ষেত্রে পেট্রোল জলের থেকে হালকা হওয়ায়, এতে জল দিলে এটি দ্রুত জলের উপর উঠে আসে এবং বাতাসের সংস্পর্শ লাভ করে। জল বাষ্পীভূত হওয়ার কোনো সুযোগ পায় না। তাছাড়া পেট্রোলের জ্বলনাঙ্ক কম। তাই পেট্রোলঘটিত আগুন জল দিয়ে নেভানো যায় না।
D.O.C কাকে বলে?
জলে দ্রবীভূত জৈব কার্বনকে বলা হয় D.O.C। D.O.C -এর পুরো কথা – Dissolved Organic Carbon। ভূপৃষ্ঠীও জলের ক্ষেত্রে এর গড় মান 5 ppm। খাল, বিল, ডোবার ক্ষেত্রে D.O.C -এর মান অনেক বেশি হয়।
T.O.C কাকে বলে?
জলে দ্রবীভূত জৈব পদার্থের মোট কার্বনকে বলা হয় T.O.C (Total Organic Carbon)। ভূগর্ভস্থ জলের ক্ষেত্রে T.O.C -এর গড় মান 1 ppm।
ট্রিপল্ পয়েন্ট কী?
যে নির্দিষ্ট উষ্ণতা ও চাপে কোনো পদার্থের তিনটি ভৌত অবস্থা (কঠিন-তরল-গ্যাসীয়) তাপগতীয় সাম্যাবস্থায় থাকে, তাকে উক্ত পদার্থটির ট্রিপল্ পয়েন্ট বা ত্রৈধ বিন্দু বলে।
যেমন – জলের ট্রিপল্ পয়েন্টে উষ্ণতা 273.16 K (0.01°C) এবং চাপ 0.006036 atm (6.11657 milibar) ।
অনুঘটকরূপে জলের ক্রিয়া বর্ণনা করো।
কতকগুলি রাসায়নিক বিক্রিয়ায় জল অনুঘটকরূপে কাজ করে বিক্রিয়ার বেগ বৃদ্ধি করে। যেমন –
- অক্সিজেনের মধ্যে স্বল্প পরিমাণ জলীয় বাষ্পের উপস্থিতিতে কার্বন মনোক্সাইড অক্সিজেনের সঙ্গে বিক্রিয়া করে কার্বন ডাইঅক্সাইড উৎপন্ন করে [2CO + O2 = 2CO2]।
- স্বল্প পরিমাণ জলীয় বাষ্পের উপস্থিতিতে হাইড্রোজেন ও অক্সিজেনের মিশ্রণে তড়িৎস্ফুলিঙ্গ চালনা করলে জল উৎপন্ন হয় [2H2 + O2 → 2H2O]।
সমুদ্রের জলকে Reverse Osmosis দ্বারা কীভাবে শোধন করা হয়?
সমুদ্রের জলকে বিশুদ্ধ পানীয় জলের সঙ্গে অর্ধভেদ্য পর্দা দ্বারা পৃথক করে রাখা হয়। সমুদ্রের জলে অভিস্রবণ চাপ অপেক্ষা বেশি চাপ প্রয়োগ করা হয়। এর ফলে সমুদ্রের জল থেকে বিশুদ্ধ জল বেরিয়ে পর্দা ভেদ করে বিশুদ্ধ পানীয় জলে প্রবেশ করে।
জলের একটি নমুনায় খরতার মাত্রা 40 ppm। যদি খরতা কেবলমাত্র ম্যাগনেশিয়াম সালফেটের জন্য হয়ে থাকে, তবে 2 kg ওই জলের নমুনায় কত পরিমাণ ম্যাগনেশিয়াম সালফেট থাকবে?
জলের একটি নমুনায় খরতার মাত্রা = 40 ppm
106 g জলে উপস্থিত ক্যালশিয়াম কার্বনেটের পরিমাণ = 40 g
1 মোল CaCO3 = 1 মোল MgSO4
বা, 100 g CaCO3 = 120 g MgSO4
40 g CaCO3 = \(\frac{120}{100}\times40\) g = 48 g MgSO4
106 g জলে উপস্থিত ম্যাগনেশিয়াম সালফেটের পরিমাণ = 48 g
1 g জলে উপস্থিত ম্যাগনেশিয়াম সালফেটের পরিমাণ = \(\frac{48}{10^6}\) g
2 kg বা, 2 × 103 g জলে উপস্থিত ম্যাগনেশিয়াম সালফেটের পরিমাণ = \(\frac{48\times2\times10^3}{10^6}\) g = 0.096 g
∴ 2 kg ওই জলের নমুনায় 0.096 g MgSO4 থাকবে।
জলের খরতা নির্ণয়ে ব্যবহৃত EDTA যৌগটির রাসায়নিক নাম লেখো।
জলের খরতা নির্ণয়ে ব্যবহৃত EDTA যোগটির রাসায়নিক নাম ইথিলিন ডাইঅ্যামিন টেট্রা অ্যাসিটিক অ্যাসিডের ডাই সোডিয়াম লবণ।
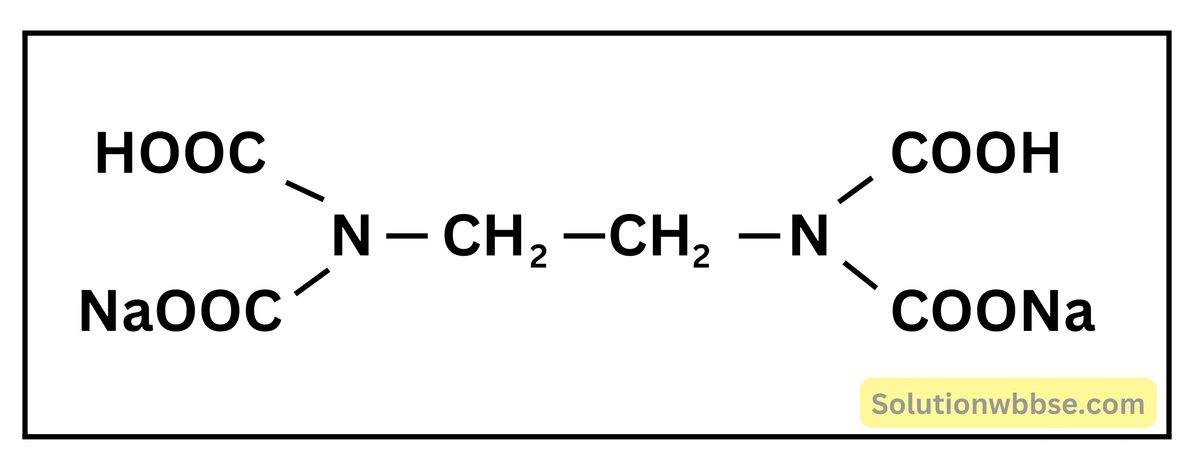
ক্যালগন কী?
ক্যালগন হল সোডিয়াম হেক্সামেটাফসফেট। এর সংকেত Na2[Na4(PO3)6]। খর জলকে মৃদু জলে পরিণত করতে এটি ব্যবহৃত হয়। বয়লারে খর জলকে মৃদু করতে ক্যালগন ব্যবহৃত হয়।
PCB বলতে কী বোঝায়?
PCB -এর পুরো কথাটি হল পলিক্লোরিনেটেড বাইফিনাইল। এটি ট্রান্সফর্মার এবং ক্যাপাসিটরের ‘ফ্লুইড’ হিসেবে ব্যবহৃত হয়। এই যৌগগুলি জীবদেহের ত্বককে ক্ষতিগ্রস্ত করায় এদের জলদূষক হিসেবে চিহ্নিত করা হয়েছে।
তাপজনিত দূষণ কী?
তাপজনিত দূষণ – তাপবিদ্যুৎ কেন্দ্র, তৈলশোধনাগার থেকে যে গরম জল বর্জ্যরূপে নদীতে বা বড়ো জলাশয়ে ফেলা হয় তাতে নদী বা জলাশয়ের জলের উয়তা যথেষ্ট পরিমাণে বৃদ্ধি পায়। উষ্ণতা বৃদ্ধির ফলে জলে দ্রবীভূত অক্সিজেন কমে যায় এবং জলজ প্রাণীরা ক্ষতিগ্রস্ত হয়। এই ধরনের দূষণকে তাপজনিত দূষণ বলে।
জৈব বিবর্ধন কী?
জৈব বিবর্ধন (Bio-magnification) – জীবদেহের মেদযুক্ত কলায় খাদ্যশৃঙ্খলের মাধ্যমে বিষাক্ত, দীর্ঘস্থায়ী জৈব দূষকের (যেমন – DDT, অ্যালড্রিন, মারকারিঘটিত যৌগ মিথাইল মারকারি ইত্যাদি) ক্রমবর্ধমান সঞ্চিত হওয়ার ঘটনাকে জৈব বিবর্ধন বলে।
মৃত্তিকায় উপস্থিত আর্সেনিক মানুষের বাস্তুতন্ত্রের ওপর কীরূপ প্রভাব ফেলে?
মৃত্তিকা মানুষের একটি অতীব উপকারী প্রাকৃতিক সম্পদ। কিন্তু আর্সেনিক ও অন্যান্য দূষিত পদার্থের উপস্থিতি ও সঞ্চয়ের কারণে এই মাটি দূষিত হয়ে পড়ে। কীটনাশক, সার, আগাছানাশক হিসেবে মাটিতে এর পরিমাণ ক্রমশ বৃদ্ধি পায়। মৃত্তিকাস্থ আর্সেনিক উদ্ভিদের ওপর বিষক্রিয়া সৃষ্টি করে এবং উদ্ভিদের পাতা, ফল, মূলে সঞ্চিত থাকে। এই উদ্ভিদ খাদ্য হিসেবে গ্রহণ করলে উদ্ভিদদেহে সঞ্চিত আর্সেনিক প্রাণীদেহে প্রবেশ করে। এইভাবে সমগ্র বাস্তুতন্ত্র আর্সেনিক দ্বারা সংক্রামিত হয়।
Endemic Fluorosis কী?
পানীয় জলে ফুওরাইডের পরিমাণ 1 – 1.5 mg/L -এর বেশি হলে যে রোগ হয়, তাকে Endemic Fluorosis বলে।
Class 9 Physical Science – Notes for All Chapters
| Chapter Name | Tropics |
|---|---|
| পরিমাপ | পরিমাপ ও একক বিভিন্ন মাপের একক মাত্রা পরিমাপ |
| বল ও গতি | স্থিতি ও গতি গতির সমীকরণ নিউটনের প্রথম গতিসূত্র নিউটনের দ্বিতীয় গতি সূত্র নিউটনের তৃতীয় গতিসূত্র বিভিন্ন ধরনের বল রৈখিক ভরবেগ রৈখিক ভরবেগ সংরক্ষণ |
| পদার্থ : গঠন ও ধর্ম | তরল ও বায়ুর চাপ আর্কিমিডিসের নীতি পৃষ্ঠটান সান্দ্রতা বার্নোলির নীতি স্থিতিস্থাপকতা |
| পদার্থ : পরমাণুর গঠন ও পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ | পরমাণুর গঠন মোলের ধারণা দ্রবণ অ্যাসিড, ক্ষার, লবণ মিশ্রণের উপাদানের পৃথকীকরণ জল |
| শক্তির ক্রিয়া , কার্য, ক্ষমতা | শক্তির ক্রিয়া , কার্য, ক্ষমতা |
| তাপ | ক্যালোরিমিতি কার্য ও তাপের তুল্যতা লীনতাপ সম্পৃক্ত ও অসম্পৃক্ত বাষ্প জলের ব্যতিক্রান্ত প্রসারণ |
| শব্দ | শব্দের উৎস : কম্পন শব্দের বিস্তার : তরঙ্গ শব্দের কয়েকটি ধর্ম শব্দের বৈশিষ্ট্য মানুষের কান ও শব্দ শোনার কৌশল শব্দদূষণ |
আজকের আর্টিকেলে আমরা নবম শ্রেণির ভৌতবিজ্ঞান বইয়ের চতুর্থ অধ্যায় “পদার্থ : পরমাণুর গঠন ও পদার্থের ভৌত ও রাসায়নিক ধর্মসমূহ” এর “জল” থেকে পরীক্ষায় আসা গুরুত্বপূর্ণ প্রশ্ন ও উত্তরগুলো আলোচনা করেছি। এই প্রশ্নোত্তরগুলো নবম শ্রেণির বার্ষিক পরীক্ষা, এমনকি চাকরি বা যেকোনো প্রতিযোগিতামূলক পরীক্ষার জন্যও উপযোগী। কারণ, এই অধ্যায়ের প্রশ্ন প্রায়ই বিভিন্ন পরীক্ষায় কমন আসে।
আশা করি, এই আর্টিকেলটি আপনাদের পরীক্ষার প্রস্তুতিতে কিছুটা হলেও সাহায্য করবে। যদি কোনো প্রশ্ন, মতামত বা সাহায্যের প্রয়োজন হয়, নিচে কমেন্ট করে জানাতে পারেন কিংবা টেলিগ্রামে যোগাযোগ করুন—আপনাদের প্রশ্নের উত্তর দিতে আমি সর্বদা প্রস্তুত।
ধন্যবাদ সবাইকে।






Leave a Comment