নমস্কার বন্ধুরা! এই আর্টিকেলটিতে আমরা মাধ্যমিক পরীক্ষার জন্য অত্যন্ত গুরুত্বপূর্ণ বিষয় ভৌত বিজ্ঞানের উপরে আলোচনা করবো। বিশেষ করে, আমরা ২০১৭ সালের মাধ্যমিক ভৌত বিজ্ঞান প্রশ্নপত্র এবং সেই প্রশ্নের উত্তর নিয়ে বিস্তারিত আলোচনা করবো।

‘ক’ বিভাগ
1. বহু বিকল্পভিত্তিক প্রশ্ন। প্রতিটি প্রশ্নের নীচে চারটি করে বিকল্প উত্তর দেওয়া আছে। যেটি ঠিক সেটি লেখো :
1.1 নীচের কোনটি গ্রিনহাউস গ্যাস নয়?
(a) মিথেন
(b) জলীয় বাষ্প
(c) কার্বন ডাইঅক্সাইড
(d) অক্সিজেন
উত্তর : (d) অক্সিজেন
1.2 নীচের কোনটি চাপের SI একক?
(a) NM2
(b) Nm-2
(c) Nm
(d) N
উত্তর : (b) Nm-2
1.3. একটি গ্যাসের বাষ্পঘনত্ব 32; নীচের কোনটি গ্যাসটির আণবিক ওজন?
(a) 8
(b) 16
(c) 32
(d) 64
উত্তর : (d) 64
1.4 নীচের কোনটির ওপর ধাতুর পরিবাহিতাঙ্ক নির্ভর করে?
(a) উষ্ণতা
(b) দৈর্ঘ্য
(c) উপাদানের প্রকৃতি
(d) প্রস্থচ্ছেদ
উত্তর : (c) উপাদানের প্রকৃতি
1.5 দর্পণের বক্রতা ব্যাসার্ধ এবং ফোকাস দৈর্ঘ্যের মধ্যে সম্পর্কটি কী?
(a) f = 2r
(b) f = \(\frac r2\)
(c) f = \(\frac r3\)
(d) f = \(\frac32\)r
উত্তর : (b) f = \(\frac r2\)
1.6 প্রিজমের মধ্যে দিয়ে সাদা আলো প্রতিসরণের ক্ষেত্রে যে বর্ণের বিচ্যুতি সর্বাধিক সেটি কোনটি?
(a) লাল
(b) হলুদ
(c) বেগুনি
(d) সবুজ
উত্তর : (c) বেগুনি
1.7 নিম্নলিখিত ভৌত রাশিগুলির মধ্যে অ্যাম্পিয়ার কোনটি?
(a) কুলম্ব.সেকেন্ড
(b) ভোল্ট.ওহম-1
(c) ভোল্ট.ওহম
(d) ভোল্ট-1.ওহম
উত্তর : (b) ভোল্ট.ওহম-1
1.8 নীচের কোনটির রোধাঙ্ক উষ্ণতা বৃদ্ধির সাথে হ্রাস পায়?
(a) পরিবাহী
(b) অর্ধপরিবাহী
(c) অতিপরিবাহী
(d) অন্তরক
উত্তর : (b) অর্ধপরিবাহী
1.9 নীচের কোনটি α, β ও রশ্মির আয়নায়ন ক্ষমতার সঠিক ক্রম?
(a) α > β > γ
(b) α > γ > β
(c) γ > β > α
(d) β > α > γ
উত্তর : (a) α > β > γ
1.10 নীচের কোনটির পারমাণবিক ব্যাসার্ধ সর্বাধিক?
(a) K
(b) H
(c) Li
(d) Na
উত্তর : (a) K
1.11 নীচের কোনটিতে সমযোজী বন্ধন বর্তমান?
(a) হাইড্রোজেন ক্লোরাইড
(b) সোডিয়াম ক্লোরাইড
(c) লিথিয়াম হাইড্রাইড
(d) ক্যালশিয়াম অক্সাইড
উত্তর : (a) হাইড্রোজেন ক্লোরাইড
1.12 নীচের কোনটি জলীয় দ্রবণে একটি মৃদু তড়িৎবিশ্লেষ্য?
(a) CH3COOH
(b) NaOH
(c) H2SO4
(d) NaCl
উত্তর : (a) CH3COOH
1.13 নীচের কোনটি আর্দ্র অ্যামোনিয়াকে শুষ্ক করতে ব্যবহৃত হয়?
(a) গাঢ় H2SO4
(b) P2O3
(c) CaO
(d) CaCl2
উত্তর : (c) CaO
1.14 নীচের কোনটি অ্যালুমিনিয়াম ধাতুর আকরিক?
(a) বক্সাইট
(b) হেমাটাইট
(c) ম্যালাকাইট
(d) চ্যালকোপাইরাইটস
উত্তর : (a) বক্সাইট
1.15 নীচের কোনটি অ্যালডিহাইডের কার্যকরী গ্রুপ?
(a) -OH
(b) -CHO
(c) >C = O
(d) -COOH
উত্তর : (b) – CHO
‘খ’ বিভাগ
2. নিম্নলিখিত প্রশ্নগুলির উত্তর দাও (বিকল্প প্রশ্নগুলি লক্ষণীয়)।
2.1 শূন্যস্থান পূরণ করো –
2.1 ট্রপোস্ফিয়ারে উচ্চতা বাড়ার সঙ্গে উষ্ণতা_______।
উত্তর : কমতে থাকে।
অথবা
ভূ-উষ্ণতা বৃদ্ধির একটি ক্ষতিকর প্রভাব উল্লেখ করো।
উত্তর : ভূ-উষ্ণতা বাড়ায় মেরুর বরফ গলে সমুদ্রপৃষ্ঠ বাড়ছে। ফলে উপকূলীয় এলাকা, যেমন বাংলাদেশ, ভারত – জলমগ্ন হচ্ছে। লবণাক্ত জল কৃষি জমিতে ঢুকে ফসল উৎপাদন কমাচ্ছে। সমুদ্রপৃষ্ঠের উচ্চতা রোধে গ্রিনহাউস গ্যাস কমাতে হবে।
2.2 UV রশ্মির প্রভাবে ক্লোরোফ্লুয়োরোকার্বন থেকে নির্গত কোন পরমাণুটি ওজোন গ্যাসকে অক্সিজেনে বিয়োজিত করে দেয়?
উত্তর : ক্লোরিন গ্যাস।
নীচের বিবৃতিটি সত্য না মিথ্যা লেখো –
2. 3 একই উষ্ণতা ও চাপে সমআয়তন CO2 ও N2 গ্যাসের মধ্যে অণুর সংখ্যা পৃথক।
উত্তর : মিথ্যা।
2.4 বয়েলের সূত্র অনুষারে অপরিবর্তিত উষ্ণতায় নির্দিষ্ট ভরের কোনো গ্যাসের চাপ ও আয়তনের মধ্যে সম্পর্কটি লেখো।
উত্তর : বয়েলের সূত্র অনুষারে অপরিবর্তিত উষ্ণতায় নির্দিষ্ট ভরের কোনো গ্যাসের চাপ ও আয়তনের মধ্যে সম্পর্কটি হল –
PV = ধ্রুবক।
2.5 তরলের আপাত ও প্রকৃত প্রসারণ গুণাঙ্কের মধ্যে কোনটি তরলের নিজস্ব বৈশিষ্ট্য?
উত্তর : তরলের আপাত ও প্রকৃত প্রসারণ গুণাঙ্কের মধ্যে তরলের প্রকৃত প্রসারণ গুণাঙ্ক হল তরলের নিজস্ব বৈশিষ্ট্য।
অথবা
তাপ পরিবাহিতাঙ্কের SI একক কী?
উত্তর : তাপ পরিবাহিতাঙ্কের SI একক হল – W.m-1.k-1
2.6 আলোকের বিচ্ছুরণের একটি প্রাকৃতিক উদাহরণ দাও।
উত্তর : আলোকের বিচ্ছুরণের একটি প্রাকৃতিক উদাহরণ হল – রামধনু।
2.7 কোন ধরনের লেন্সের দ্বারা হ্রস্বদৃষ্টির প্রতিকার করা যায়?
উত্তর : অবতল লেন্সের দ্বারা হ্রস্বদৃষ্টির প্রতিকার করা যায়।
2.8 যদি তড়িৎপ্রবাহের অভিমুখ বিপরীত করা হয় তাহলে বার্লোচক্রের গতিতে কী পরিবর্তন ঘটবে?
উত্তর : যদি তড়িৎ প্রবাহের অভিমুখ পরিবর্তন করা হয়, তাহলে বলোচক্র বিপরীত দিকে ঘুরবে। কারণ, তড়িৎ প্রবাহের অভিমুখ পরিবর্তনের ফলে বলোচক্রের চারপাশে তৈরি চৌম্বক ক্ষেত্রের দিকও পরিবর্তিত হবে। এই পরিবর্তিত চৌম্বক ক্ষেত্র বলোচক্রের উপর বিপরীত দিকে বল প্রয়োগ করবে, যার ফলে বলোচক্র বিপরীত দিকে ঘুরতে শুরু করবে।
2.9 1 কুলম্ব আধানকে 1 ভোল্ট বিভব প্রভেদের বিরুদ্ধে নিয়ে যেতে কত কার্য করতে হবে?
উত্তর : 1 কুলম্ব আধানকে 1 ভোল্ট বিভব প্রভেদের বিরুদ্ধে নিয়ে যেতে 1 জুল কার্য করতে হবে।
2.10 তেজস্ক্রিয় পরমাণুর কোন অংশ থেকে β কণা নির্গত হয়?
উত্তর : তেজস্ক্রিয় পরমাণুর নিউক্লিয়াস অংশ থেকে β কণা নির্গত হয়।
অথবা
\(\frac{238}{92}\)U থেকে α কণা নিঃসরণের ফলে যে মৌলটি উৎপন্ন হয় তার পারমাণবিক সংখ্যা কত?
উত্তর : \(\frac{238}{92}\)U থেকে α কণা নিঃসরণের ফলে যে মৌলটি উৎপন্ন হয় তার পারমাণবিক সংখ্যা 90
2.11 বামস্তম্ভের সঙ্গে ডানস্তম্ভের সামঞ্জস্য বিধান করো-
| 2.11.1 একটি সন্ধিগত মৌল | (a) অ্যালুমিনিয়াম |
| 2.11.2 একটি ইউরেনিয়ামোত্তর মৌল | (b) নিকেল |
| 2.11.3 থার্মিট পদ্ধতিতে উচ্চ উষ্ণতায় Fe2O3-কে বিজারিত করে | (c) টিন |
| 2.11.4 ধাতু সংকর কাঁসাতে উপস্থিত | (d) প্লুটোনিয়াম |
উত্তর :
| 2.11.1 একটি সন্ধিগত মৌল | 2.11.2 (b) নিকেল |
| 2.11.2 একটি ইউরেনিয়ামোত্তর মৌল | 2.11.4 (d) প্লুটোনিয়াম |
| 2.11.3 থার্মিট পদ্ধতিতে উচ্চ উষ্ণতায় Fe2O3-কে বিজারিত করে | 2.11.1 (a) অ্যালুমিনিয়াম |
| 2.11.4 ধাতু সংকর কাঁসাতে উপস্থিত | 2.11.3 (c) টিন |
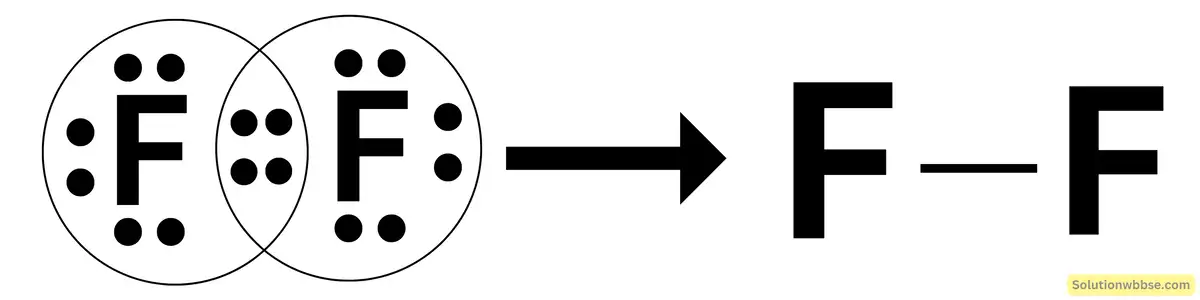
2.12 F2 অণুর লুইস ডট চিত্র অঙ্কন করো। (F = 9)
উত্তর : দেওয়া আছে, F = 9 ∴ 1s1 2s2 2p5
F2 = 7 × 2 = 14
2.13 বিশুদ্ধ জলে অল্প পরিমাণ সালফিউরিক অ্যাসিড যোগ করলে উৎপন্ন দ্রবণের, তড়িৎ পরিবাহিতা বিশুদ্ধ জলের থেকে বেশি হয় কেন?
উত্তর : জলের বেশির ভাগ অনু বিয়োজিত হয়ে বেশি সংখ্যক H+ ও OH– আয়ন উৎপন্ন করে। তাই দ্রব্যের তড়িৎ পরিবাহিতা বেশি হয়।
অথবা
কোনো তড়িৎ বিশ্লেষ্যের জলীয় দ্রবণের তড়িৎ বিশ্লেষণের সময় দ্রবণে তড়িতের বাহক কারা?
উত্তর : কোনো তড়িৎ বিশ্লেষ্যের জলীয় দ্রবণের তড়িৎ বিশ্লেষণের সময় দ্রবণে তড়িতের বাহক আয়ন।
2.14 Cu-তড়িৎদ্বার ব্যবহার করে CuSO4, এর জলীয় দ্রবণের তড়িৎ বিশ্লেষণে কোন আয়ন ক্যাথোডের দিকে ধাবিত হয়?
উত্তর : Cu-তড়িৎদ্বার ব্যবহার করে CuSO4, এর জলীয় দ্রবণের তড়িৎ বিশ্লেষণে Cu2+ আয়ন ক্যাথোডের দিকে ধাবিত হয়।
2.15 লেড নাইট্রেটের জলীয় দ্রবণে H2S গ্যাস চালনা করলে যে কালো রঙের অধঃক্ষেপ পড়ে তার সংকেত লেখো।
উত্তর : লেড নাইট্রেটের জলীয় দ্রবণে H2S গ্যাস চালনা করলে যে কালো রঙের অধঃক্ষেপ পড়ে তার সংকেত হল PbS।
অথবা
আম্লিক পটাশিয়াম ডাইক্রোমেটের জলীয় দ্রবণে H2S গ্যাস চালনা করলে বর্ণের কী পরিবর্তন হয়?
উত্তর : আম্লিক পটাশিয়াম ডাইক্রোমেটের জলীয় দ্রবণে H2S গ্যাস চালনা করলে দ্রবনের বর্ণ সবুজ হয়।
2.16 ইউরিয়া উৎপাদনে দুটি পদার্থ ব্যবহৃত হয়। একটি অ্যামোনিয়া, অপরটি কী?
উত্তর : ইউরিয়া উৎপাদনে দুটি পদার্থ ব্যবহৃত হয়। একটি অ্যামোনিয়া, অপরটি কার্বন ডাই অক্সাইড।
2.17 পলি (ভিনাইল ক্লোরাইড) এর একটি ব্যবহার উল্লেখ করো।
উত্তর : পলি (ভিনাইল ক্লোরাইড) এর একটি ব্যবহার হল – বৈদ্যুতিক তার, তুলা বা লিনেন দিয়ে ক্যানভাস তৈরিতে ব্যবহার করা হয়।
2.18 CH3CH2CH2OH -এর IUPAC নাম লেখো।
উত্তর : CH3CH2CH2OH -এর IUPAC নাম হল – প্রোপান – 1 – অল।
অথবা
CH3CH2OH -এর একটি সমাবয়বের গঠন সংকেত লেখো।
উত্তর : CH3-O-CH3 (ডাইমিথাইল ইথার) এবং CH3-CH2-OH (ইথাইল অ্যালকোহল) দুটি ভিন্ন যৌগ, কিন্তু তাদের আণবিক সংকেত C2H6O একই। এই দুটি ভিন্ন যৌগের মধ্যে কার্যকরী মূলক ঘটিত সমবয়বতা দেখা যায়।

‘গ’ বিভাগ
3. নিম্নলিখিত প্রশ্নগুলির উত্তর দাও (বিকল্প প্রশ্নগুলি লক্ষণীয়)
3.1 কোনো জ্বালানীর তাপনমূল্য বলতে কী বোঝায়? কয়লা ও ডিজেলের মধ্যে কোনটির তাপনমূল্য বেশি?
উত্তর : কোনো জ্বালানির তাপনমূল্য হলো ১ কেজি ভরের সেই জ্বালানি পুরোপুরিভাবে দহন করলে যে পরিমাণ তাপশক্তি উৎপন্ন হয়। তাকে জ্বালানির তাপনমূল্য বলে।
এবং কয়লা ও ডিজেলের মধ্যে ডিজেলের তাপনমূল্য বেশি।
3.2 STP-তে নিদিষ্ট ভরের কোনো গ্যাসের আয়তন 52m3 হলে অপরিবর্তিত উষ্ণতায় 104cmHg চাপে গ্যাসটির আয়তন কত হবে?
উত্তর : গ্যাসের প্রাথমিক চাপ (P1) = 76cm Hg
গ্যাসের প্রাথমিক আয়তন (V1) = 52cm3
গ্যাসের অন্তিম চাপ (P2) = 104 Cm Hg
গ্যাসের অন্তিম আয়তন (V2) = ?
যেহেতু গ্যাসের উষ্ণতা ও ভর অপরিবর্তিত তাই বয়েলের সূত্রানুযায়ী,
∴ P1V1 = P2V2
বা, 76 × 52 = 104 × V2
বা, \(V_2=\frac{\left(76\times52\right)}{104}\)
বা, V2 = 38m3
∴ গ্যাসটির অন্তিম আয়তন 38cm³।
অথবা
4 অ্যাটমস্ফিয়ার চাপে ও 300k উষ্ণতায় 8g H2 গ্যাসের (H = 1) আয়তন কত হবে? (K = 0.082 লিটার অ্যাটমস্ফিয়ার মোল-1 K-1)
উত্তর : গ্যাসটির প্রাথমিক চাপ (P) = 4 atm
গ্যাসটির প্রাথমিক উষ্ণতা (T) = 300K
গ্যাসের ভর (W) = 8 গ্রাম
গ্যাসের আণবিক ভর (H2 গ্যাসের) (M) = 1
মোলার গ্যাস ধ্রুবক (R) = 0.082 লিটার আটস্ফিয়ার মোল-1 K-1
গ্যাসটির আয়তন (V) =?
এখন PV = \(\left(\frac WM\right)\) RT সূত্র থেকে পাই,
বা, 4 × V = \(\left(\frac81\right)\) × 0.082 × 300
বা, V = \(\frac{8\times0.082\times300}4\)
বা, V = 49.2
∴ গ্যাসটির আয়তন 49.2 লিটার।
3.3 কোনো মাধ্যমের প্রতিসরাঙ্ক আলোর বেগের ওপর কীভাবে নির্ভর করে?
উত্তর : আলো একটি বেগের গতি যা বিভিন্ন মাধ্যমে প্রতিসরাঙ্ক বা প্রতিভাবের সাথে সম্পর্কিত। যদি আলো একটি মাধ্যমে বেগের অনেক বেশি হয়, তাহলে সে মাধ্যমে প্রতিসরাঙ্ক কম হবে। অন্যদিকে, যদি আলো মাধ্যমে বেগ কম হয়, তাহলে প্রতিসরাঙ্ক বেশি হবে। অর্থাৎ, মাধ্যমের আলোর গতি বাড়লে প্রতিসরাঙ্ক কম হয় এবং গতি কমলে প্রতিসরাঙ্ক বেড়ে। অর্থাৎ কোনো মাধ্যমে আলোর বেগের সাথে প্রতিসরাঙ্কের ব্যাস্তানুপাতিক সম্পর্ক।
অথবা
গাড়ির হেডলাইটে কী ধরনের দর্পণ ব্যবহার করা হয় ও কেন?
উত্তর : গাড়ির হেডলাইটে ব্যবহৃত দর্পণ হল ধাতব অবতল দর্পণ।
এই ধাতব অবতল দর্পণ ব্যবহার করা হয় কারণ গাড়ির হেডলাইটের বাতিটি দর্পণের ফোকাসে রাখা হয় যাতে বাতি থেকে নির্গত আলোকরশ্মি অবতল প্রতিফলকে প্রতিফলিত হয় এবং সমান্তরাল রশ্মিগুচ্ছে পরিণত হয়। এর ফলে আলোর রশ্মি দূর পর্যন্ত ছড়ায় এবং গাড়ির চালকের খুব সুবিধা হয়।
3.4 ভাস্বর বাতি ব্যবহারের চেয়ে CFL বাতি ব্যবহারের দুটি সুবিধা উল্লেখ করো।
উত্তর : ভাস্বর বাতি ব্যবহারের চেয়ে CFL বাতি ব্যবহারের দুটি সুবিধা –
(i) ভাস্বর বাতিতে প্রায় 98% তাপ শক্তির রূপান্তর হয় এবং অল্প পরিমাণে দৃশ্যমান আলো উৎপন্ন হয়, যেটি অন্যান্য কাজে ব্যয় হয় না।
(ii) ভাস্বর ল্যাম্পের তুলনায়, CFL বাতি দাম বেশি হতে পারে কিন্তু এটি অনেক বেশি দৃশ্যমান আলো উৎপন্ন করে এবং তার ব্যবহারের খরচ কমে। তাই দামের বিপরীতে কিছু সময় পরে এটি মূল্যবান ব্যবস্থাপনা হতে পারে।
3.5 চিনির জলীয় দ্রবণ তড়িৎ পরিবহন করতে পারে না, কিন্তু সোডিয়াম ক্লোরাইডের জলীয় দ্রবণ পারে। কেন?
উত্তর : সোডিয়াম ক্লোরাইড (NaCl) একটি আয়নিক যৌগ এবং জলে NaCl এর মিশ্রণের ফলে Na+ এবং Cl– আয়ন মুক্ত হয়। এই আয়নগুলি তড়িৎ চালনা করতে সক্ষম, যা মানে সোডিয়াম ক্লোরাইড জল তড়িৎ পরিবহণ করতে পারে। অন্যদিকে, চিনি বা গ্লুকোজের অণুগুলি জলে আয়নিত হয় না, তাই তারা জলের মধ্যে তড়িৎ চালনা করতে পারে না।
অথবা
সোডিয়াম ক্লোরাইডের ক্ষেত্রে আণবিক ওজনের বদলে সাংকেতিক ওজন কথাটি ব্যবহার করা সঙ্গত কেন?
উত্তর : সোডিয়াম ক্লোরাইড একটি ধরনের আয়নীয় যৌগ। এই যৌগে, আয়নগুলি একে অপরকে আকর্ষণ করে মিলিত থাকে। আয়নীয় যৌগ হলে অণুর অস্তিত্ব নেই, অর্থাৎ তারা একটি নির্দিষ্ট ধরনের অণুর মতো স্থায়ী আকার ধারণ করে। তাই আয়নীয় যৌগের ক্ষেত্রে, সাংকেতিক ওজন ব্যবহার করা হয়। অর্থাৎ সোডিয়াম ক্লোরাইডের আয়নিক ওজন 58.5 নয়, পরিবর্তে সাংকেতিক ওজন 58.5 হয়।
3.6 ন্যাপথালিন ও সোডিয়াম ক্লোরাইডের নীচের দুটি ধর্মের তুলনা করো – গলনাঙ্ক ও জলে দ্রাব্যতা।
উত্তর : ন্যাপথালিন ও সোডিয়াম ক্লোরাইডের নীচের দুটি ধর্মের তুলনা হল –
(i) সোডিয়াম ক্লোরাইড একটি পরিষ্কার দ্রব্য এবং ন্যাপথালিন একটি গ্যাসীয় পদার্থ। সোডিয়াম ক্লোরাইডের গলনাঙ্ক ন্যাপথালিনের থেকে অনেক বেশি।
(ii) সোডিয়াম ক্লোরাইড একটি আয়নীয় যৌগ এবং ন্যাফথালিন একটি সমযোজী যৌগ। এই কারণে সোডিয়াম ক্লোরাইড পানি জলে দ্রাব্য হয় কিন্তু ন্যাফথালিন জলে দ্রাব্য হয় না। অতএব, সোডিয়াম ক্লোরাইড হতে দ্রাব্যতা উপভোগ করা যায় কিন্তু ন্যাফথালিন হতে না।
3.7 কিপযন্ত্রে প্রস্তুত করা যায় এমন একটি গ্যাসের নাম করো। গ্যাসটি প্রস্তুতির বিক্রিয়ার সমিত রাসায়নিক সমীকরণ লেখো।
উত্তর : কিপযন্ত্রে প্রস্তুত করা যায় এমন একটি গ্যাসের নাম হল – H2S।
কিপযন্ত্রে প্রস্তুত হাইড্রোজেন সালফাইড (H2S) তৈরির রাসায়নিক সমীকরণ হল – FeS + H2SO4 → FeSO4 + H2S↑
3.8 জিঙ্ক অক্সাইড থেকে কীভাবে জিঙ্ক ধাতু পাওয়া যায়? বিক্রিয়াটি সমিত রাসায়নিক সমীকরণ সহ লেখো।
উত্তর : জিঙ্ক অক্সাইড (ZnO) এর সাথে অতিরিক্ত কোক চূর্ণ ভালোভাবে মিশিয়ে মিশ্রণ তৈরি করা হয়। এই মিশ্রণটি অগ্নিসহ মাটিতে রাখা হয়, এবং 1300-1400°C উষ্ণতায় উত্তপ্ত করা হয়। এর ফলে জিঙ্ক অক্সাইড থেকে ধাতব জিঙ্ক উদ্ভাবিত হয় এবং কার্বন মনক্সাইড (CO) গ্যাস উৎপন্ন হয়। এই প্রক্রিয়ায় বিজারক হিসাবে কোক চূর্ণ ব্যবহার করা হয়।
বিক্রিয়াটির সমিত রাসায়নিক সমীকরণ – ZnO + C → Zn + CO↑
অথবা
CuSO4-এর জলীয় দ্রবণে জিঙ্কের একটি টুকরো যোগ করলে কী হয়? ইলেকট্রনীয় তত্ত্বের সাহায্যে দেখাও যে এটি একটি জারণ-বিজারণ বিক্রিয়া।
উত্তর : ধাতুর সক্রিয়তা সারিতে জিঙ্ক প্রথমে অবস্থিত। এবং যখন কপার সালফেটের জলীয় দ্রবণে জিঙ্কের টুকরো ফেলা হয়, তখন জিঙ্ক কপার সালফেটের জলীয় দ্রবণ থেকে কপারকে প্রতিস্থাপিত বা নিচে পাঠাবে। এই নিচে পাঠানো কপার, জিঙ্কের টুকরোর পৃষ্ঠতলে পরিস্থিত হবে এবং সে সাথে জিঙ্কের টুকরোর উপরে লালচে বাদামি রঙের ছোপ দেখা যাবে।
রাসায়নিক বিক্রিয়া – ZnO + CuSO4 → ZnSO4 + Cu↓(লাল)
দ্বিতীয়ত,
রাসায়নিক বিক্রিয়া – Zn + CuSO4 → ZnSO4 + Cu↓(লাল)
বিজারণ বিক্রিয়া – Cu2+ + 2e- → Cu
জারণ বিক্রিয়া – Zn → Zn2+ + 2e-
এই বিক্রিয়া থেকে আমরা জানতে পারি যে, কপার জারণের স্তর (+2) থেকে (0) স্তরে আসে এবং জিঙ্ক জারণের স্তর (0) থেকে (+2) স্তরে পৌঁছে। সুতরাং, কপার একটি জারক দ্রব্য এবং জিঙ্ক বিজারক দ্রব্য। অর্থাৎ এটি একটি জারণ-বিজারণ বিক্রিয়া।
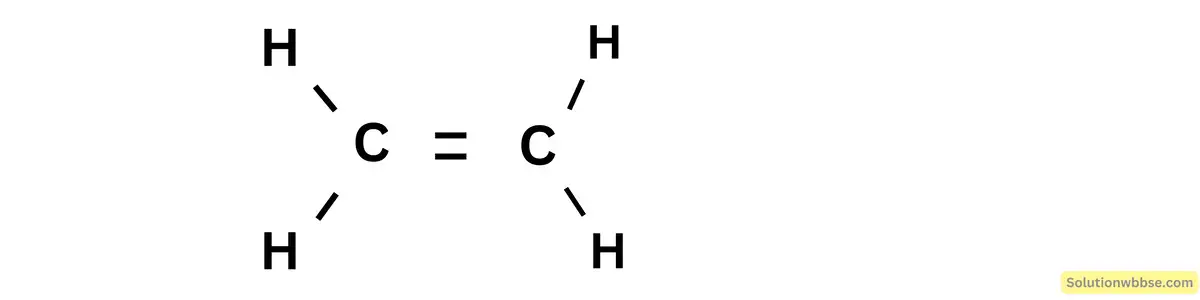
3.9 ইথিলিন-এর গঠন সংকেতের সাহায্যে দেখাও যে এটি একটি অসম্পৃক্ত হাইড্রোকার্বন।
উত্তর : ইথিলিন হল এক ধরনের হাইড্রোকার্বন, যা কার্বন এবং হাইড্রোজেন মিশ্রণ দ্বারা তৈরি হয়। এটি হাইড্রোকার্বনের একটি বিশেষ ধরন, যেখানে কার্বন এবং হাইড্রোজেন মধ্যে একাধিক বন্ধন রয়েছে। C2H4 বা ইথিলিনে, দুটি কার্বন পরমাণু নিজেদের মধ্যে একটি বন্ধন গঠন করে এবং প্রতিটি কার্বন পরমাণুর সাথে দুটি হাইড্রোজেন পরমাণু বন্ধন গঠন করে। এটি ইথিলিনকে একটি বিশেষ ধরনের অসম্পৃক্ত হাইড্রোকার্বন করে।
অথবা
ডিনেচার্ড স্পিরিট’ কী?
উত্তর : ডিনেচার্ড স্পিরিট হল এমন একটি মিশ্রণ যা ইথাইল অ্যালকোহলের মধ্যে মিথাইল অ্যালকোহল (প্রায় 10%) এবং কিছু উৎকট স্বাদযুক্ত পদার্থ, যেমন – পিরিডিন, কপার সালফেট, ন্যাপথা ইত্যাদির মিশ্রণ থাকে। এই মিশ্রণকে মেথিলেটেড স্পিরিট বা ডিনেচার্ড স্পিরিট বলা হয়।
‘ঘ’ বিভাগ
4. নিম্নলিখিত প্রশ্নগুলির উত্তর দাও (বিকল্প প্রশ্নগুলি লক্ষণীয়)
4.1 গ্যাস সংক্রান্ত চার্লস সূত্রটি বিবৃত করো এবং সূত্রটিকে লেখচিত্রের (V বনাম t) সাহায্যে প্রকাশ করো।
উত্তর : গ্যাস সংক্রান্ত চার্লসের সূত্রটি হল –
স্থির চাপে নির্দিষ্ট ভরের কোন গ্যাসের আয়তন প্রতি ডিগ্রি সেলসিয়াস তাপমাত্রা বাড়ানো বা কমানোর ফলে 0°C তাপমাত্রায় তার আয়তনের \(\frac1{273}\) ভাগ হারে যথাক্রমে বাড়বে বা কমবে।
যখন আমরা একটি গ্যাস নিয়ে কাজ করছি এবং তার চাপ স্থির রয়েছে, এবং গ্যাসের ভর নির্দিষ্ট আছে, তখন যদি আমরা গ্যাসের উষ্ণতা (t) এবং তার আয়তন (V) এর মান লিখতে চাই, তবে সে লেখচিত্র একটি সরলরেখা হবে।

4.2 অ্যামোনিয়াম সালফেটকে কস্টিক সোডা দ্রবণসহ উত্তপ্ত করে 6.8g অ্যামোনিয়া উৎপন্ন করতে কত গ্রাম অ্যামোনিয়াম সালফেট প্রয়োজন হবে? (H = 1, N = 14, O = 16, S = 32)
উত্তর : 2NaOH (aq) + (NH4)2SO4 (aq) → 2NH3(aq) + Na2SO4 (aq) + 2H2O (I)
(NH4)2SO4 -এর আণবিক ভর – (14 × 2) + (8 × 1) + 32 + (4 × 16) = 132
NH3 –এর আণবিক ভর – 14 + (3 × 1)
= 14 + 3
= 17
∴ (2 × 17) = 34 গ্রাম অ্যামোনিয়া প্রস্তুত করতে 132 গ্রাম অ্যামোনিয়াম সালফেট প্রয়োজন।
∴ 6.8 গ্রাম অ্যামোনিয়া প্রস্তুত করতে \(\frac{(132\times6.8)}{34}\) গ্রাম অ্যামোনিয়াম সালফেট প্রয়োজন
= 26.4 গ্রাম অ্যামোনিয়াম সালফেট প্রয়োজন।
অথবা
CaCO3-এর সঙ্গে লঘু HCl-এর বিক্রিয়ায় CaCl2, CO2 ও H2O উৎপন্ন হয়। 50.0 g CaCO, থেকে 55.5g CaCl2, 22.0g CO2 ও 9.0g H2O উৎপন্ন করতে কত গ্রাম HCl-এর প্রয়োজন হবে? প্রয়োজনীয় HCl এর মোল সংখ্যা কত? (H = 1, Cl = 35.5)
উত্তর : প্রথমে, বিক্রিয়ার সমীকরণটি সমতায় আনতে হবে
CaCO3 (s) + 2HCl (aq) → CaCl2 (aq) + CO2 (g) + H2O (l)
মোলার ভর গণনা
প্রতিটি যৌগের মোলার ভর নির্ধারণ করতে হবে,
CaCO3 =100 g/mol
HCl = 36.5 g/mol (H = 1, Cl = 35.5)
CaCl2 = 122 g/mol
CO2 = 44 g/mol
H2O = 18 g/mol
মোল গণনা
প্রদত্ত ভরের প্রতিটি যৌগের মোল সংখ্যা নির্ধারণ করতে হবে:
CaCO3 = 50.0 g/100 g/mol = 0.50 mol
CaCl2 = 55.5 g/122 g/mol = 0.455 mol
CO2 = 22.0 g/44 g/mol = 0.50 mol
H2O = 9.0 g/18 g/mol = 0.50 mol
মোলার অনুপাত ব্যবহার
সমীকরণ অনুযায়ী, 1 mol CaCO3 2mol HCl তৈরি করে।
তাই, 0.50 mol CaCO3 এর জন্য HCl এর প্রয়োজনীয় মোল সংখ্যা
0.50 mol CaCO3 (2 mol HCl/1 mol CaCO3) = 1.00 mol HCl
HCl এর ভর গণনা
প্রয়োজনীয় HCl এর ভর নির্ধারণ করতে হবে
1.00 mol HCl = 36.5 g/mol = 36.5 g HCl
∴ 50.0 g CaCO3 থেকে 55.5 g CaCl2, 22.0 g CO2 ও 9.0 g H2O উৎপন্ন করতে 36.5 g HCl প্রয়োজন।
প্রয়োজনীয় HCl এর মোল সংখ্যা 1.00 mol
4.3 স্থির চাপে গ্যাসের আয়তন প্রসারণ গুণাঙ্ক কাকে বলে? এর মান কত?
উত্তর : চাপ স্থির রেখে নির্দিষ্ট ভরের কোনো গ্যাসের তাপমাত্রা 0°C থেকে 1°C বৃদ্ধি পেলে গ্যাসের প্রতি একক আয়তনে যে পরিমাণ আয়তন বৃদ্ধি পায়, তাকে ওই গ্যাসের আয়তন গুণাঙ্ক বলা হয়।
তাপীয় গুণাঙ্কের মান = \(\frac1{273}^\circ C^{-1}\)
= 3.666 10-3 °C-1
অথবা
তাপ পরিবহণ ও তড়িৎ পরিবহণের মধ্যে দুটি সাদৃশ্যের উল্লেখ করো। উচ্চ তাপপরিবাহিতা বিশিষ্ট একটি অধাতুর নাম করো।
উত্তর : তাপ পরিবহন এবং তড়িৎ পরিবহনের মধ্যে একইভাবে সমানতা রয়েছে –
(i) যখন কোনও পরিবাহীর দুটি প্রান্তে বিভব প্রভেদ নেই তখন তড়িৎ প্রবাহ ঘটে না, এমনই যেমন কোনও ধাতব ফলকের দুটি বিপরীত পৃষ্ঠের মধ্যে তাপমাত্রার পার্থক্য নেই তখন তাপ পরিবহন ঘটে না।
(ii) একইভাবে কোনও পদার্থের মধ্যে তাপ প্রবাহের সময় তাপীয় রোধ সৃষ্টি হয় তেমনই যেমন কোনও পরিবাহীর মধ্যে তড়িৎ প্রবাহের সময় পরিবাহীর রোধ সৃষ্টি হয়।
(iii) তাপ পরিবহনের অপরদিকে থাকলেও এটি একটি স্কেলার রাশি হয়, আর তড়িৎ প্রবাহের অপরদিকে থাকলেও এটি স্কেলার রাশি হয়।
উচ্চ তাপপরিবাহিতা বিশিষ্ট একটি অধাতুর নাম হল হীরা।
4. 4 আলোকের প্রতিসরণ সংক্রান্ত সূত্র দুটি বিবৃত করো। দ্বিতীয় সূত্রের গানিতিক রুপটিও লেখো।
উত্তর : আলোর প্রতিবিবর্তনের সূত্র দুটি এমন –
(i) আপাত রশ্মি, প্রতিস্থাপিত রশ্মি এবং আপাতন বিন্দুতে দুই মাধ্যমের প্রতিবেদনকে পৃষ্ঠকের উপর চিহ্নিত লম্বদিকের সাথে একই সমতলে থাকে।
(ii) দুটি নির্দিষ্ট মাধ্যম এবং নির্দিষ্ট বর্ণের আলোর প্রতিবিবর্তনের ক্ষেত্রে, আপাতন কোণের সাইনের অনুপাত ধ্রুবক।
4.5 অবতল দর্পণের ক্ষেত্রে ফোকাস দূরত্ব ও বক্রতা ব্যাসার্ধের মধ্যে সম্পর্কটি নির্ণয় করো।
উত্তর :
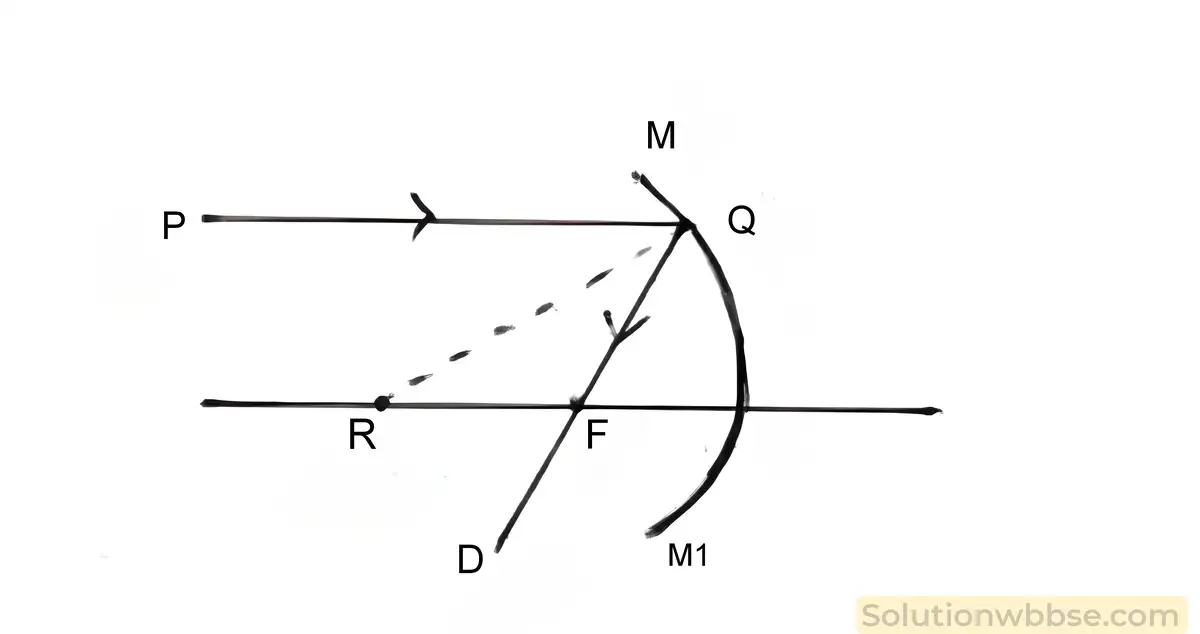
একটি ছোট উন্মেষযুক্ত অবতল দর্পন NUN1 হল প্রধান ছেদ। এখানে, U, F, এবং R প্রত্যেকেই অবতল দর্পনের মারমূল, প্রধান ফোকাস, এবং বক্রতা কেন্দ্র যথাক্রমে। ফোকাস দূরত্ব, UF = f, এবং বক্রতা ব্যাসার্ধ, UR = r। অবতল দর্পনের প্রধান অক্ষের সঙ্গে সমান্তরাল PQ আলোকরশ্মি Q বিন্দুতে দর্পনের ওপর আপাতিত হয় এবং পরবর্তী প্রতিবিবর্তনের পর ফোকাসে (f) পৌঁছায়, যা RQ লাইনের মধ্যে রয়েছে, যা R,Q এবং Q যুক্ত করে করা হয়েছে।
মনে করি, আপাতন কোণ ∠PQR = θ।
∴ প্রতিফলন কোণ, ∠FQR = θ।
আবার, PQ || RU ও QR ভেদক।
∴ ∠PQR = ∠QRF [একান্তর কোণ]
∴ ∠QRF = θ
∴ ∠QRV এর ∠FQR = ∠QRF
ΔQRF সমদ্বিবাহু ত্রিভুজ
∴ RV = FQ
যেহেতু দর্পণের উম্মেশ খুবই ক্ষুদ্র ও PQ হল উপাক্ষীয় রশ্মি, সেহেতু Q ও U বিন্দু দুটি খুবই নিকতবর্তী।
∴ VQ ≈ UF
অর্থাৎ, UF = RF
বা, UF = \(\frac{UR}2\)
বা, f = \(\frac r2\)
∴ ফোকাস দূরত্ব(f) =
অথবা
একটি আলোকরশ্মি প্রিজমের মধ্যে দিয়ে যায়। দেখাও যে চ্যুতি কোণের মান δ = i1 + i2 – A। (চিহ্নগুলি প্রচলিত অর্থে ব্যবহৃত)
উত্তর :

ABC হল A প্রতিসারক কোণ ও M প্রতিসরাঙ্ক যুক্ত একটি প্রিজমের প্রধান ছেদ যার BC ভূমি ,AB ও AC দুটি প্রতিসারক তলকে নির্দেশ করে। PQRS হল প্রিজমের মধ্য দিয়ে আলোর প্রতিসরণে আলোর গতিপথ। AB তলে আলোর প্রতিসরণে আপাতন কোণ, ∠PQM = i1 ও প্রতিসরণ কোণ, ∠RQT =r1
AB তলে আলোর প্রতিসরণে চ্যুতিকোণ, δ1 = ∠EQR = i1 – r1
AC তলে QR আপাতিত রশ্মির ক্ষেত্রে আপাতন কোণ, ∠QRT = r2 ও প্রতিসরণ কোণ ∠NRS = i2
∴ চ্যুতি কোণ, δ2 = ∠NRF = i2 – r2
PQ হল প্রিজমে আপাতিত রশ্মি এবং RS নির্গম রশ্মি। SR-কে পিছন দিকে বাড়ালে বর্ধিত SR, PE কে U বিন্দুতে ছেদ করে। সুতরাং আলোকরশ্মির Q ও R দুটি বিন্দুতে প্রতিসরণ হওয়ার জন্য চ্যুতিকোণ হয়, ∠EUR = δ
ΔUQR -এর ∠EUR হল বহিঃস্থ কোণ।
∴ ∠EUR = ∠UQR + ∠QRU
বা, ∠EUR = ∠UQR + ∠FRS [যেহেতু, ∠QRU = ∠FRS (বিপ্রতীপ কোণ)]
বা, δ = δ1 + δ2
বা, δ = i1 – r1 + i2 – r2
বা, δ = i1 + i2 -(r1 + r2)_______(i)
Δ QTR থেকে পাই, r1 + r2 + ∠QTR = 180°_______(ii)
আবার চতুর্ভুজ AQTR –এর
∠AQT + ∠ART = 90° + 90° = 180°
∴ ∠QAR + ∠QTR = 360° – 180° = 180°_______(iii)
(ii) ও (iii) নং সমীকরণ থেকে পাই,
∠QAR = r1 + r2
বা, ∠A = r1 + r2
∴ (i) নং সমীকরণ থেকে পাই, চুতিকোণ δ = i1 + i2 – A
4.6 তড়িৎ চুম্বকীয় আবেশ সংক্রান্ত ফ্যারাডের সূত্রগুলি লেখো। পরিবর্তী তড়িৎপ্রবাহ বলতে কী বোঝায়?
উত্তর : তড়িৎ চুম্বকীয় আবেশ সংক্রান্ত ফ্যারাডের সূত্রগুলি হল –
তড়িৎ চুম্বকীয় আবেশ সংক্রান্ত ফ্যারাডের প্রথম সূত্র – কোনো বদ্ধ কুণ্ডলীর সঙ্গে জড়িত চৌম্বক প্রবাহের পরিবর্তন হলে কুণ্ডলীতে তড়িৎচালক বল আবিষ্ট হয় এবং কুণ্ডলীতে তড়িৎ প্রবাহ চলে।
তড়িৎ চুম্বকীয় আবেশ সংক্রান্ত ফ্যারাডের দ্বিতীয় সূত্র – তড়িৎ চুম্বকীয় আবেশের ক্ষেত্রে আবিষ্ট তড়িৎচালক বলের মান কুণ্ডলীর সঙ্গে জড়িত চৌম্বক প্রবাহের পরিবর্তনের হারের সঙ্গে সমানুপাতিক।
পরিবর্তী তড়িৎপ্রবাহের সংজ্ঞা – যে তড়িৎ প্রবাহের দিক একটি নির্দিষ্ট পর্যায় পর পর বিপরীতমুখী হয় তাকে পরিবর্তী তড়িৎ প্রবাহ বলে।
4.7 440 ওহম রোধের বাতিকে 220 ভোল্ট মেইনসে 10 ঘন্টার জন্য যুক্ত করা হল। ব্যয়িত তড়িৎশক্তির পরিমান BOT এককে নির্ণয় করো।
উত্তর : 440 ওহম রোধের বাতিকে 220 ভোেল্ট মেইনসে 10 ঘন্টার জন্য যুক্ত করা হল,
∴ v = 220 ভোল্ট, R = 440 ওহম
∴ তড়িৎ ক্ষমতা,
P = \(\frac{V^2}R\)
বা, P = \(\frac{\left(220\right)^2}{40}\)
বা, P = 110
∴ তড়িৎ ক্ষমতা = 110 W
বাতিটি 10 ঘণ্টা চললে ব্যায়িত তড়িৎ শক্তি = (110 × 10)W = 1100Wh
∴ নির্ণেয় B.O.T = \(\frac{1100}{1000}\)
1.1 KWh বা 1.1 Β.Ο.Τ
অথবা
6 ওহম রোধের ধাতব তারকে টানা হল যাতে এর দৈর্ঘ্য প্রাথমিক দৈর্ঘ্যের দ্বিগুণ হয়। অন্তিম রোধ কত হবে?
উত্তর : মনে করি, মূল তারটির দৈর্ঘ্য = I একক ও প্রস্থচ্ছেদের ক্ষেত্রফল = A
তারের উপাদানের রোধাঙ্ক = ρ হলে তারটির রোধ , R = \(\frac{\rho I}A\) = 6 ওহম
তারটিকে টানার পর যে নতুন তার তৈরি হল তার দৈর্ঘ্য, I1 = 2
ধরা যাক, নতুন তারটির প্রস্থচ্ছেদের ক্ষেত্রফল = A
যেহেতু, তারটির আয়তন অপরিবর্তিত আছে সেহেতু,
I1A1 = A
বা, 2.A1 = A
বা, \(A_1=\frac A2\)
নতুন তারটির রোধ, \(R_1=\rho\frac{I_1}{A_1}\)
বা, \(R_1=\rho\times\frac{I}{\displaystyle\frac A2}\)
বা, \(R_1=\rho\times\frac{4I}A\)
বা, \(R_1=4\times\frac{\rho I}A\)
বা, R1 = 4R
বা, R1 = 4 × 6
বা, R1 = 24
∴ অন্তিম রোধ = 24 ওহম।
4.8 ভর ত্রুটি বলতে কী বোঝায়? নিউক্লিয় সংযোজনে যে শক্তি মুক্ত হয় তার উৎস কী?
উত্তর : ভর ত্রুটির সংজ্ঞা – যখন একটি নিউক্লিয়াস তার গঠিত প্রোটন এবং নিউট্রনের মোট ভরের সমষ্টি নিউক্লিয়াসের প্রতিবেশী গঠন থেকে কিছুটা কম হয়, তখন এই পার্থক্যকে ভর ত্রুটি বলা হয়।
নিউক্লিয় সংযোজনে যে শক্তি মুক্ত হয় তার উৎস হল ভর ত্রুটি।
4.9 মৌলসমূহের পর্যাবৃত্ত ধর্ম বলতে কী বোঝায় একটি উদাহরণ সহ লেখ। একটি ধর্মের উল্লেখ করো যেটি পর্যাবৃত্ত ধর্ম নয়।
উত্তর : পর্যায় সারণিতে সাজানো মৌলগুলো, তাদের ইলেকট্রন বিন্যাসের ভিন্নতার কারণে, বিভিন্ন ভৌত ও রাসায়নিক বৈশিষ্ট্য প্রদর্শন করে। এই বৈশিষ্ট্যগুলো, যেমন ধাতব ধর্ম, অধাতব ধর্ম, পরমাণুর আকার, গলনাঙ্ক, স্ফুটনাঙ্ক, আয়নীকরণ শক্তি, তড়িৎ ঋণাত্মকতা, ইলেকট্রন আসক্তি ইত্যাদি, পর্যায়ক্রমিকভাবে পরিবর্তিত হয়। এই ধর্মগুলোকেই মৌলসমূহের পর্যায়বৃত্ত ধর্ম বলা হয়।
পর্যায়বৃত্ত ধর্মের উদাহরণ – আয়নীভবন শক্তি, তড়িৎ ইত্যাদি।
ইলেকট্রন বিন্যাস, মৌলের পর্যায়বৃত্ত ধর্ম নয়।
অথবা
মৌলের তড়িৎঋণাত্মকতা বলতে কী বোঝায়? ওপর থেকে নীচের দিকে দীর্ঘ পর্যায় সারণির গ্রুপ 1 মৌলগুলির তড়িৎঋণাত্মকতা কীভাবে পরিবর্তিত হয়?
মৌলের তড়িৎ ঋণাত্মকতা হলো অন্য কোনো মৌলের পরমাণুর সাথে সমযোজী বন্ধন গঠনের সময় বন্ধন সৃষ্টিকারী ইলেকট্রন জোড়াকে নিজের দিকে আকর্ষণ করার ক্ষমতা। সহজ ভাষায় বলতে গেলে, তড়িৎ ঋণাত্মকতা হলো ইলেকট্রন আকর্ষণ করার প্রবণতাকেই মৌলের তড়িৎঋণাত্মকতা বলে।
ঊপর থেকে নিচে যাওয়ার সময়ে গ্রুপ ১ মৌলগুলির বৈদ্যুতিক গুণগত পরিবর্তন – যখন আমরা ঊপর থেকে নিচে যাই, পরমাণুর আকার বাড়ে। তার পরিণামে ঊপর থেকে নিচে নিউক্লিয়াসের আকার বাড়তে পারে, তবে আকার বাড়ানোর সাথে সাথে ইলেকট্রন – প্রতিটি নিউক্লিয়াসের দ্বারা আকর্ষণ হ্রাস পায়। এ কারণে গ্রুপ ! মৌলগুলি যারা ঊপর থেকে নিচে যায়, তাদের বৈদ্যুতিক গুণগত ধারণকে অবশ্যই হ্রাস পায়।
4.10 তড়িৎ বিশ্লেষণের সময় কোন শক্তি রাসায়নিক বিক্রিয়া ঘটানোর জন্য ‘দায়ী? অম্লায়িত জলের তড়িৎ বিশ্লেষণের সময় ক্যাথোডে ও অ্যানোডে কী কী বিক্রিয়া সংঘটিত হয়?
উত্তর : অম্লায়িত জলের তড়িৎ বিশ্লেষণে সময় ক্যাথোড বিক্রিয়া – অ্যাসিড মিশ্রিত জলে তড়িৎ চলাচল করলে H+ আয়নগুলি ক্যাথোডে আকর্ষিত হয় এবং ক্যাথোডে প্রবেশ করে ইলেকট্রন গ্রহণ করে, প্রথমে হাইড্রোজেন পারমাণুতে পরিণত হয়। পরে দুটি হাইড্রোজেন পারমাণু যুক্ত হয়ে হাইড্রোজেন অণু পারমাণুতে পরিণত হয়, ফলে ক্যাথোডে হাইড্রোজেন গ্যাস মুক্ত হয়।
অম্লায়িত জলের তড়িৎ বিশ্লেষণে সময় ক্যাথোড বিক্রিয়া – H+ + e → H, H + H → H2(g)
অম্লায়িত জলের তড়িৎ বিশ্লেষণে সময় অ্যানোড বিক্রিয়া জলের বিয়োজনে উৎপন্ন অহাইড্রোক্সাইড (OH-) আয়নগুলি অ্যানোডে আকর্ষিত হয় এবং অ্যানোডে প্রবেশ করে ইলেকট্রন বর্জন করে, প্রথমে OH মূলকে পরিণত করে। পরে এই OH মূলক গুলি পরস্পরের সঙ্গে বিক্রিয়া করে হাইড্রোজেন অক্সিজেন (H2O) ও অক্সিজেন (O2) অণু উৎপন্ন করে। উৎপন্ন O2 গ্যাস অ্যানোডে মুক্ত হয়।
অম্লায়িত জলের তড়িৎ বিশ্লেষণে সময় অ্যানোড বিক্রিয়া – OH– – e → OH, 40H → 2H2O + O2
4.11 স্পর্শ পদ্ধতিতে SO2 থেকে SO3-এর শিল্প উৎপাদনের শর্তসহ সমিত রাসায়নিক সমীকরণ লেখো। উৎপন্ন SO3 থেকে কীভাবে H2SO4 প্রস্তুত করা হয়?
উত্তর : স্পর্শ পদ্ধতিতে SO2 থেকে SO3-এর শিল্প উৎপাদনের শর্ত – এটার জন্য প্রথমে SO2 গ্যাসকে পরিষ্কার করে অধিক ধূলিকণা ও বায়ু থেকে মুক্ত করে নেয়া হয়। তারপরে এই গ্যাসকে 450°C উষ্ণতায় এবং 1.5 বায়ুমণ্ডলীয় চাপে, উত্তপ্ত প্লাটিনাম, চূর্ণাবৃত এসবেস্টস বা ভ্যানাডিয়াম পেন্টক্সাইড (V2O5) অনুঘটকের সাথে প্রতিক্রিয়ায় নেয়া হয়। এর ফলে SO2 গ্যাসের অক্সিজেন দ্বারা পরিণত হয়ে সালফারট্রাইঅক্সাইড (SO3) তৈরি হয়।
রাসায়নিক বিক্রিয়া – 2SO2 (g) + O2 (g) ⇌ 2SO3 (g) + 45 kcal
SO3 থেকে H2SO4 তৈরি করার পদ্ধতি হলো প্রথমে উৎপন্ন SO3 গ্যাসকে ঠাণ্ডা করে একটি কোক খণ্ড পূর্ন শোষক স্তম্ভে পাঠানো হয়। এই স্তম্ভে অধিকাংশ গাঢ় H2SO4 শোষন হয় যা 98% পরিমাণে থাকে। এরপর এই শোষিত H2SO4 থেকে পাইরো সালফিউরিক অ্যাসিড (H2S2O7) বা ওলিয়াম তৈরি হয়।
SO3 (g) + H2SO4 (I) → H2S2O7 (I)
পরবর্তী ধাপে, ওলিয়ামের সাথে পরিমাণ মত পাতিত জল মিশিয়ে শোধন করা হয় যাতে 98% গাঢ় H2SO4 প্রস্তুত করা যায়।
H2S2O7 (I) + H2O (I) → 2H2SO4 (I)
4.12 আসিটিলিনের সঙ্গে হাইড্রোজেনের যুত বিক্রিয়ার শর্ত উল্লেখ সহ সমিত রাসায়নিক সমীকরণ লেখো। LPG – এর একটি ব্যাবহার উল্লেখ করো।
উত্তর : আসিটিলিনের সঙ্গে হাইড্রোজেনের যুত বিক্রিয়ার শর্ত – 200°C উষ্ণতায় নিকেল চূর্ণ অনুঘটকের উপস্থিতিতে অথবা সাধারণ চাপ ও উষ্ণতায় নিকেল, বিচূর্ণ প্লাটিনাম বা প্যালাডিয়াম অনুঘটকের উপস্থিতিতে আসিটিলিন ও হাইড্রোজেনের বিক্রিয়ায় প্রথম ধাপে অণু হাইড্রোজেন যুক্ত হয়েইথিলিন এবং দ্বিতীয় ধাপে আরও 1 অণু হাইড্রোজেন যুক্ত হয়ে ইথেন উৎপন্ন হয়।
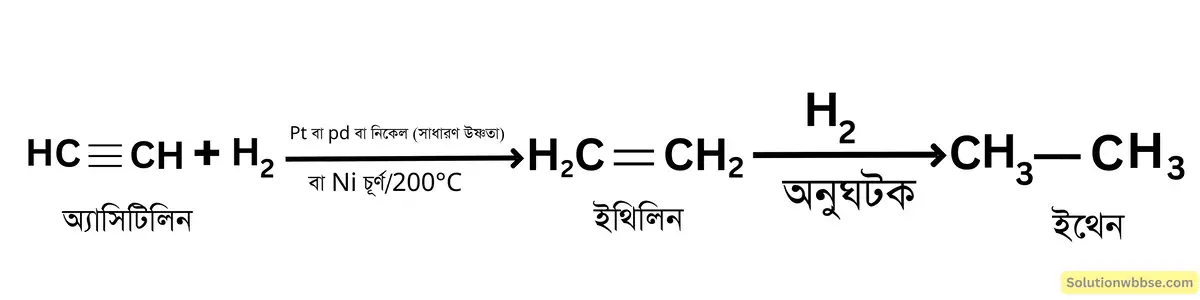
রান্নার কাজে LPG – গ্যাস ব্যাবহার করা হয়।
দ্বিতীয় অংশ – প্রাকৃতিকভাবে উপস্থিত জৈব পলিমারগুলি বিভিন্ন অণুজীব যেমন – ব্যাকটেরিয়া, ছত্রাক প্রভৃতি থেকে নিঃসৃত উৎসেচক দ্বারা বিশ্লিষ্ট হয় এবং CO2, H2O ইত্যাদির সঙ্গে সরল যৌগে রূপান্তরিত হয়।
অথবা
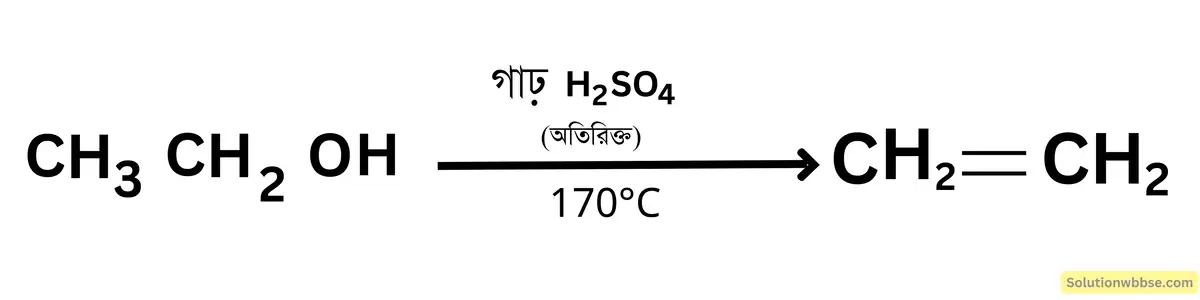
কীভারে পরিবর্তিত করবে?
CH3 CH2 OH → CH2 = CH2
প্রকৃতিতে জৈব পলিমার প্রোটিনের বায়োডিগ্রেডেশন হয় কীভাবে?
উত্তর : CH3CH2OH (ইথানল) – যখন এটি অতিরিক্ত পরিমাণ গাঢ় H2SO4 এর সাথে মিশে 170°C উষ্ণতায় উত্তপ্ত হয়, তখন এটি নিরুদিত হয় এবং ইথিন বা ইথিলিন উৎপন্ন হয়।
দ্বিতীয়ত, প্রাকৃতিকভাবে উপস্থিত জৈব পলিমারগুলি বিভিন্ন অণুজীব যেমন – ব্যাকটেরিয়া, ছত্রাক প্রভৃতি থেকে নিঃসৃত উৎসেচক দ্বারা বিশ্লিষ্ট হয় এবং CO2, H2O ইত্যাদির সঙ্গে সরল যৌগে রূপান্তরিত হয়।
এই ব্লগ পোস্টে আমরা মাধ্যমিক পরীক্ষার পুরোনো বছরের প্রশ্ন ও উত্তর নিয়ে আলোচনা করেছি। বিশেষ করে, আমরা ২০১৭ সালের মাধ্যমিক ভৌত বিজ্ঞান পরীক্ষার প্রশ্ন ও উত্তর বিশ্লেষণ করেছি।
মাধ্যমিক পরীক্ষায় আগের বছরের প্রশ্নগুলি বিশ্লেষণ করা শিক্ষার্থীদের জন্য বেশ গুরুত্বপূর্ণ কারণ এটি পরীক্ষার ধরন, প্রশ্নের মান এবং পরীক্ষার প্রস্তুতির জন্য প্রয়োজনীয় দিকগুলি সম্পর্কে ধারণা দেয়। ২০১৭ সালের প্রশ্নপত্র বিশেষ করে গুরুত্বপূর্ণ কারণ এটি বর্তমান পাঠ্যক্রমের সাথে সামঞ্জস্যপূর্ণ এবং পরবর্তী বছরের পরীক্ষায়ও অনুরূপ প্রশ্ন আসার সম্ভাবনা রয়েছে।






মন্তব্য করুন